3.2. Ранние осложнения со стороны брюшной полости
3.2.1. Внутрибрюшное кровотечение
Это осложнение встречается в 0,1-0,3% случаев и является результатом недостаточно прочной перевязки артерии отростка или по причине соскальзывания лигатуры с культи сосуда брыжейки отростка. Следовательно, кровотечение в какой-то мере является виной хирурга.
Часто кровотечение бывает не профузным, вследствие чего в первое время (1-5 часов) может протекать скрытно и вызывать определенные трудности для диагностики. Поэтому во всех случаях, при отсутствии полной уверенности в хорошем гемостазе, целесообразно прибегать к использованию тампонов и дренажных трубок с целью как можно раньше обнаружить внутрибрюшное кровотечение.
Классификация внутрибрюшного кровотечения (с учетом объема):
1 степень - кровопотеря до 500 мл (10-15% от ОЦК);
2 степень - от 500 до 1000 мл (16-20% от ОЦК);
3 степень - от 1 000 до 1500 мл (21-30% от ОЦК);
4 степень - более 1500 мл (свыше 30% от ОЦК);
Первыми симптомами внутрибрюшного кровотечения являются нарастающая слабость, заметная бледность кожного покрова и слизистых, сухость в ротовой полости, умеренная жажда, тахикардия, снижение АД. Наличие крови в брюшной полости проявляется перитонизмом, определяется симптом Кулленкампфа (мягкий живот, болезненная пальпация и значительное усиление болей при быстром отнятии руки) и укорочение перкуторного звука в отлогих местах брюшной полости. Появляется тупая боль в правой половине живота с иррадиацией в правое плечо и надключичную область. На этом фоне ведущим симптомом становится паралитическая кишечная непроходимость, ошибочно воспринимающаяся как послеоперационный парез. В анализе крови обнаруживается уменьшение эритроцитов, гемоглобина и гематокрита. УЗИ брюшной полости практически в 100% случаев верифицируют послеоперационное внутрибрюшное кровотечение.
Диагностика. В отсутствие УЗИ и сомнение в наличии кровотечения, следует через рану, предварительно сняв 1-2 шва с кожи и апоневроза наружной косой мышцы, осторожно провести в брюшную полость металлический или тонкий резиновый катетер. Поступление из брюшной полости кровянистого отделяемого убеждает в наличии данного осложнения.
Лечение. При малейшем подозрении на послеоперационное внутрибрюшное кровотечение показана повторная срединная лапаротомия, остановка кровотечения и дренирование брюшной полости. Восполнение ОЦК и переливание препаратов крови проводится по показаниям в зависимости от количества потерянной крови.
3.2.2. Инфильтрат брюшной полости
Возникает в 0,3-0,44 %. Причина: инфицирование окружающих тканей (при инвагинации культи отростка; при наложении кисетного шва из-за прокола кишечной стенки); оставление в брюшной полости части отростка (верхушки, части серозного покрова); инородное тело брюшной полости; образование (гематомы в брюшной полости; недостаточное дренирование или отказ от дренирования брюшной полости.
Клиническая картина: на 3-5 сутки после операции, отмечается усиление боли в правой подвздошной области, особенно при движении; при пальпации определяется умеренно болезненное уплотнение в правой подвздошной области (необходимо границы инфильтрата обозначить на коже для контроля над изменением eгo объема); субфебрильная гипертермия тела. В клиническом анализе крови отмечается незначительный лейкоцитоз.
Лечение: постельный режим; противовоспалительная (диклофенак, найз и др.) и антибактериальная терапия; физиотерапевтические процедуры (УВЧ); теплые микроклизмы (у женщин спринцевание) с ромашкой (50-75 мл) 2 раза в день.
Профилактика: удаление всех некротизированных тканей из брюшной полости, использование современного шовного материала, бережное отношение к тканям.
Исходы: рассасывание инфильтрата (92%); образование абсцесса брюшной полости (5%); развитие перитонита (3%).
3.2.3. Абсцесс культи червеобразного отростка
Осложняет течение послеоперационного периода в 0,01 %. Причина: оставление длинной культи черверобразного отростка (>0,5 см); недостаточная обработка просвета культи спиртом или спиртовым раствором йода, перед погружением его в кисетный шов; широкое наложение кисетного шва, что образует после его затягивания, большой «слепой мешок».
Клиническая картина: чаще на 4-8 сутки после операции, усиливается боль в правой подвздошной области, определяется опухолевидное образование, симптомы интоксикации. При прорыве абсцесса культи в просвет слепой кишки все симптомы моментально проходят, в этот день у больного возможен однократный жидкий стул. Если же абсцесс культи прорывает в брюшную полость, то развивается клиника перитонита (см. Послеоперационный перитонит).
Лечение: выжидательная тактика на фоне антибиотикотерапии (антибиотики выбора: цефалоспорины II-III генерации + метронидазол). При развитие перитонита, показана релапаротомия срединным доступом.
Диагностика. Возможно использование УЗИ, КТ и МРТ.
Профилактика: соблюдение оперативной техники аппендэктомии (культя червеобразного отростка должна быть длинной не более 0,5 см; кисетный шов накладывается отступя от основания отростка не более 0,7-1,0 см) и всех вышеописанных мер асептики.
3.2.4. Абсцессы брюшной полости
Абсцесс аппендикулярный представляет собой осложнение деструктивных форм острого аппендицита (и обычно возникает в 2% всех видов острого аппендицита). Первоначально формируется аппендикулярный инфильтрат, а затем последний либо рассасывается под влиянием консервативной терапии, либо, несмотря на соответствующее лечение, абсцедирует (Рис. 10).
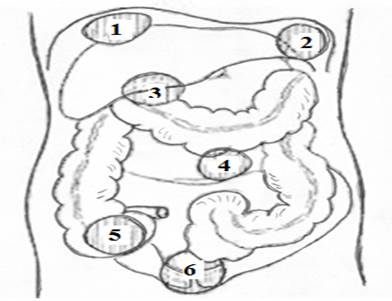
Рисунок 10. Схема локализации аппендикулярных абсцессов брюшной полости: 1 – в поддиафрагмальной области справа; 2 – в поддиафрагмальной области слева; 3 – в подпеченочном пространстве; 4 – межпетельный абсцесс; 5 – в подвздошной ямке; 6 - в малом тазу.[10]
3.2.4.1. Абсцесс в подвздошной ямке
При деструктивном перфоративном аппендиците зона расположения отростка является местом потенциальной инфекции и трудно полагать, что патогенная флора во время операции может быть полностью удалена. Основными причинами образования абсцесса в этой области, является оставление фекальных масс или участка червеобразного отростка. Особенно опасно развитие абсцесса при зашитой наглухо брюшной полости. Абсцесс из подвздошной ямки может прорваться в свободную брюшную полость и привести к распространенному перитониту. Встречается в 76-89% случаев от всех абсцессов брюшной полости.
Клиническая картина: на 2-3 сутки после операции, отмечается усиление болей в животе в проекции послеоперационной раны, при этом сама рана малоболезненна, без признаков воспаления. Симптомы раздражения брюшины отрицательны, наблюдается повышение температуры тела до фебрильных цифр (38О-40ОС), тахикардия, проблемы со стулом (чаще запоры). При абсцессе объемом более 100 мл присоединяется выраженный синдром интоксикации (нарастание слабости, сухость в ротовой полости, жажда, адинамия и др.). В клиническом анализе крови появляется лейкоцитоз с нейтрофильным сдвигом формулы влево (палочкоядерных 25-40%).
В диагностике абсцесса помогают УЗИ брюшной полости - жидкостное образование в подвздошной ямке (Рис. 11) и КТ (Рис.12).
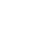
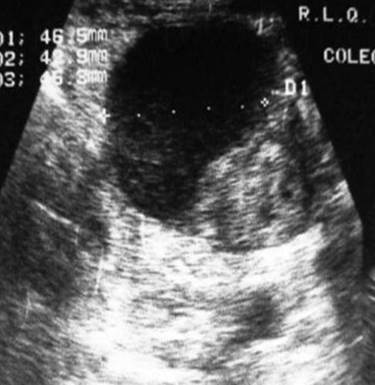
Рисунок 11. УЗИ. Абсцесс в подвздошной ямке.[11]

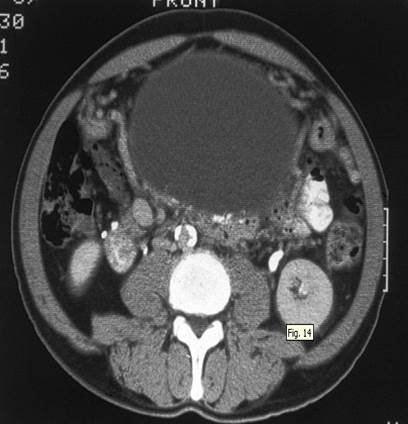
Рисунок 12. Компьютерная томография. Гигантский абсцесс в подвздошной ямке.[12]
Лечение: чаще всего достаточно релапаротомии путем снятия швов с раны, эвакуация гноя, промывание гнойной полости и ее дренирование через рану.
Профилактикой образования абсцессов в зоне отростка являются: тщательный гемостаз, удаление некротических тканей, а когда это не удается, следует выполнить дренирование этой области по самому короткому пути, через рану.
3.2.4.2. Тазовый абсцесс
Доля тазового абсцесса 5-7%. Причина: неполное удаление гноя или инфицированного экссудата из полости малого таза. Скопление инфицированной жидкости в полости мaлого таза может быть при расположении деструктивного аппендикса в тазу, при стекании инфицированной жидкости в полость таза из верхних отдeлов брюшной полости, осумковании экссудата при перитоните, тампонаде брюшной полости марлевыми тампонами. Тазовые абсцессы могут образоваться в результате кровотечения во время операции из различных мелких сосудов, скопления этой крови в малом тазу и последующего ее инфицирования.
Клиническая картина: на 5-7 день на фоне благополучного течения, появляются боли внизу живота с иррадиацией ее в промежность и прямую кишку, повышение температуры тела до фебрильных цифр (38º-40ºС), тахикардия, синдром интоксикации (нарастание слабости, сухость в ротовой полости, жажда, адинамия и др.), нарастание боли над лобком, без симптомов раздражения брюшины. Определяется разница ректальной и подмышечной температуры более чем на 1ºС. Появляются и прогрессируют симптомы нарушения функции тазовых opганов (частое и затрудненное мочеиспускание, тенезмы, выделение жидкого стула со слизью). При исследовании per r ectum (per vagiпum у женщин) определяются нависание (Рис. 13) и резкая болезненность передней стенки прямой кишки (задней стенки влагалища), инфильтрация и симптом флюктуации, снижение тонуса сфинктера прямой кишки.
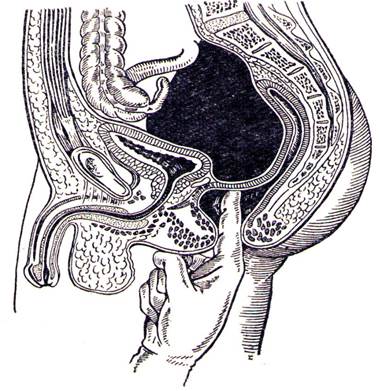
Рисунок 13. Исследование per r ec t um. Определяется нависание передней стенки прямой кишки.[13]
Позже возможно появление картины кишечной непроходимости с клиническими (вздутие живота, не отхождение стула и газов, тошнота, рвота) и рентгенологическими симптомами (пневматоз, чаши Клойбера). В клиническом анализе крови появляется лейкоцитоз свыше 14-20×109 с нейтрофильным сдвигом формулы влево (палочкоядерных 25-45%).
Тазовый абсцесс может самостоятельно вскрыться в брюшную полость, прямую кишку, мочевой пузырь, во влагалище (Рис. 14).
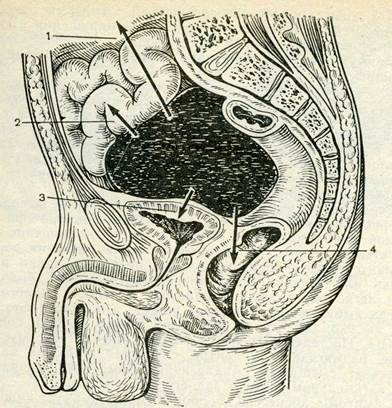
Рисунок 14. Схема путей возможного прорыва гноя: 1 и 2 – в брюшную полость; 3 – в мочевой пузырь; 4 – в прямую кишку.[14]
Диагностика. При УЗИ органов малого таза ректальным (влагалищным) датчиком четко определяется жидкостное образование в малом тазу.
Лечение: оперативное. Вскрытие гнойника проводят через переднюю стенку прямой кишки (впервые предложил М. Jaboulay в 1895 году), либо, через задний свод влагалища у женщин. Гнойник в области максимальной флюктуации пунктируется толстой иглой, получают гной, затем по игле, остроконечным скальпелем рассекаю переднюю стенку прямой кишки (или влагалища), разрез длинной до 1,5 см. Эвакуируют гной, а полость гнойника дренируют толстой силиконовой трубкой, которую фиксируют к слизистой прямой кишки (либо влагалища) кетгутом. Больному в постели придается полусидячее положение, назначают антибиотики и ежедневно 4-5 раз промывают полость абсцесса раствором антисептика (фурацилин, хлоргексидин и т.п.). Дренажную трубку убирают из 3-4 день (Рис. 15).
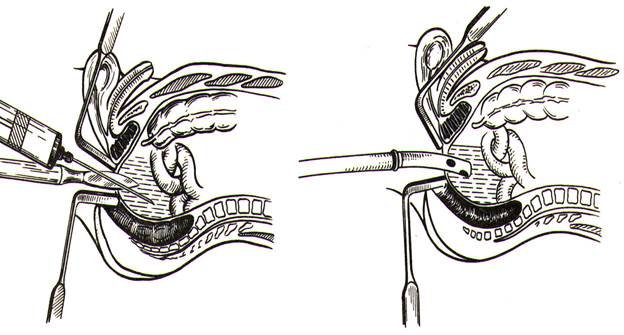
Рисунок 15. Вскрытие и дренирование абсцесса в малом тазу через прямую кишку.[15]
Профилактика: соблюдение правил асептики и антисептики во время операции, тщательный гемостаз и удаление экссудата из брюшной полости, антибиотикопрофилактика.
3.2.4.3. Межпетельный абсцесс
Возникает в 0,01 % случаев на 4-6 сутки после операции, пройдя в своем развитии стадию инфильтрации.
Причина: неполное удаление гноя или инфицированного экссудата, некротических тканей из брюшной полости. Скопление инфицированной жидкости в брюшной полости возможно при отсутствии дренирования брюшной полости после операции, раннем удалении дренажа, технически неправильно выполненном дренировании брюшной полости, недостаточной санации брюшной полости.
Клиническая картина: на 4-6 сутки после операции, наблюдается усиление болей в животе, нередко схваткообразного характера, повышение температуры тела до фебрильных цифр, тахикардия, синдром интоксикации (сухость во рту, жажда, адинамия и др.), появление симптомов раздражения брюшины. При пальпации в брюшной полости зачастую определяется опухолевидное образование. Далее может развиться клиника кишечной непроходимости с соответствующей клинико-рентгенологической картиной. В клиническом анализе крови появляется выраженный лейкоцитоз с нейтрофильным сдвигом влево.
В диагностике абсцесса помогают УЗИ брюшной полости (межпетлевые жидкостные образования, нередко с четкой капсулой) и КТ.
Лечение: оперативное. Срединная лапаротомия, вскрытие гнойника, удаление гноя, санация и дренирование брюшной полости, декомпрессия кишечника.
Профилактика: соблюдение правил асептики и антисептики во время операции, максимальное удаление экссудата и некротических тканей из брюшной полости, антибиотикопрофилактика.
3.2.4.4. Поддиафрагмальный абсцесс
Встречается в 0,005 %. Причинами служат: неполное удаление гноя или инфицированного экссудата из брюшной полости. Скопление инфицированной жидкости в правом поддиафрагмальном пространстве возможно при подпеченочном расположении деструктивно измененного червеобразного отростка; при неправильной санации брюшной полости после перитонита, раннем удалении дренажа, технически неправильно выполненном дренировании брюшной полости; как следствие пилефлебита.
Клиническая картина: обычно на 5-7 сутки после операции, появляются интенсивные боли в правом подреберье, усиливающиеся на вдохе; резкая болезненность при пальпации правого подреберья, где возможно определение опухолевидного образования; нарастающие симптомы интоксикации (повышение температуры тела до фебрильных цифр, тахикардия, сухость во рту, жажда, адинамия и др.). Присоединяется сухой мучительный кашель (симптом А.А. Троянова, 1896), больные принимают вынужденное положение тела - лежа на правом боку с поджатыми ногами; наблюдается выпячивание правого бока (симптом В.Ф. Войно-Ясинецкого, 1946), также определяется боль в животе при надавливании на нижние ребра справа (симптом М.М. Крюкова, 1913).
Диагностика. Рентгенологическими симптомами поддиафрагмального абсцесса справа являются: высокое стояние правого купола диафрагмы; малая подвижность купола диафрагмы; под диафрагмой возможен газовый пузырь с уровнем жидкости (уровень жидкости смещается при смене положения тела больного), определяется содружественный реактивный плеврит и опущение тени печени (Рис. 16).
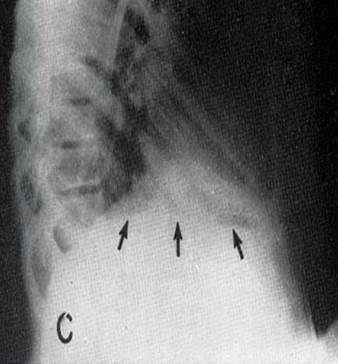

Рисунок 16. Рентгенологическая картина поддиафрагмального абсцесса.[16]
В диагностике существенную помощь оказывают УЗИ (Рис. 17) и КТ.
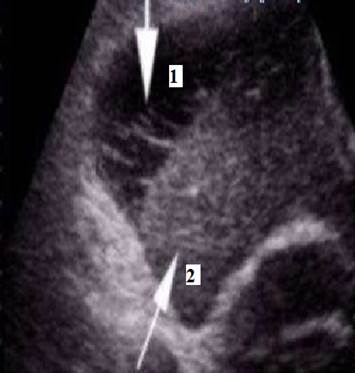
Рисунок 17. УЗИ. Поддиафрагмальный абсцесс справа: 1 – абсцесс; 2 – печень.[17]
Лечение: оперативное. Основными доступами к поддиафрагмальным абсцессам являются - лапаротомные внеплевральные. Внеплевральные доступы хорошо переносятся больными, так как не сопровождаются нарушениями дыхания и исключают риск развития эмпиемы плевры.
При гнойниках, расположенных ближе к передней брюшной стенке (над V-VI сегментами), разрез мягких тканей передней брюшной стенки производится вдоль правой реберной дуги до IX или X ребра от наружного края прямой мышцы живота до передней подмышечной линии, и производится отделение брюшины от реберной дуги и диафрагмы тупым путем на всем протяжении, пока не будет достигнута полость абсцесса. Гнойник пунктируют и по игле вскрывают, гной эвакуируют, полость гнойника промывают антисептиками, затем в него вводят 2-3 двухпросветные дренажные трубки и выводят их на боковую поверхность брюшной стенки, желательно через отдельный разрез в минимально низком месте, по отношению к полости абсцесса, по средней или задней подмышечной линии (Рис. 18). В дальнейшем проводится ее проточно-аспирационная санация.
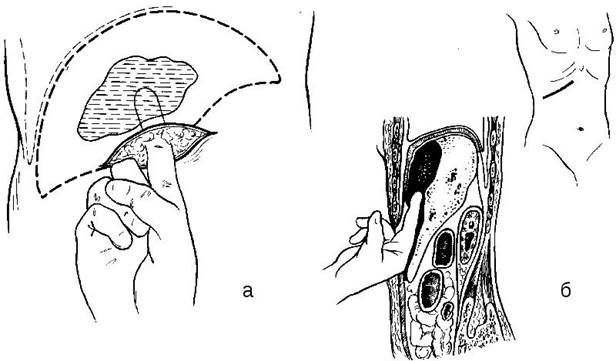
Рисунок 18. Внебрюшинный доступ к абсцессу в правом поддиафрагмальном пространстве: а – вид спереди; б – вид с боку.[18]
Применительно к гнойникам, расположенным в задней части поддиафрагмального пространства (над VII-VIII сегментами), обычно используют доступ A.B. Мельникова. При этом разрез длинной 5-6 см производят по ходу X ребра, между передней и задней подмышечными линиями с последующей поднадкостничной резекцией ребра на протяжении 10-12 см. После резекции ребра производят пункцию поддиафрагмального пространства толстой иглой и после получения гноя, не вынимая иглы, вскрывают абсцесс по игле. Если реберно-диафрагмальный синус плевры мешает рассечению диафрагмы, хирург тупо мобилизует его кверху. После эвакуации гноя, полость абсцесса обследуют пальцем, промывают раствором антисептиков и дренируют 2-3 двухпросветными трубками для проточно-аспирационной санации.
В редких случаях доступ к абсцессам производят посредством верхне-срединной лапаротомии, при этом поддиафрагмальную область прежде обкладывают пеленками или марлевыми салфетками с целью не допустить попадания гноя в брюшную полость. Гнойники вскрываются посредством тупого разделения передне-верхней поверхности правой доли печени и диафрагмы. Полость абсцесса также промывается растворами антисептиков и дренируется 2-3 двухпросветными трубками с выведением их на переднюю брюшную стенку через отдельные контрапертуры в правых боковых отделах живота, по средней или задней подмышечной линии. Нередко этим больным выполняется программная санационная релапаротомия (через 48-72 часа) с ревизией полости поддиафрагмального абсцесса, редренирования.
В настоящее время все шире применяется пункционное дренирование абсцессов под контролем УЗИ, однако в случаях неадекватного дренирования (множественные перемычки между полостями абсцессов), переходят на лапаротомные внеплевральные доступы.
3.2.5. Послеоперационный перитонит
Встречается в 0,4-0,7% случаев. Причиной развития послеоперационного перитонита является кишечное содержимое, попавшее в брюшную полость во время операции в результате разрыва напряженного отростка при его удалении; грубых манипуляций во время отделения сальника, прикрывающего перфоративное отверстие; выхода гноя в свободную брюшную полость при разделении аппендикулярного
инфильтрата или абсцесса.
Однако перитонит может развиться и вследствие технических погрешностей:
- плохого осушивания (санации) брюшной полости от гнойного экссудата;
- кровотечения в брюшную полость с последующим нагноением;
- несостоятельности швов культи;
- сквозного прокола стенки толстой кишки при наложении кисетного шва;
- формирования абсцесса в правой подвздошной области с последующим прорывом eгo в брюшную полость;
- неправильного выбора способа дренирования брюшной полости;
- отказа от дренирования брюшной полости;
- оставления в брюшной полости инородных тел.
Клиническая картина послеоперационного перитонита отличается своеобразным тeчением, атипичностью и бессимптомностью, что обусловлено применением обезболивающих средств и антибактериальных препаратов после операции. Такой перитонит, обычно не дает яркой клинической картины, как это бывает при перфорации червеобразного отростка или прорыве аппендикулярного абсцесса, поэтому его часто своевременно не диагностируют и не принимают соответствующих мер.
Основным клиническим проявлением послеоперационного перитонита является боль в животе, однако она не столь интенсивна, как при перфорации червеобразного отростка, носит постоянный характер и имеет тенденцию к усилению. Боль чаще начинается в правой подвздошной области, затем принимает более разлитой характер. У некоторых больных этот симптом менее выражен, доминируют резкое вздутие живота и чувство распирания в брюшной полости. Рвота, тошнота являются почти постоянными симптомами послеоперационного перитонита. Нередко больного беспокоит икота, не отходят газы и кал. Характерен внешний вид больного: лицо бледное с сероватым оттенком, позже – заостренные черты лица, адинамия. Появляются бессонница, частый пульс, артериальное давление снижается. Несоответствие частоты пульса и температуры тела является характерным признаком перитонита.
В ранней стадии послеоперационного перитонита отмечается напряжение мышц брюшной стенки, затем этот признак становится менее выраженным, преобладает вздутие брюшной стенки с последующей картиной паралитической кишечной непроходимости. Прекращается кишечная перистальтика, появляется шум плеска в брюшной полости. Выражен симптом Щеткина-Блюмберга. При пальцевом исследовании через прямую кишку можно определить болезненные места брюшины или нависание передней стенки прямой кишки, указывающее на скопление экссудата в малом тазу. Характерна для перитонита картина крови; динамическое наблюдение за ней при развивающемся перитоните показывает прогрессивное увеличение количества лейкоцитов (до 30-35×109) и нейтрофильный сдвиг влево (палочкоядерные до 35-55%). В редких случаях, в большей степени у пациентов пожилого и старческого возраста, изменения в крови при перитоните могут оставаться минимальными.
В плане инструментальной диагностики, незаменимым является УЗИ брюшной полости (парез кишечника, утолщение стенки кишки, наличие в брюшной полости неоднородной жидкости с осадком, визуализация свободно плавающих в жидкости нитей фибрина).
Лечение. При развитии перитонита после аппендэктомии, только ранняя релапаротомия спасает больного. Повторное оперативное вмешательство проводится с использованием широкого срединного разреза брюшной стенки. Первичный очаг инфекции устраняется, выполняется санация брюшной полости и ее широкое дренирование (см. Перфорация червеобразного отростка, перитонит). При выраженном парезе кишечника с большим количеством депонированных в нем жидкости и газа, должна быть выполнена декомпрессия кишечника, с целью быстрейшего купирования синдрома кишечной недостаточности и уменьшения компартмент-синдрома (повышенного внутрибрюшного давления).
После операции обязательна массивная антибактериальная терапия (2-3 антибиотика, в т.ч. с применением антибиотиков резерва), дезинтоксикационная терапия, раннее восстановление моторно-эвакуаторной функции кишечника, коррекция белкового обмена и водно-электролитного баланса. При необходимости применяются все методы экстракорпоральной детоксикации (плазмоферез, гемосорбция и т.д.). В запущенных случаях больным программируются санационные релапаротомии.
Профилактика: правильная техника выполнения операции.
3.2.6. Флегмона забрюшинной клетчатки
Встречается в 0,01-0,02 %. Причина: развивается при выраженной деструкции червеобразного отростка при peтpoперитонеальном расположении или при прорыве ретроцекального абсцесса в забрюшинное пространство; возможно развитие флегмоны через инфицированную брыжеечку отростка.
Клиническая картина: на 3-4 сутки после операции, отмечается постепенное усиление боли в животе и поясничной области, гипертермия, озноб, возможно пальпирование инфильтрата в правой подвздошной области без четких границ, положительный псоас-симптом (симптом поясничной мышцы) – при поднимании выпрямленной ноги появляется сгибательная контрактура и наружная ротация бедра, наблюдается отек мягких тканей правой поясничной области, боль при пальпации правой поясничной и правой подвздошной областей, при этом симптомы раздражения брюшины сомнительны. Нарастают патологические изменения в клинических анализах крови (лейкоцитоз, нейтрофильный сдвиг влево) и мочи (лейкоурия). Гной, распространяясь по межфасциальным пространствам и по m . il eopsoas, может образовывать затеки на бедро и клетчатку малого таза.
Диагностика. УЗИ позволяет проводить локальную диагностику распространения гнойного процесса и наметить линии для более рационального доступа к ним. В сомнительных случаях возможно выполнение КТ.
Лечение: оперативное. Вскрытие забрюшинного пространства осуществляется поясничными разрезами (Рис. 19), либо, по точкам намеченным врачом УЗИ-диагностики. Приозводят удаление некротических тканей и дренирование зоны поражения.
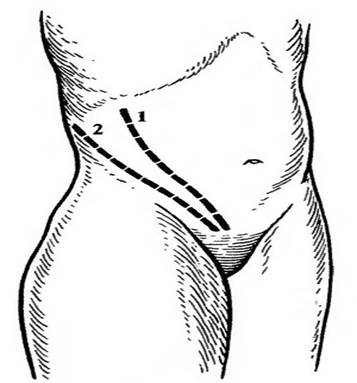
Рисунок 19. Разрезы для вскрытия забрюшинных флегмон: 1 - разрез по Пирогову; 2 - разрез по Шевкуненко.[19]
Антибиотикотерапия, дезинтоксикационная терапия, раннее восстановление функции ЖКТ, коррекция белкового обмена и водноэлектролитного баланса. При необходимости применяются методы экстра-
корпоральной детоксикации.
Профилактика: технически правильное выполнение первичной операции. Если при ревизии слепой кишки отросток и его основание не обнаружены, а выявлена забрюшинная флегмона, то необходимо ушить наглухо разрез и вскрыть забрюшинное пространство доступом Пирогова, выполнить аппендэктомию, дренировать забрюшинное пространство. При этом купол слепой кишки точно так же выводится в рану, отыскивается основание отростка, и только лишь потом проводится непосредственно аппендэктомия.
Если же основание отростка лежит в брюшной полости, а верхушка в забрюшинной клетчатке, которая уже деструктивно изменена, показана ретроградная аппендэктомия по всем вышеописанным правилам.
Дренирование забрюшинного пространства показано всегда, при этом следует обратить внимание на то, чтобы были дренированы все затеки и отлогие места.
3.2.7. Пилефлебит
Одним из самых редких (0,0001%) осложнений острого деструктивного аппендицита является пилефлебит - септический тромбофлебит брыжеечных и воротной вен. Летальность при развитии этого осложнения близка к 100%.
Причиной возникновения пилефлебита, как правило, является перфорация стенки червеобразного отростка по брыжеечному краю с развитием флегмоны или абсцесса брыжеечки, откуда септические тромбы попадают или заносятся током крови в брыжеечные вены, вызывая тромбофлебит воротной вены и ее печеночных разветвлений с образованием в дальнейшем множественных абсцессов в печени (Рис. 20).
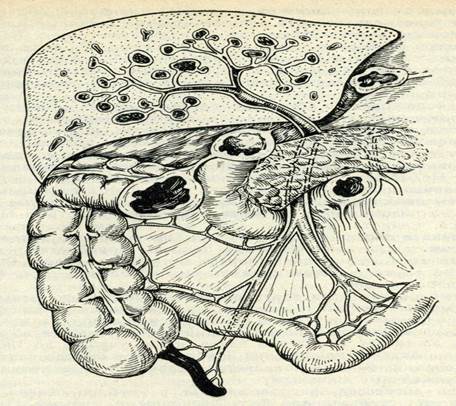
Рисунок 20. Схематично изображены пути распространения гнойного тромбофлебита при остром аппендиците и формирование абсцессов печени[20].
При развитии этого осложнения после аппендэктомии, спустя несколько часов, а иногда 2-4 суток (реже 7 суток), повышается температура, принимая гектический характер, присоединяются ознобы. Живот остается мягким, болезненным при пальпации правом подреберье, определяется увеличение печени. Вскоре удается отметить легкую желтушность кожного покрова и слизистых оболочек. Лабораторные исследования крови обнаруживают выраженный лейкоцитоз (25-30×109) с резким нейтрофильным сдвигом влево (палочкоядерных 35-60%), билирубинемию (>50 мкмоль/л), умеренное повышение показателей трансаминаз (АлАт > 60-90 Ед/л). ССВР свидетельствует о сепсисе. Клинико-лабораторная диагностика пилефлебита в ранние сроки чрезвычайно трудна, так как нет ни одного характерного признака для этого осложнения.
Диагностика. При УЗИ подтверждается гепатоспленомегалия, причем в первые сутки от начала заболевания, возможно без наличия очаговых изменений в печени. Однако уже через 36-48 часов будут определяться множественные внутрипеченочные абсцессы. При допплеровском исследовании обнаруживается нарушение кровотока по ветвям воротной вены. Выполняется трехкратный посев крови на бактериологические среды для определения ее стерильности.
Значительно реже, пилефлебит встречается при деструктивном аппендиците до операции. Клинические проявления заболевания в таких случаях характеризуются «аппендикулярными» симптомами в начале заболевания с последующим стремительным развитием сепсиса и соответствующей лабораторно-сонографической картиной печеночно-почечной недостаточности. Лечение – экстренное оперативное вмешательство. Операция заключается в удалении червеобразного отростка и если обнаружены гнойная имбибиция брыжеечки и тромбированные вены червеобразного отростка и брыжеечки - дополнительное блокирование брыжеечной вены раствором новокаина с антибиотиками.
Медикаментозное лечение пилефлебита представляет чрезвычайно сложную задачу, так как речь фактически идет о развитии септического состояния. Сразу после установки диагноза назначается терапия, которая включает в себя антибиотики резерва (карбапенемы - меронем; цефалоспорины IV генерации – цефепим), антикоагулянты (гепарин, клексан и др.), антиагреганты (пентоксифиллин и др.), тромболитики (фибринолизин, урокиназа, стрептокиназа), привнесение иммунных комплексов (ронколейкин, пентаглобин и др.), антиоксиданты (цитофлавин и др.). Широко используются интракорпоральные (инфузионная терапия + форсированный диурез, реамберин, УФО-крови, лазерное облучение крови и др.) и экстракорпоральные (плазмоферез, гемосорбция) способы детоксикации.
Профилактика: своевременная аппендэктомия.
3.2.8. Ранняя спаечная послеоперационная острая кишечная непроходимость
Частота ранней послеоперационной острой кишечной непроходимости колеблется в пределах 0,1-2,5%. Основная причина – послеоперационный спаечный процесс.
Клиническая диагностика ранней острой кишечной непроходимости часто бывает затруднительной. Нередко ухудшение состояния больного объясняют послеоперационным парезом кишечника, пропуская ранние сроки оперативного лечения. Особенно сложно установить правильный диагноз, когда механическая кишечная непроходимость возникает на 2-3 день после операции. Основным и первым сигналом развития острой кишечной непроходимости в послеоперационном периоде является изменение характера боли в животе. Боль либо сразу принимает резкий схваткообразный характер, либо нарастает постепенно, а в дальнейшем также становится схваткообразной. Часто боль локализуется в области пупка, правой подвздошной области, сопровождается тошнотой, прогрессирующей рвотой, которая быстро принимает каловый характер. Наступает задержка отхождения кала и газов, а очистительная клизма не дает облегчения даже после отхождения каловых масс. Состояние больного быстро ухудшается, поведение его становится беспокойным, нарастает тахикардия. Наряду с болью, ухудшением общего состояния значительно изменяются местные симптомы: увеличивается вздутие живота, в ряде случаев наблюдается его асимметрия и видимая кишечная перистальтика во время болевой схватки, выявляется симптом Валя в зоне препятствия, причем в этой зоне иногда можно пальпировать нечеткий болезненный инфильтрат. При выслушивании живота в ранней фазе совершенно отчетливо определяются волнообразная звонкая перистальтика, симптомы - «падающая капля» и «шум плеска». В поздние сроки картина меняется: появляются мышечное напряжение, симптом Щеткина-Блюмберга, притупление в отлогих местах живота и «гробовое молчание» при выслушивании кишечника. При ректальном исследовании в поздней фазе сфинктер ослаблен, ампула балонообразно расширена. Со стороны крови в первые часы заболевания значительных изменений не отмечается. Обычно имеется небольшой лейкоцитоз, связанный с основным заболеванием. Позднее в крови отмечается уменьшение количества ионов Na+ и K+.
Диагностика. Большую ценность в ранней диагностике острой кишечной непроходимости имеет рентгенологическое обследование. Обзорная рентгенограмма брюшной полости во всех случаях констатирует появление чаш Клойбера в тонкой кишке, а позднее и в толстой (Рис. 21).
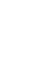

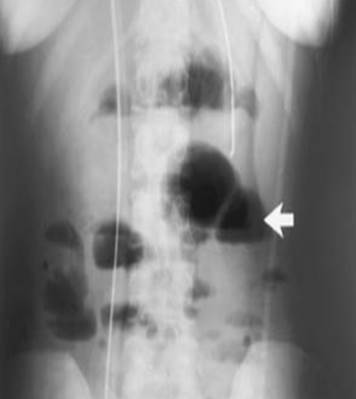
Рисунок 21. На обзорной рентгенограмме чаши Клойбера[21].
При УЗИ определяются расширенные петли кишки, утолщение ее стенки, депонирование в ней жидкости и газа, складчатость слизистой и «маятникообразная» перистальтика (Рис. 22).
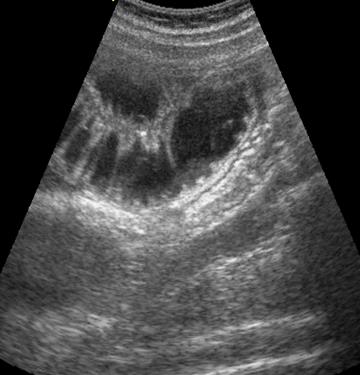
Рисунок 22. Ультразвуковая картина кишечной непроходимости[22].
При ухудшении состояния больного и подозрении на кишечную непроходимость следует в первую очередь применять активные консервативные мероприятия – постоянную аспирацию желудочного содержимого, очистительную клизму, парентеральное введение жидкостей. Если эти мероприятия дали положительный эффект, но рентгенологическая картина остается прежней или нарастает, показана срочная повторная операция.
Большой ошибкой являются чрезмерно длительное наблюдение и дальнейшая консервативная терапия у таких больных. Срок наблюдения не должен превышать 3-5 часов с момента появления признаков кишечной непроходимости.
Лечение оперативное. Выполняется срединная лапаротомия. При ревизии брюшной полости выявляют причины кишечной непроходимости, которыми чаще всего бывают инфильтраты в области операции или спайки, деформирующие петлю кишечника (перетяжки, перегибы) и создающие препятствие. После устранения причины кишечной непроходимости необходимо удалить избыточное содержимое из тонкой кишки, для этого используется интестинальный зонд Миллера-Эббота (см. Рис. 6). В случаях когда провести его не удалось, возможно нежное «сцеживание» в толстую кишку. Если при чрезмерном переполнении тонкой и растянутой толстой кишки и этот прием не дает успеха, то приходится прибегать к пункции тонкой кишки, которую нужно производить после наложения кисетного шва на стороне, противоположной брыжеечному краю. Опустевшие петли тонкой кишки обкладывают пеленками смоченными теплым физиологическим раствором (улучшает микроциркуляцию в ее стенке) и вводят новокаин 0,5% - 100 мл в ее брыжейку для обрыва болевого импульса, что в совокупности способствует быстрому восстановлению перистальтики. Наложение илеостомы при переполненном кишечнике обычно эффекта не дает.
Если во время операции хирург устанавливает нежизнеспособность петли кишки, показана ее резекция, которая производится обязательно с удалением не менее 30-40 см приводящей петли и 15–20 см отводящей петли кишечника (из-за особенностей кровоснабжения кишки).
Профилактика. При выполнении операции по поводу острого аппендицита хирург должен принять возможные профилактические меры против развития кишечной непроходимости. Они должны заключаться в следующем: широкий оперативный доступ к червеобразному отростку, исключающий грубую травматизацию брюшины и кишечника; ушивание всех десерозированных участков кишки и дефектов на брюшине. В послеоперационном периоде с первых дней, активное ведение больного и лечебная физкультура, являются эффективными мерами профилактики послеоперационной кишечной непроходимости.
3.2.9. Кишечные свищи
Не менее опасными осложнениями раннего послеоперационного периода при остром аппендиците являются кишечные свищи, которые встречаются в 0,002-0,004% случаев. Причинами образования кишечных свищей могут быть: прогрессирующий деструктивный процесс, распространяющийся с червеобразного отростка на слепую кишку (тифлит), обусловившим сложности при погружении культи червеобразного отростка в стенку слепой кишки; операционные технические ошибки при погружении культи отростка в стенку слепой кишки; не ушитые десерозированные участки кишок; различные другие послеоперационные осложнения (межкишечные абсцессы, забрюшинные флегмоны, эвентрация и пр.).
Локализация кишечных свищей при деструктивном аппендиците может быть различной, но преимущественно (95%) они возникают на слепой кишке, 90% из них или предлежащей петле подвздошной кишки - 10%. На подвздошной кишке свищи чаще возникают на расстоянии до 20 см проксимальнее илеоцекального угла, так как этот участок кишки кровоснабжается хуже других.
Классификация кишечных свищей:
- трубчатый, губовидный, газовый (свищевое точечное отверстие, из которого поступает только газ);
- наружный, внутренний, комбинированный;
- полный (наружу выделяется все кишечное содержимое), неполный (наружу выделяется лишь часть кишечного содержимого);
- тонкокишечный (высокий и низкий), толстокишечный;
- одиночный (одно- или двуствольный), множественный;
- каловый, слизистый, гнойный;
- неосложненный и осложненный (истощение, депрессия, мацерация, гнойная инфекция окружающих мягких тканей, дерматит, пролапс слизистой стенки кишки),
Отличительная особенность кишечных свищей состоит в том, что они не сопровождаются грануляциями.
Чаще кишечные свищи возникают на 5-10 день. Ранние сроки образования кишечных свищей свидетельствуют о том, что основной причиной их возникновения является деструктивный процесс в стенке слепой кишки.
Первые клинические проявления кишечных свищей зависит от механизма их образования. Если свищ образуется после аппендэктомии в результате прогрессирующего деструктивного процесса, переходящего на брюшину и забрюшинную клетчатку, клиническое течение характеризуется тяжелым общим состоянием с выраженной интоксикацией, интермиттирующей высокой температурой, изменениями в периферической крови (высокий лейкоцитоз с выраженным нейтрофильным сдвигом влево и исчезновением эозинофилов). К моменту открытия свища всегда наблюдается нагноение раны захватывающей все слои брюшной стенки.
Если кишечный свищ образуется вследствие расхождения швов культи отростка, при уже удаленных дренажах или сразу наглухо ушитой ране, то обычно через 4-7 дней после аппендэктомии, появляются боли в правой подвздошной области, там же, может определяется глубокий болезненный инфильтрат. Затем появляется клиника прободения полого органа: внезапное резкое ухудшение состояния больного на фоне относительного благополучия, частый пульс, острая боль в животе, локальное или распространенное резкое напряжение мышц живота.
В случаях, когда оперирующий хирург прогнозирует образование свища, он специально подводит тампоны к куполу слепой кишки. Тампонада и дренирование при этом являются спасением для больного, так как рано выявляют осложнение, чего не происходит при закрытии раны наглухо. В случае образования кишечного свища, тампоны, за счет сформировавшегося вокруг них спаечного процесса, предотвращают попадание кишечного содержимого в свободную брюшную полость. Клинически это проявляется лишь обнаружением содержимого кишки на перевязочном материале, отхождением газа через рану.
В ряде случаев кишечные свищи образуются поздно (свыше 14 дней), как следствие межкишечных абсцессов, забрюшинных и тазовых флегмон, вялотекущего перитонита.
Первыми признаками наружных кишечных свищей являются наличие на коже отверстий, через которые выделяется кишечное содержимое. При высоких тонкокишечных свищах оно жидкое, желто-зеленого цвета, пенящееся, с остатками непереваренной пищи. Содержимое низких тонкокишечных свищей более вязкое, а толстокишечных - оформленное. Наряду с выделением кала у больных с толстокишечными свищами наблюдается отхождение газов. Кожные покровы в окружности наружного отверстия свища мацерированы, изъязвлены. Больные с высокими длительно существующими тонкокищечными свищами обезвожены и истощены. Некоторые из них теряют до 25-50 % массы тела. Постоянно их беспокоит жажда.
Отмечаются сдвиги в нервно-психической сфере (бессонница, возбуждение, раздражительность или, наоборот, депрессия, адинамия, интоксикационные психозы). Кожные покровы и видимые слизистые больных сухие. АД снижено. Пульс учащен, суточный диурез уменьшен. В крови определяются повышение гематокритного числа, гипо- и диспротеинемия, снижение общего количества электролитов, увеличение мочевины, остаточного азота, непрямого билирубина.
Сформированные толстокишечные свищи не сопровождаются столь выраженной симптоматикой. Основными их признаками являются выделение кала и воспалительные изменения окружающей кожи. Клинические проявления наружных свищей кишечника становятся более выраженными в случае присоединения различных осложнений: эвентрация приводящей петли через свищ с ее ущемлением; кровотечения из свища; отторжения кишки со свищом от брюшной стенки с развитием перитонита или гнойно-каловых затеков.
Внутренние кишечные свищи, как правило, ничем не проявляются. Однако при, высоких тонко-толстокишечных соустьях могут отмечаться прогрессирующее похудание, диарея.
По строению различают трубчатые и губовидные свищи (Рис. 23).
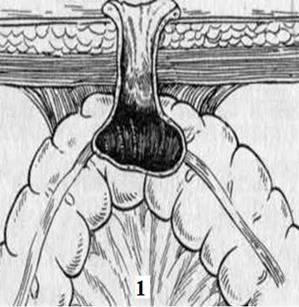
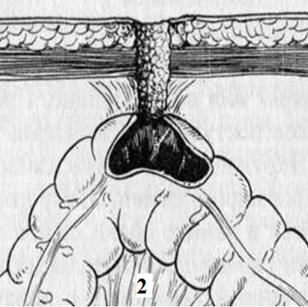
Рисунок 23. Виды кишечных свищей: 1- губовидный свищ; 2 - трубчатый свищ[23].
Трубчатый свищ представляет собой изолированный канал, выстланный грануляционно-рубцовой тканью или покровным эпителием, соединяющий просвет кишки с кожей. Его размеры и форма вариабельны. Свищевой ход может быть коротким или длинным, извилистым или прямолинейным, иметь множество внутренних и наружных отверстий. В ряде случаев на его пути находится гнойная полость. Наружный диаметр трубчатого кишечного свища значительно меньше, чем губовидного. Основным признаком губовидного свища является непосредственное срастание слизистой оболочки кишки по краю дефекта ее стенки с кожей.
Диагностика кишечных свищей включает визуальное исследование раны со свищом, использование красителей, проведение лабораторных, рентгеновских и эндоскопических методов исследования. Осмотр наружного отверстия свища и его отделяемого, пальцевое исследование свищевого хода дают первое представление о локализации и морфологических характеристиках свища.
Расположение свища, его функция могут быть оценены на основании
проб с красителями. Наиболее часто больному дают выпить метиленовый синий или ставят с ним клизму. По времени появления красящего вещества и судят об уровне нахождения кишечного свища. По тонкой кишке химус движется со скоростью 2-3 см/мин, в толстой кишке 1-2 см/мин. В какой-то степени этому помогает определение содержания в отделяемом свища билирубина, ферментов поджелудочной железы, мочевины.
Вид и размеры свища, состояние слизистой оболочки отводящих сегментов кишечника устанавливаются с помощью УЗИ, эндоскопической техники - фиброколоноскопии, фиброгастроскопии и т.д., а также рентгенологического исследования. Оно включает обзорное полипозиционное исследование брюшной полости, контрастные методы: фистулографию (введение в свищевое отверстие рентгенконтрастного препарата), пассаж бария по тонкому кишечнику, ирригоскопию, компьютерную томографию и т.д. Часто указанные методы диагностики кишечных свищей следует сочетать.
Лечение больных с кишечными свищами – чрезвычайно трудное дело. Как правило, больным с диагностированными кишечными свищами назначается консервативное лечение, которое позволяет добиться заживления 85-95% трубчатых свищей и 40-50% несформированных губовидных свищей. Одновременно это является подготовкой к операции у больных со сформированными губовидными свищами.
Комплексная консервативная терапия включает: назначение калорийного питания, регуляцию секреторной и моторной функций органов желудочно-кишечного тракта, устранение имеющихся в организме расстройств гомеостаза (нарушений белкового, углеводного, жирового обменов, водно-электролитного баланса и т.д.), симптоматическую терапию, местное лечение. Последнее предполагает купирование гнойно-воспалительного процесса в тканях, окружающих свищ; предохранение их от воздействия кишечного отделяемого; уменьшение или прекращение потерь кишечного содержимого.
Для защиты кожи от действия кишечного отделяемого используются физические, биохимические и механические способы. Физические способы основаны на применении пасты Лассара, клея БФ-2, БФ-6, силиконовой пасты, полимеризующейся пленки, которая наносится на кожу, окружающую наружное отверстие свища. В основе биохимических способов защиты лежит нейтрализация пищеварительных соков: 1) тампонами, смоченными яичным белком, которые помещаются непосредственно на свищ; 2) постоянным орошением раны раствором молочной кислоты (1 л изотонического раствора натрия хлорида + 4,7 л раствора молочной кислоты) и т.д.
Механические способы направлены на уменьшение или прекращение выделения из свища путем закупорки его наружного отверстия различными обтураторами, пелотами, обтурирующими заслонками и повязками.
Хирургическое вмешательство проводится для закрытия незаживающих на фоне консервативного лечения трубчатых и практически всех губовидных свищей. Плановые операции выполняются не ранее 2-3 месяцев после их формирования.
Наиболее широко распространены различные модификации резекции участка кишки несущей свищ - пристеночная, циркулярная.
В случаях сложных кишечных свищей более целесообразно использование операции выключения (полного и неполного) свищей. Суть операции неполного выключения состоит в наложении анастомоза между приводящим к свищу и отводящим от свища участком кишки. При полном выключении приводящая и отводящая петли кишечника прошиваются между анастомозом и свищом, а затем выключенная часть кишки вместе со свищом удаляются. Наиболее часто этот вид операции применяется при множественных свищах и в случае высоких свищей у больных с быстро ухудшающимся состоянием.
В качестве вариантов операции при небольших неполных трубчатых и губовидных свищах применяются внебрюшинные методы их закрытия, а при остальных - внутрибрюшинные. Сущность внебрюшинных методов лечения заключается в выделении стенки свища в зоне свищевого хода с ушиванием дефекта. Летальность при кишечных свищах аппендикулярного генеза достигает 6-8%.








