Рецепторно-канальные комплексы
По конструкции различают два типа рецепторно-канальных комплексов. В одних случаях (тип I) рецепторы жестко сцеплены со своими эффекторами и сопряжение между ними осуществляется контактным способом. В других случаях (тип II) рецепторы отделены от своих эффекторов и сочленяются с ними с помощью оформленных сопрягающих элементов. Рецепторно-канальные комплексы обеспечивают проведение ионов из внеклеточной среды во внутриклеточную. Непосредственными исполнителями проведения ионов являются так называемые транспортные трансмембранные (интегральные) белки, конформационные структуры которых формируют внутренний канал, способный открываться или закрываться в результате конформационных изменений, индуцированных активированным рецептором.
Рецепторно-канальные комплексы типа I
Как показано на рисунке 16, в комплексе типа I рецепторное звено встроено в эффекторное звено – стенку белкового канала. Вместе они образуют рецептор-канал, в котором функцию сопрягающего звена выполняет непосредственный контакт, что обеспечивает быстроту физиологического ответа на действие лиганда.
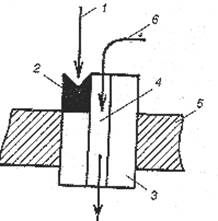
| Рис.16. Схема организации рецепторно-канального комплекса типа I. 1 – лиганд; 2 – рецепторное звено (участок) в канальном белке; 3 – эффектор (стенка канала); 4 – ионный канал; 5 – плазмолемма; 6 – ион. |
Известны четыре вида рецептор-каналов: никотиновый холинорецептор (Н-холинорецептор), гамма-аминомасляный, глутаматный и глициновый. В качестве примера рассмотрим два из них: Н-холиновый и глутаматный.
· Н-холинорецепторы
К одному и тому же нейромедиатору ацетилхолину существует два типа рецепторов, один из которых возбуждается никотином (Н-холинорецепторы), другой – мускарином (М-холинорецепторы).
Н-холинорецептор является составной частью быстродействующего рецептор-канала (Рис.17). М-холинорецепторы управляют своими эффектор-каналами посредством специализированных белков, что значительно снижает быстродействие.
Н-холинорецептор имеет грибовидную форму. Он пронизывает клеточную мембрану насквозь, выступая концами за наружную и внутреннюю ее стороны. Сверху молекула Н-холинорецептора имеет вид неправильной по форме розетки из пяти субъединиц, расположенных вокруг центрального электронно-плотного образования, ограничивающего ионный канал.
В Н-холиновом рецептор-канале выделяют два функционально различных компонента – узнающий центр и ионный канал. Узнающий центр – участки альфа-субъединиц, выступающие над поверхностью клеточной мембраны и обладающие способностью к опознанию и связыванию молекул ацетилхолина. Эти участки и составляют собственно Н-холинорецептор.
Молекулярный по своей организации рецептор встроен в стенку исполнительной части - канального белка, так что в целом все образование представляет собою рецепторно-эффекторный комплекс, предназначенный для генерирования потенциала действия в плазмолемме. Н-холинорецепторный комплекс является первым звеном Н-холинореактивной системы более высокого уровня, осуществляющей функцию сокращения поперечнополосатой мышцы.
| Рис.17. Схематическое изображение Н-холинового рецептор-канала (трехмерное изображение). I – грибовидный рецептор-канал; II – плазматическая мембрана. | 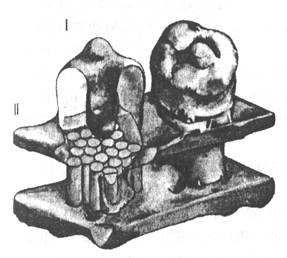
|
В фармакологии и нейротоксикологии известно большое число химиопрепаратов, которые специфически взаимодействуют с рецепторными участками, ионными каналами, а также с отдельными звеньями на пути дальнейшего прохождения сигналов к эффекторам, обеспечивающим конечные биохимические и физиологические ответы клетки. Такие вещества используются для изучения холинореактивных и других систем, а также в лечебных целях.
· Глутаматные рецепторы
Ряд аминокислот (глутаминовая, аспарагиновая, гамма-аминомасляная, тауриновая и др.), кроме энергетических, выполняют еще и медиаторные функции, оказывая на клетки-мишени возбуждающие и тормозные действия. Глутамат (анион глутаминовой кислоты) является одним из основных возбуждающих нейропередатчиков в нервной системе.
Наибольшее количество глутаматных рецепторов находится в коре больших полушарий, гиппокампе, полосатом теле, среднем мозге и в гипоталамусе.
Глутаматный рецептор-канал состоит из четырех белковых субъединиц, образующих эллипсоидной формы комплекс с центрально расположенным воронкообразным каналом для селективного пропуска ионов натрия, калия, хлора, кальция (Рис.18).
Вполне вероятно, что природа ионов, проходящих через канал, определяется типом нейронов и их функциональной специализацией. Рецепторный участок встроен в одну из субъединиц.
В отличие от Н-хлоинорецепторов, стабильно закрепленных в клеточной мембране, белковые субъединицы глутаматных рецептор-каналов в отсутствие лигандов находятся в диссоциированном состоянии и свободно плавают внутри мембраны или на ее поверхности.
При поступлении глутамата субъединицы, по-видимому, ассоциируются, образуя рецептор-канал, причем непосредственно над предсуществующим трансмембранным ионным каналом, выступая над ним в виде пристройки и стимулируя его раскрытие. Следует подчеркнуть, что строгих доказательств в пользу вышеупомянутых событий в литературе еще нет. Появляются сведения о том, что имеются разные типы глутаматных рецепторов: быстродействующие (тип I) и медленнодействующие (тип II).
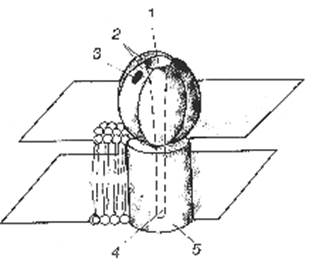
| Рис.18. Глутаматные рецепторы. 1 – воронкообразный канал рецептор-канале; 2 – белковые субъединицы; 3 – участокопознанияи связывания глутамата на одной из субъединиц; 4 –канал внутри трансмембранного белка (5). |
Описанный выше рецептор-канал является быстродействующим. Медленнодействующие глутаматные рецепторы участвуют в реализации химического сигнала через систему внутриклеточных посредников: циклических нуклеотидов и ионов кальция, однако соотношение их с быстродействующими и преимущественные места расположения еще не ясны.
Механизм действия глутамата в системе головного мозга заключается в индукции состояния возбуждения нейронов и их ансамблей. Связывание глутамата с рецептор-каналом вызывает в постсинаптической мембране волну возбуждения, которая распространяется по всему нейрону и по синапсам перекидывается на соседние нейроны.
Глутаматные рецепторы широко представлены в структурах головного мозга, ответственных за проявление высших психических и двигательных функций. Ряд нервно-психических заболеваний, таких, как хорея Гентингтона, шизофрения, эпилепсия, связаны с количественными и качественными изменениями глутаматергических систем.
Рецепторно-канальные комплексы типа II
В РКК типа II рецепторы отделены от своих эффекторов и сочленяются с ними с помощью оформленных сопрягающих элементов (Рис.19). Сингнал проходит медленно.
Рассмотрим:
- Мускариновые рецепторы;
- Альфа1-адренорецепторы
| Рис.19. Схема организации рецепторно-канальных комплексов типа II: 1 – лиганд; 2 – рецепторное звено; 3 – эффектор (стенка канала); 4 – ионный канал; 5 – плазмолемма; 6 – ион; 7 – сопрягающее звено. Стрелками показано движение сигнала. | 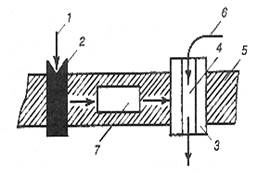
|
· Мускариновые рецепторы.
(М-холинорецепторы) обнаруживаются в гладкой мышечной ткани, сердечной мышечной ткани, секреторных клетках вегетативных ганглиях, в клетках каротидного синуса, горизонтальных клетках сетчатки, в нервных образования ЦНС – базальном ядре, хвостатом ядре, черной субстанции, пирамидный нейронах, гиппокампе, обонятельной луковице. Возбуждение М-холинорецепторов вызывает такие эффекты, как сужение зрачка, сокращение гладких мышц, иннервируемых парасимпатическими волокнами, стимуляцию секреции слюнных и желудочных желез, комплексное изменение функций сердечно-сосудистой системы и др. собственно М-холинорецептор представляет собою трансмембранное образование.
Схема работы комплекса «М-холинорецептор – G-белок – ионный канал» показана на рисунке, в данном случае ацетилхолин, взаимодействуя с рецептором, переводит его из неактивного состояния в активное. Это состояние передается сопрягающему G-белку и далее к эффектору, то есть кальциевому каналу. Канал открывается, ионы кальция устремляются в клетку и, как вторичный мессенджер, запускают в действие зависимые от него внутриклеточные процессы: сокращение мышечных волокон, активирование гуанилатциклазы к синтезу цГМФ, фосфорилирование некоторых белков, включая и сам М-холинорецептор, высвобождение секретов из железистых клеток и др.
Исследования, проводимые по изучению М-холинорецепторов при ряде заболеваний, указывают на связь некоторых нарушений жизненных отправлений человека с качественными и количественными отклонениями рецепторных характеристик. Так, при болезни Гентингтона количество М-холинорецепторов в полосатом теле головного мозга в два раза ниже нормы; при болезни Альцгеймера в гиппокампе число их понижено на 40%.
· Альфа1-адренорецепторы.
Существуют два типа адренергических рецепторов – альфа- и бета-рецепторы. Альфа-рецепторы опосредуют, в основном, возбуждение функции (сужение сосудов, сокращение гладких мышц матки, мочевого пузыря, сфинктера зрачка) и в ряде случаев ингибирование функции (расслабление мускулатуры кишечника).
Рецепторы альфа-типа в свою очередь подразделяет на два подкласса – альфа1- и альфа2-адренорецепторы. Альфа1-адренорецепторы, связанные в своей функции с работой ионных каналов, будут рассмотрены в этом разделе. Альфа2- и бета-адренорецепторы в качестве исполнительного звена имеют ферментные молекулы и будут рассмотрены в следующем разделе.
Альфа1-адренорецепторы располагаются повсеместно в организме на постсинаптических мембранах. Рецепторы этого типа обнаружены в гладких миоцитах сосудов и других органов, в кардиомиоцитах, в гепатоцитах, экзокриноцитах, клетках ЦНС, эпителиоцитах кишки и др. Принципиальная схема структуры альфа1-адренорецепторных комплексов в клетках разных тканей имеет некоторые различия.
Почти во всех тканях стимуляция альфа1-адренорецепторов сопровождается повышением внутриклеточной концентрации Ca2+. В этом случае рецепторное звено сопряжено с кальциевым каналом.
В ЦНС стимуляция тех же рецепторов сопровождается изменением внутриклеточного уровня вторичного мессенджера цАМФ, выработка которого связана с деятельностью фермента аденилатциклазы как эффектора. Таким образом, в отношении подгруппы альфа1-адренорецепторов можно полагать, что в большинстве тканей они представлены рецепторно-канальными комплексами, в ЦНС – рецепторно-ферментными.
Рецепторно-ферментные комплексы
Структурно они состоят из собственно рецепторных молекул, сопрягающих белков и ферментных молекул в качестве эффекторов (рис.20). Рецепторы представляют собой интегральные белки. Сопряжение рецептора с эффектором осуществляется с помощью G-белков.
Различают стимулирующие и ингибирующие сопрягающие белки (соответственно Gs- и Gi-белки).
В качестве эффекторных молекул служат ферменты аденилатциклаза и гуанилатциклаза, являющиеся интегральными белками. Они катализируют реакции образования цАМФ и цГМФ из АТФ и ГТФ. Тот и другой являются вторичными мессенджерами. С аденилатциклазой работают моноаминергические рецепторы (адрен-, норадрен- и дофаминергические), опиатные, инсулиновые часть М-холинергических, серотониновые, энкефалиновые, Г2-гистаминовые и др. С гуанилатциклазой связана большая часть М-холинорецепторов, альфа-норадреналиновые, Г2-гистаминовые и другие рецепторы.
В качестве конкретных примеров возьмем два вида адренорецепторов, в одном из которых сопрягающий белок выполняет ингибирующую роль, в другом – стимулирующую.
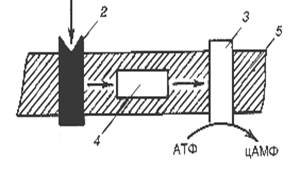
| Рис.20. Схема организации рецепторно-ферментных комплексов: 1 – лиганд; 2 – рецепторное звено; 3 – эффекторное звено (ферменты аденилатциклаза, фосфолипаза и др.); 4 – сопрягающее звено; 5 – плазмолемма. |
· Альфа2-адренорецепторы.
Характерной особенностью альфа2-адренорецеторов является их способность в активированном состоянии ингибировать синтез цАМФ, т.е. рецепторная молекула взаимодействует со своим эффектором аденилатциклазой через ингибиторный G1-белок. В общем виде представляется следующим образом.
Потенциал действия распространяется по нейрону, достигает нервного окончания и открывает кальциевые каналы в пресинаптической мембране. Ионы кальция стимулируют выброс нейромедиатора в синаптическую щель. Из синаптической щели молекулы лиганда устремляются к альфа2-адренорецепторам в пре- и постсинаптических мембранах. В постсинаптической мембране лиганд соединяется с рецептором и вызывает конформационное изменение, влекущее его к соединению с Gi-белком. Последний активируется и соединяется с аденилатциклазой. В комплексе «лиганд-рецептор-Gi-белок-аденилатциклаза» синтез вторичного мессенджера цАМФ снижается. Снижение концентрации цАМФ опосредует физиологический эффект в клетках щитовидной железы, в корковом веществе почек, околоушной железе, в клетках островков поджелудочной железы и др. Лиганд из синаптической щели поступает и на альфа2-андренорецепторы пресинаптической мембраны. Активация рецептора через вторичный посредник цАМФ приводит к ингибированию в нервном окончании секреции нейромедиаторов.
· Бета-адренорецепторы .
В основном опосредуют угнетение функции (расширение сосудов, релаксация гладких мышц матки и бронхов) и в ряде случаев ее возбуждение (стимуляция миокарда). Они локализуются преимущественно в постсинаптических мембранах, но обнаруживаются в пресинаптических участках нервных окончаний. Бета-адренорецепторы подразделяются на два подтипа. Рецептора бета1-подтипа примерно одинаково чувствительны к адреналину и норадреналину. Они, главным образом, присутствуют в сердце, жировой ткани, сосудах и в головном мозге. Бета1-адренорецепторы входят в состав синапсов и реагируют в основном на нормадреналин. Бета2-адренорецепторы имеют большее сродство к адреналину, чем к норадреналину. Они обнаружены в легких, печени, исчерченных и неисчерченных мышцах различных органов. Бета2-адренорецепторы располагаются внесинаптически и реагируют, в первую очередь, на катехоламины микроциркуляторного русла.
По морфобиохимической организации бета-андренорецепторы относятся к аденилатциклазной группе, т.к. имеют аденилатциклазу в качестве эффектора. Детали строения и механизм опосредования физиологического ответа изложены выше при описании общей характеристики групп. Механизмы работы бета-адренорецепторов в отличие от альфа2-адренорецепторов сводятся к активации аденилатциклазы в ответ на действие адреналина или норадреналина и к синтезу цАМФ.
Те или иные нарушения любого из звеньев клеточного адренорецепторного комплекса, будь то альфа- или бета-комплексы, могут явиться причиной заболеваний. Аутоантитела к альфа2-адренорецепторам вызывают у пациентов аллергический ринит и астму. Для некоторых заболеваний выяснены места нарушений в адренорецепторах. Мишенью действия ряда бактериальных экзотоксинов являются стимуляторные G2-белки сопряжения. Токсин холеры, специфически соединяясь с такими белками, поддерживает постоянную активность аденилатциклазы и выработку избыточной цАМФ. Токсин коклюша не влияет на стимуляторные сопряжения, но тормозит действие ингибиторных белков. Известны и другие заболевания, связанные с врожденной или приобретенной недостаточностью тех или иных классов адренорецепторов.








