Второй закон термодинамики. Свободная энергия.
1. Задание {{ 1 }} ТЗ № 1
При протекании реакции PBr5(т) = PBr3(ж)+ Br2(г) энтропия
- не изменяется
- изменяется незначительно
- уменьшается
+ увеличивается
2. Задание {{ 2 }} ТЗ № 2
Отметьте правильный ответ
В реакции C 2 H 4 (г)+ H 2 (г)= C 2 H 6 (г) энтропия
- не изменяется
+ уменьшается
- увеличивается
3. Задание {{ 3 }} ТЗ № 3
В реакции B2O3+2Al=Al2O3+2B энтропия
- уменьшается затем увеличивается
+ изменяется незначительно
- уменьшается
- увеличивается
4. Задание {{ 4 }} ТЗ № 4
Отметьте правильный ответ
Мерой неупорядоченности системы в термодинамике принято считать
- энтальпию
+ энтропию
- свободную энергию
- теплоту
5. Задание {{ 5 }} ТЗ № 5
 Отметьте правильный ответ
Отметьте правильный ответ
Направление протекания реакции N 2 O 4 2 NO при D H =+24 кДж и D G = –46кДж определяет
+ изменение энтропии
- изменение энтальпии
- изменение свободной энергии
6. Задание {{ 6 }} ТЗ № 6
Отметьте правильный ответ
Реакция может протекать самопроизвольно при
- DH<0 и DS<0
- DH>0 и DS<0
+ DH<0 и DS>0
- DH>0 и DS>0
7. Задание {{ 9 }} ТЗ № 9
Отметьте правильный ответ
Функциями состояния системы являются
- теплота
- работа
+ энтропия
+ энтальпия
8. Задание {{ 19 }} ТЗ № 19
Отметьте правильный ответ
При переходе от графита к алмазу энтропия
- не изменяется
+ уменьшается
- увеличивается
9. Задание {{ 20 }} ТЗ № 20
Отметьте правильный ответ
При растворении твердых веществ энтропия
- не изменяется
- уменьшается
+ увеличивается
10. Задание {{ 21 }} ТЗ № 21
Отметьте правильный ответ
При переходе от кислорода к озону энтропия
- не изменяется
- уменьшается
+ увеличивается
11. Задание {{ 22 }} ТЗ № 22
Отметьте правильный ответ
В ряду LiCl (т), NaCl (т), KCl (т), RbCl (т), CsCl (т) энтропия
- не изменяется
- уменьшается
+ увеличивается
12. Задание {{ 23 }} ТЗ № 23
Отметьте правильный ответ
При растворении перекиси водорода в воде энтропия
- не изменяется
+ уменьшается
- увеличивается
13. Задание {{ 24 }} ТЗ № 24
Отметьте правильный ответ
При растворении хлороводорода в воде энтропия
- не изменяется
+ уменьшается
- увеличивается
14. Задание {{ 25 }} ТЗ № 25
Отметьте правильный ответ
Для идеального газа изменения энергии Гиббса при изменении давления от P 1 до P 2 в условиях T = const равно
- ΔG= -RT ln 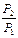
+ ΔG=RT ln 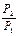
- ΔG=RT ln 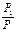
- ΔG=RT ln(P2-P1)
15. Задание {{ 128 }} ТЗ № 128
Отметьте правильный ответ
Энтропия изолированной системы стремится к
- минимуму
+ максимуму
- нулю
- единице
16. Задание {{ 129 }} ТЗ № 129
Отметьте правильный ответ
В условиях постоянной температуры и давления самопроизвольно могут протекать только такие процессы, для которых изменение энергии Гиббса
+ меньше нуля
- больше нуля
- равна нулю
17. Задание {{ 130 }} ТЗ № 130
Отметьте правильный ответ
Живой организм представляет собой систему
- закрытую
- изолированную
+ открытую
- адиабатическую
18. Задание {{ 131 }} ТЗ № 131
Отметьте правильный ответ
Для необратимых процессов второй закон термодинамики имеет вид
- 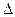 S =
S = 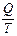
+ 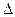 S >
S > 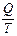
- 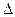 S <
S < 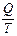
- S = klnW
- S = 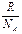 lnW
lnW
19. Задание {{ 132 }} ТЗ № 132
Отметьте правильный ответ
Для обратимых процессов второй закон термодинамики имеет вид
+ 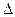 S =
S = 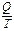
- 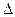 S >
S > 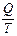
- 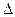 S <
S < 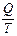
- S = klnW
- S = 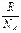 lnW
lnW
20. Задание {{ 446 }} ТЗ № 446
Отметьте правильный ответ
Реакция возможна при любых температурах при
+  Н<0,
Н<0,  S>0
S>0
-  Н<0,
Н<0,  S<0
S<0
-  Н>0,
Н>0,  S>0
S>0
-  Н>0,
Н>0,  S<0
S<0
21. Задание {{ 447 }} ТЗ № 447
Отметьте правильный ответ
При любых температурах реакция невозможна при
-  Н<0,
Н<0,  S>0
S>0
-  Н<0,
Н<0,  S<0
S<0
-  Н>0,
Н>0,  S>0
S>0
+  Н>0,
Н>0,  S<0
S<0
22. Задание {{ 448 }} ТЗ № 448
Отметьте правильный ответ
Если  Н<0 и
Н<0 и  S<0, то реакция может протекать самопроизвольно при
S<0, то реакция может протекать самопроизвольно при
+ |  Н| > |T
Н| > |T  S|
S|
- |  Н| < |T
Н| < |T  S|
S|
- |  Н| = |T
Н| = |T  S|
S|
23. Задание {{ 449 }} ТЗ № 449
Отметьте правильный ответ

 При определенной температуре Т эндотермическая А В реакция практически идет до конца. При этом возможность протекания В А при низких температурах определяется значением
При определенной температуре Т эндотермическая А В реакция практически идет до конца. При этом возможность протекания В А при низких температурах определяется значением
-  G <0
G <0
-  G > 0
G > 0
-  S >0
S >0
-  Н >0
Н >0
+  S <0
S <0
24. Задание {{ 450 }} ТЗ № 450
Отметьте правильный ответ
 При определенной температуре Т эндотермическая реакция А В практически идет до конца. При этом
При определенной температуре Т эндотермическая реакция А В практически идет до конца. При этом
+  Н > 0
Н > 0
-  Н<0
Н<0
-  G >0
G >0
+  G < 0
G < 0
+  S >0
S >0
-  S<0
S<0
25. Задание {{ 454 }} ТЗ № 454
Отметьте правильный ответ
Всякий самопроизвольный процесс в изолированной системе идет с
- уменьшением энтропии
+ возрастанием энтропии
- без изменения энтропии
26. Задание {{ 455 }} ТЗ № 455
Отметьте правильный ответ
В обратимом процессе
-  S >0
S >0
-  S <0
S <0
-  S=1
S=1
+  S=0
S=0
27. Задание {{ 456 }} ТЗ № 456
Отметьте правильный ответ
Процесс термодинамически возможен при
-  S=0
S=0
+  S>0
S>0
-  S<0
S<0
28. Задание {{ 457 }} ТЗ № 457
Отметьте правильный ответ
Процесс термодинамически невозможен при
-  S=0
S=0
-  S>0
S>0
+  S<0
S<0
29. Задание {{ 458 }} ТЗ № 458
Отметьте правильный ответ
Мерой вероятности состояния системы в термодинамике принято считать
- энтальпию
+ энтропию
- свободную энергию
- внутреннюю энергию
30. Задание {{ 459 }} ТЗ № 459
Отметьте правильный отве
Возможность самопроизвольного протекания реакции определяется знаком изменения функций при любых температурах
-  Н > 0
Н > 0
+  Н<0
Н<0
-  S<0
S<0
+  S>0
S>0
-  G >0
G >0
+  G <0
G <0
31. Задание {{ 460 }} ТЗ № 460
Отметьте правильный ответ
Невозможность самопроизвольного протекания реакции определяется знаком изменения функции при любых температурах
+  Н > 0
Н > 0
-  Н<0
Н<0
+  S<0
S<0
-  S >0
S >0
+  G > 0
G > 0
-  G <0
G <0
32. Задание {{ 461 }} ТЗ № 461
Отметьте правильный ответ
Возможность самопроизвольного протекания реакции определяется знаком изменения функций при достаточно низких температурах
-  Н >0
Н >0
+  Н<0
Н<0
+  S<0
S<0
-  S>0
S>0
33. Задание {{ 462 }} ТЗ № 462
Отметьте правильный ответ
Возможность самопроизвольного протекания реакции определяется знаком изменения функций при достаточно высоких температурах
+  Н >0
Н >0
-  Н<0
Н<0
-  S<0
S<0
+  S >0
S >0
34. Задание {{ 463 }} ТЗ № 463
Отметьте правильный ответ
Для реакций, протекающих в стандартных условиях, из нижеприведенных утверждений правильны
+ эндотермические реакции не могут протекать самопроизвольно
- эндотермические реакции могут протекать при достаточно низких температурах
+ эндотермические реакции могут протекать при достаточно высоких температурах, если изменение энтропии реакции положительно
Принцип Ле-Шателье.
 1. Задание {{ 340 }} ТЗ № 340
1. Задание {{ 340 }} ТЗ № 340
При понижении температуры равновесие реакции 2SO2 + O2 2 SO3 + 192 кДж сместится
+ вправо
- влево
- не сместится
2. Задание {{ 341 }} ТЗ № 341
 При добавлении катализатора равновесие реакции N2 + 3H2 2NH3 + 90 кДж
При добавлении катализатора равновесие реакции N2 + 3H2 2NH3 + 90 кДж
- вправо
- влево
+ не сместится
3. Задание {{ 342 }} ТЗ № 342
Изменение давления смещает равновесие реакции
 - H2(г) + Cl2(г) 2HCl(г)
- H2(г) + Cl2(г) 2HCl(г)
 + H2(г) + I2(к) 2HI (г)
+ H2(г) + I2(к) 2HI (г)
 - C(к) + O2(г) CO2(г)
- C(к) + O2(г) CO2(г)
 - H2(г) + S(к) H2S(г)
- H2(г) + S(к) H2S(г)
4. Задание {{ 343 }} ТЗ № 343
 Равновесие в реакции Fe2+ + HOH FeOH+ + H+ - Q смещается вправо при
Равновесие в реакции Fe2+ + HOH FeOH+ + H+ - Q смещается вправо при
+ повышение температуры
- понижение температуры
+ уменьшение концентрации ионов H+
- увеличение концентрации ионов H+
5. Задание {{ 344 }} ТЗ № 344
 Равновесие реакции H2S(ж) H+(ж) + HS-(ж) – Q смещается влево при
Равновесие реакции H2S(ж) H+(ж) + HS-(ж) – Q смещается влево при
- повышение температуры
+ понижение температуры
- уменьшение концентрации ионов H+
+ увеличение концентрации ионов H+
6. Задание {{ 345 }} ТЗ № 345
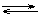 Равновесие реакции 2CO + O2 2CO2 + Q смещает вправо при
Равновесие реакции 2CO + O2 2CO2 + Q смещает вправо при
- увеличении температуры
+ уменьшении температуры
+ увеличении давления
- уменьшении давления
+ уменьшении объема
- увеличении концентрации CO2
7. Задание {{ 346 }} ТЗ № 346
 При повышении давления в системе N2+O2 2NO равновесие сместится
При повышении давления в системе N2+O2 2NO равновесие сместится
- вправо
- влево
+ не сместится
8. Задание {{ 347 }} ТЗ № 347
 Чтобы равновесие в системе 2CO + O2 2CO2 сместить вправо следует давление
Чтобы равновесие в системе 2CO + O2 2CO2 сместить вправо следует давление
+ повысить
- понизить
- не изменять
9. Задание {{ 348 }} ТЗ № 348
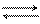 Чтобы сместить равновесие 2СO CO2 + C вправо концентрацию CO2 следует
Чтобы сместить равновесие 2СO CO2 + C вправо концентрацию CO2 следует
+ понизить
- повысить
- не изменять
10. Задание {{ 349 }} ТЗ № 349
 При понижении температуры равновесие системы 2CO + O2 2CO2 + 568,5 кДж смещается
При понижении температуры равновесие системы 2CO + O2 2CO2 + 568,5 кДж смещается
+ вправо
- влево
- не смещается
11. Задание {{ 350 }} ТЗ № 350
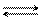 При увеличении концентрации CO2 в системе 2CO + O2 2CO2 + 568,5 кДж равновесие смещается
При увеличении концентрации CO2 в системе 2CO + O2 2CO2 + 568,5 кДж равновесие смещается
- вправо
+ влево
- не смещается
12. Задание {{ 351 }} ТЗ № 351
 Если увеличить концентрацию водорода в системе 2HBr H2 + Br2-70 кДж равновесие сместится
Если увеличить концентрацию водорода в системе 2HBr H2 + Br2-70 кДж равновесие сместится
- вправо
+ влево
- не сместится
13. Задание {{ 352 }} ТЗ № 352
 Равновесие системы 2HCl H2 + Cl2 –Q при повышении давления сместится
Равновесие системы 2HCl H2 + Cl2 –Q при повышении давления сместится
- вправо
- влево
+ не сместится
14. Задание {{ 353 }} ТЗ № 353
 Равновесие NH3 + H2O NH4+ + OH- при добавлении к раствору щелочи сместится
Равновесие NH3 + H2O NH4+ + OH- при добавлении к раствору щелочи сместится
- вправо
+ влево
- не сместится
15. Задание {{ 354 }} ТЗ № 354
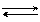 Чтобы сместить равновесие реакции CO2(г) + С(тв) 2CO-173 кДж вправо необходимо
Чтобы сместить равновесие реакции CO2(г) + С(тв) 2CO-173 кДж вправо необходимо
+ повысить температуру
- понизить температуру
- повысить давление
- уменьшить концентрацию CO2
+ увеличить концентрацию CO2
- увеличить концентрацию CO
16. Задание {{ 523 }} ТЗ № 523
 При сжатии равновесной системы H2(г)+I2(г) 2HI(г) равновесие сместится
При сжатии равновесной системы H2(г)+I2(г) 2HI(г) равновесие сместится
- вправо
- влево
+ не сместится
17. Задание {{ 524 }} ТЗ № 524
 При повышении давления равновесие системы 2СО+О2 2СО2 сместится
При повышении давления равновесие системы 2СО+О2 2СО2 сместится
+ вправо
- влево
- не сместится
18. Задание {{ 525 }} ТЗ № 525
 При повышении температуры равновесие обратимой реакции СО+Н2О СО2+Н2+10 ккал сместится
При повышении температуры равновесие обратимой реакции СО+Н2О СО2+Н2+10 ккал сместится
- вправо
+ влево
- не сместится
 19. Задание {{ 526 }} ТЗ № 526
19. Задание {{ 526 }} ТЗ № 526
При повышении температуры равновесие обратимой реакции N2+O2 2NO-43 ккал сместится
+ вправо
- влево
- не сместится
 20. Задание {{ 527 }} ТЗ № 527
20. Задание {{ 527 }} ТЗ № 527
При понижении температуры равновесие системы PCl5 PCl3 + Cl2 -31 ккал сместится
- вправо
+ влево
- не сместится
21. Задание {{ 528 }} ТЗ № 528
 При понижении температуры равновесие системы N2+3H2 2NH3 +22 ккал сместится
При понижении температуры равновесие системы N2+3H2 2NH3 +22 ккал сместится
+ вправо
- влево
- не сместится
 22. Задание {{ 529 }} ТЗ № 529
22. Задание {{ 529 }} ТЗ № 529
Чтобы повысить выход SO3 по реакции 2SO2+O2 2SO3 + 45 ккал надо
- повысить температуру
+ понизить температуру
+ увеличить концентрацию SO2
+ понизить концентрацию SO3
+ повысить давление
- понизить давление
 23. Задание {{ 530 }} ТЗ № 530
23. Задание {{ 530 }} ТЗ № 530
Чтобы сместить равновесие реакции СО2(г) + С(тв) 2СО(г)-173 кДж вправо надо
+ повысить температуру
- повысить давление
- понизить температуру
+ понизить давление
- уменьшить концентрацию СО2
+ уменьшить концентрацию СО
24. Задание {{ 531 }} ТЗ № 531
При повышении температуры равновесие экзотермической реакции смещается
- вправо
+ влево
- не смещается
25. Задание {{ 532 }} ТЗ № 532
При повышении температуры равновесие эндотермической реакции смещается
+ вправо
- влево
- не смещается
26. Задание {{ 533 }} ТЗ № 533
При понижении температуры равновесие экзотермической реакции смещается
+ вправо
- влево
- не изменяется
27. Задание {{ 534 }} ТЗ № 534
При понижении температуры равновесие эндотермической реакции смещается
- вправо
+ влево
- не смещается
28. Задание {{ 535 }} ТЗ № 535
 При повышении давления в системе 2HCl H2+ Cl2 – Q равновесие сместится
При повышении давления в системе 2HCl H2+ Cl2 – Q равновесие сместится
- вправо
- влево
+ не сместится
29. Задание {{ 536 }} ТЗ № 536
Отметьте правильный ответ.
 При увеличении концентрации водорода равновесие системы 2HBr H2+ Br2 – 70кДж сместится
При увеличении концентрации водорода равновесие системы 2HBr H2+ Br2 – 70кДж сместится
- вправо
+ влево
- не сместится








