Тема. Водородная связь
Сущность химической связи
1. Устойчивым является такое состояние атома, при котором его внешний энергетический уровень завершён до 8 электронов (Н, Не – до 2 электронов).
2. Завершённый внешний уровень имеют атомы VIII A группы.
3. Oдиночные атомы связанные атомы
○ + ○ → ○○ + Е
Главная причина образования химической связи – выделение энергии и повышение устойчивости системы.
4. Чем меньше запас энергии атома, тем более он устойчив в химическом отношении и его состояние наиболее энергетически выгодное.
5. Пути завершения внешнего уровня атомов:
- образование общих электронных пар
- отдача или присоединение электронов
- обобществление электронов.
Объясним механизм образования водородной связи с учётом электронного и пространственного строения молекул воды (
Ни одна из планет Солнечной системы не содержит на своей поверхности такого большого количества воды, как наша Земля. Моря и океаны, средняя глубина которых около 6 км, покрывают 71 % поверхности Земли. Огромное количество воды в виде снега и льда сосредоточено в приполярных районах.
Этот удивительный факт пока не нашел однозначного объяснения. Безусловно, вода играет огромную роль в возникновении и существовании жизни на нашей планете. Во многом это связано со свойствами, которых нет у ее ближайших соседей и аналогов. Прежде всего нужно разобраться, почему вода может находиться в жидком и даже в твердом состоянии (лед) в условиях, в которых похожие соединения водорода с более тяжелыми элементами (серой, селеном и т.д.) газообразны.
Молекула воды состоит из атома кислорода и двух атомов водорода,
В атоме водорода один неспаренный электрон, в атоме кислорода шесть валентных электронов, два из которых неспарены. Неспаренные электроны образуют две общие электронные пары по обменному механизму.
Неподелённые пары электронов на атоме кислорода «мешают» атомам находиться на одной линии, поэтому молекула воды имеет угловое строение. Валентный угол равен 104,5 градусов:
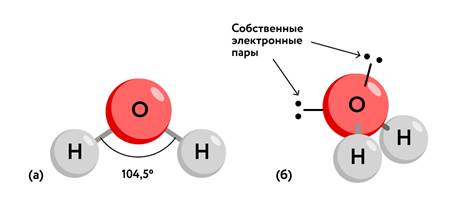
Рис. 1. Образование общих электронных пар и строение молекулы воды
Связь между атомами в молекуле воды ковалентная полярная. Электронная плотность смещена в сторону более электроотрицательного атома кислорода. Таким образом, в молекуле воды можно выделить «положительный полюс» (атом кислорода) и «отрицательный полюс» (атомы водорода).
Молекула воды является диполем ( Диполем называется система из двух одинаковых по величине, но разных по знаку электрических зарядов, находящихся на расстоянии друг от друга)..
Водородная связь
Между молекулами воды возникает водородная связь. Обратите внимание: данный тип взаимодействия является межмолекулярным, а не внутримолекулярным!








