14. окисления этанола оксидом меди (II)
15. бромирования фенола
16. межмолекулярной дегидратации этанола
17. нитрования фенола
сумма коэффициентов равна
1) 4
2) 5
3) 7
4) 8
18. В реакции этерификации группа ОН отщепляется от молекулы
1) спирта
2) альдегида
3) кетона
4) кислоты
19. С помощью хлорофилла в зеленом растении образуются
1) кислород
2) вода
3) глюкоза
4) этанол
20–21. Химические свойства глюкозы, характерные для
20. спиртов
21. альдегидов
проявляются в реакции
1) спиртового брожения
2) «серебряного зеркала»
3) этерификации
4) нейтрализации
22–24. При нагревании с водой в присутствии H2SO4 углевода
22. крахмал
23. целлюлоза
24. сахароза
после окончания гидролиза получают
1) этанол
2) фруктозу
3) глюконовую кислоту
4) глюкозу
25. Способы получения этанола – это
1) гидратация этена
2) брожение глюкозы
3) восстановление этаналя
4) окисление этаналя
26. Способы получения этиленгликоля – это
1) окисление этена
2) гидратация этена
3) действие щелочи на 1,2‑С2Н4Cl2
4) гидратация этина
27. Способы получения муравьиной кислоты – это
1) окисление метана
2) окисление фенола
3) окисление метанола
4) реакция СН3ОН с СО
28. Для синтеза уксусной кислоты используют соединения
1) С2Н5ОН
2) С4Н10
3) C2H5NO2
4) СН3ОН
29. Метанол применяется в производстве
1) пластмасс
2) каучуков
3) бензинов
4) жиров и масел
30. Для распознавания фенола (в смеси с бутанолом‑1) используют
1) индикатор и раствор щелочи
2) бромную воду
3) гидроксид меди (II)
4) аммиачный раствор оксида серебра (I)
31. Для распознавания в своих растворах глицерина, уксусной кислоты, ацетальдегида и глюкозы подходит один и тот же реактив
1) NaOH
2) Cu(OH)2
3) H2SO4 (конц.)
4) Ag2O (в р‑ре NH3)
32. Органическое вещество – продукт гидратации ацетилена, которое вступает в реакцию «серебряного зеркала», а при восстановлении образует этанол, – это
1) ацетальдегид
2) уксусная кислота
3) пропан
4) ацетон
33. Продукты А, Б, и В в схеме реакций СO2 + Н2O → фотосинтез А → брожение – СO2 Б → HCOOH B
– это соответственно
1) этанол
2) глюкоза
3) пропановая кислота
4) этилформиат
34. Фенол будет участвовать в процессах:
1) дегидратации
2) бромирования
3) изомеризации
4) нейтрализации
5) нитрования
6) «серебряного зеркала»
35. Возможно протекание реакций:
1) твердый жир + водород →…
2) муравьиная кислота + формальдегид →…
3) метанол + оксид меди (II) →…
4) сахароза + вода (в конц. H2SO4) →…
5) метаналь + Ag2O (в р‑ре NH3) →…
6) этиленгликоль + NaOH (р‑р) →…
36. Для промышленного синтеза фенолформальдегидной смолы следует взять набор реагентов
1) С6Н6, НС(Н)O
2) С6Н6, СН3С(Н)O
3) С6Н5ОН, НС(Н)O
4) С6Н5ОН, СН3С(Н)O
11. Азотсодержащие органические соединения
11.1. Нитросоединения. Амины
Очень важны в народном хозяйстве азотсодержащие органические вещества. Азот может входить в органические соединения в виде нитрогруппы NO2, аминогруппы NH2 и амидогруппы (пептидной группы) – C(O)NH, причем всегда атом азота будет непосредственно связан с атомом углерода.
Нитросоединения получают при прямом нитровании предельных углеводородов азотной кислотой (давление, температура) или при нитровании ароматических углеводородов азотной кислотой в присутствии серной кислоты, например:
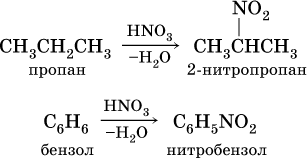
Низшие нитроалканы (бесцветные жидкости) используются как растворители пластмасс, целлюлозного волокна, многих лаков, низшие нитроарены (желтые жидкости) – как полупродукты для синтеза аминосоединений.
Амины (или аминосоединения) можно рассматривать как органические производные аммиака. Амины могут быть первичными R – NH2, вторичными RR'NH и третичными RR'R" N, в зависимости от числа атомов водорода, которые замещены на радикалы R, R', R". Например, первичный амин – этиламин C2H5NH2, вторичный амин – дижетиламин (CH3)2NH, третичный амин – триэтиламин (C2H5)3N.
Амины, как и аммиак, проявляют основные свойства, они в водном растворе гидратируются и диссоциируют как слабые основания:
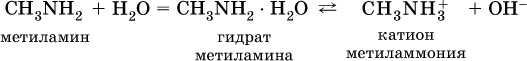
а с кислотами образуют соли:
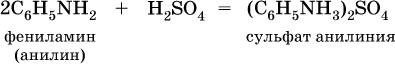
Третичные амины присоединяют галогенпроизводные с образованием солей четырехзамещенного аммония:
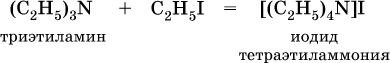
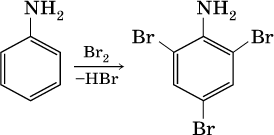
Ароматические ажины (в которых аминогруппа связана непосредственно с бензольным кольцом) являются более слабыми основаниями, чем алкиламины, из‑за взаимодействия неподеленной пары электронов атома азота с π‑электронами бензольного кольца. Аминогруппа облегчает замещение водорода в бензольном кольце, например на бром; из анилина образуется 2,4,6‑триброманилин:
Получение: восстановление нитросоединений с помощью атомарного водорода (получают либо непосредственно в сосуде по реакции Fe + 2НCl = FeCl2 + 2Н0, либо при пропускании водорода Н2 над никелевым катализатором Н2 = 2Н0) приводит к синтезу первичных аминов:
a)
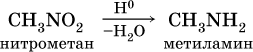
б) реакция Зинина
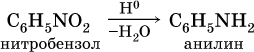
Амины используются в производстве растворителей для полимеров, лекарственных препаратов, кормовых добавок, удобрений, красителей. Очень ядовиты, особенно анилин (желто‑коричневая жидкость, всасывается в организм даже через кожу).
11.2. Аминокислоты. Белки
Аминокислоты – органические соединения, содержащие в своем составе две функциональные группы – кислотную СООН и аминную NH2; являются основой белковых веществ.
Примеры:

Аминокислоты проявляют свойства и кислот, и аминов. Так, они образуют соли (за счет кислотных свойств карбоксильной группы):
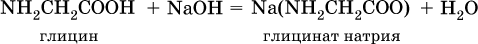
и сложные эфиры (подобно другим органическим кислотам):
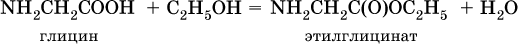
С более сильными (неорганическими) кислотами они проявляют свойства оснований и образуют соли за счет основных свойств аминогруппы:
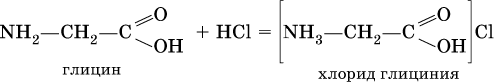
Реакцию образования глицинатов и солей глициния можно объяснить следующим образом. В водном растворе аминокислоты существуют в трех формах (на примере глицина):
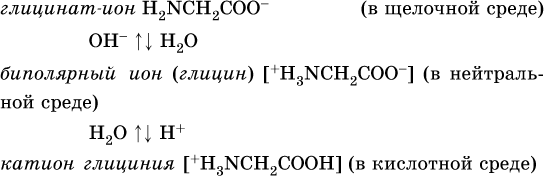
Поэтому глицин в реакции со щелочами переходит в глицинат‑ион, а с кислотами – в катион глициния, равновесие смещается соответственно в сторону образования анионов или катионов.
Белки – органические природные соединения; представляют собой биополимеры, построенные из остатков аминокислот. В молекулах белков азот присутствует в виде амидогруппы – С(О) – NH– (так называемая пептидная связь С – N). Белки обязательно содержат С, Н, N, О, почти всегда S, часто Р и др.
При гидролизе белков получают смесь аминокислот, например:
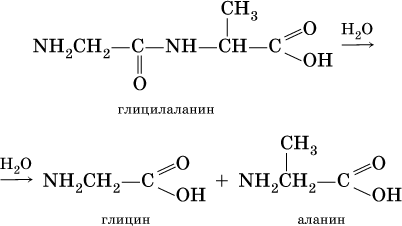
По числу остатков аминокислот в молекуле белка различают дипептиды (приведенный выше глицилаланин), трипептиды и т. д. Природные белки (протеины) содержат от 100 до 1 105 остатков аминокислот, что отвечает относительной молекулярной массе 1 • 104 – 1 • 107.
Образование макромолекул протеинов (биополимеров), т. е. связывание молекул аминокислот в длинные цепи, происходит при участии группы СООН одной молекулы и группы NH2 другой молекулы:

Физиологическое значение белков трудно переоценить, не случайно их называют «носителями жизни». Белки – основной материал, из которого построен живой организм, т. е. протоплазма каждой живой клетки.
При биологическом синтезе белка в полипептидную цепь включаются остатки 20 аминокислот (в порядке, задаваемом генетическим кодом организма). Среди них есть и такие, которые не синтезируются вообще (или синтезируются в недостаточном количестве) самим организмом, они называются незаменимыми аминокислотами и вводятся в организм вместе с пищей. Пищевая ценность белков различна; животные белки, имеющие более высокое содержание незаменимых аминокислот, считаются для человека более важными, чем растительные белки.
Примеры заданий частей А, В, С
1–2. Класс органических веществ
1. нитросоединения
2. первичные амины
содержит функциональную группу
1) – О – NO2
2) – NO2
3) – NH2
4) – NO3‑
3. Водородные связи образуются между молекулами
1) формальдегида
2) пропанола‑1
3) циановодорода
4) этиламина
4. Число структурных изомеров из группы предельных аминов для состава C3H9N равно
1) 1
2) 2
3) 3
4) 4
5. В водном растворе аминокислоты CH3CH(NH2)COOH химическая среда будет
1) кислотной
2) нейтральной
3) щелочной
4) любой
6. Двойственную функцию в реакциях выполняют (по отдельности) все вещества набора
1) глюкоза, этановая кислота, этиленгликоль
2) фруктоза, глицерин, этанол
3) глицин, глюкоза, метановая кислота
4) этилен, пропановая кислота, аланин
7–10. Для реакции в растворе между глицином и
7. гидроксидом натрия
8. метанолом
9. хлороводородом
10. аминоуксусной кислотой продуктами будут
1) соль и вода
2) соль
3) дипептид и вода
4) сложный эфир и вода
11. Соединение, которое реагирует с хлороводородом, образуя соль, вступает в реакции замещения и получается восстановлением продукта нитрования бензола, – это
1) нитробензол
2) метиламин
3) анилин
4) фенол
12. При добавлении лакмуса к бесцветному водному раствору 2‑аминопропановой кислоты раствор окрашивается в цвет:
1) красный
2) желтый
3) синий
4) фиолетовый
13. Для распознавания изомеров со строением СН3–СН2–СН2–NO2 и NH2–СН(СН3) – СООН следует использовать реактив
1) пероксид водорода
2) бромная вода
3) раствор NaHCO3
4) раствор FeCl3
14. При действии концентрированной азотной кислоты на белок появляется… окрашивание:
1) фиолетовое
2) голубое
3) желтое
4) красное
15. Установите соответствие между названием соединения и классом, к которому оно относится

16. Анилин действует в процессах:
1) нейтрализация муравьиной кислотой
2) вытеснение водорода натрием
3) получение фенола
4) замещение с хлорной водой
17. Глицин участвует в реакциях
1) окисления с оксидом меди (II)
2) синтеза дипептида с фенилаланином
3) этерификации бутанолом‑1
4) присоединения метиламина
18–21. Составьте уравнения реакций по схеме
18.
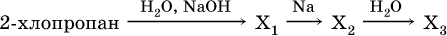
19.
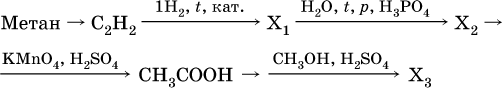
20.
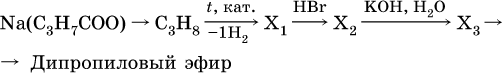
21.

12. Химические реакции. Скорость, энергетика и обратимость
12.1. Скорость реакций
Количественной характеристикой быстроты течения химической реакции А + B → D + E является ее скорость, т. е. скорость взаимодействия частиц реагентов А и В или скорость появления продуктов D и Е. Изучением скорости химических реакций занимается особый раздел химии – химическая кинетика.
В гомогенных (однородных) системах исследуется скорость реакции между реагентами, не имеющими границы раздела (газовые реакции, реакции в растворах). В гетерогенных системах изучается скорость реакции на поверхности раздела между реагирующими веществами (например, А – твердое вещество, В – газ или А – твердое вещество, В – вещество в растворе).
Для гомогенных систем скорость реакции – это изменение концентраций реагентов или продуктов в единицу времени:
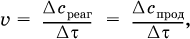
где v – скорость реакции, моль/(л с);
Δcреаг = (с'реаг – с"реаг) ― уменьшение концентрации реагентов, моль/л, за промежуток времени Δτ = τ2 – τ1;
Δcпрод = (с"прод – с'прод) – увеличение концентрации продуктов, моль/л, за тот же промежуток времени.
В начальный момент времени (τ = 0) концентрация реагентов наибольшая, а концентрация продуктов равна нулю. В процессе реакции концентрация реагентов уменьшается, а концентрация продуктов растет.
К факторам, влияющим на скорость реакции, относятся природа реагентов, катализатор, температура, концентрация реагентов.
1. Природа реагентов. Здесь большую роль играет характер химических связей в соединениях, строение их молекул. Например, выделение водорода цинком из раствора хлороводорода происходит значительно быстрее, чем из раствора уксусной кислоты, так как полярность связи Н – Cl больше, чем связи О – Н в молекуле СН3СООН; иначе говоря, из‑за того, что НCl – сильный электролит, а СН3СООН – слабый электролит в водном растворе.
Чем больше поверхность соприкосновения реагирующих веществ, тем быстрее протекает реакция. Поверхность твердого вещества может быть увеличена путем его измельчения или растворения (если вещество растворимо). Реакции в растворах протекают практически мгновенно.
2. Катализаторы. Большое влияние на скорость реакции оказывают катализаторы – вещества, увеличивающие скорость реакции (часто от нуля до очень больших значений), но не входящие в состав продуктов. Увеличение скорости реакции под влиянием катализаторов называется катализом. Во многих случаях катализаторы образуют с одним из реагирующих веществ промежуточное соединение, которое реагирует с другим исходным веществом, в результате получается продукт и высвобождается катализатор.
Иногда употребляют отрицательные катализаторы – ингибиторы, которые, наоборот, замедляют нежелательные химические реакции (например, коррозию металлов).
3. Температура. Для газовых реакций известно, что при повышении температуры на десять градусов (ΔТ = 10 К или Δt = 10 °C) скорость реакции возрастает в 2–4 раза (правило Вант‑Гоффа). Для скорости реакции ν2 и ν1 при значениях температуры t2 и t1 имеем:
ν2 = ν1 γ0,1(t2‑t1),
где γ – температурный коэффициент скорости реакции, γ = 2–4.
Для реакций в растворах скорость также увеличивается с ростом температуры и часто в той же мере, как и для газовых реакций.
При повышении температуры возрастает число активных молекул, т. е. таких молекул, которые в момент столкновения обладают большей энергией и могут образовать продукты.
Как показывают исследования, активных молекул в реакционной среде при обычных условиях очень мало. Иначе все реакции между газами протекали бы мгновенно, и в воздухе не было бы, например, свободного кислорода, необходимого для дыхания. Реакции между газами при обычных условиях практически не идут (встречаются исключения, например, при 20 °C полностью протекает реакция 2NO + O2 = 2NO2).
4. Концентрация реагентов. Чтобы произошло взаимодействие, частицы реагирующих веществ в гомогенной среде должны столкнуться. Число столкновений пропорционально числу частиц реагирующих веществ в объеме реактора, т. е. молярным концентрациям этих веществ.
Чем большие количества веществ взяты для реакции в данном объеме системы, т. е. чем выше концентрация реагентов, тем больше число столкновений частиц и тем больше скорость реакции. Зависимость скорости реакции от концентрации реагентов распространяется на газовые смеси и растворы.
Установлено, что:








