Третичные радикалы стабильнее, чем вторичные, которые стабильнее первичных (трет.>втор.> перв.).
Это приводит к тому, что третичные атомы водорода замещаются проще всего (так как связь С-Н при третичном углероде проще всего рвется- ведь при этом образуются наиболее стабильные из всех возможных радикалов).
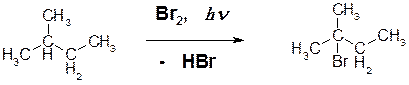
23. Приведите механизм реакции хлорирования метана, приводящей к хлорметану.
Ответ:
Схема реакции хлорирования имеет вид:
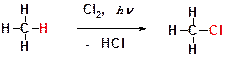
Считается, что процесс хлорирования включает несколько стадий: зарождения цепи, развития цепи и обрыва цепи. Стоит обратить внимание на то, что процесс хлорирования метана носит цепной радикальный характер, связи рвутся гомолитически, а образуются по обменному механизму:


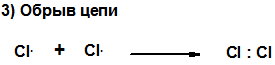
При анализе механизма реакции особо следует остановиться на двух стадиях развития цепи. Если сложить эти реакции и сократить частицы, находящиеся в правой и левой частях одновоременно, то тогда мы получим:
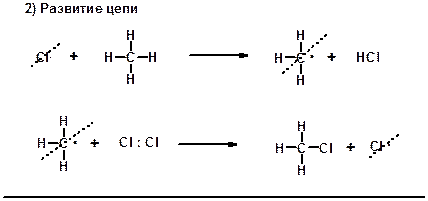
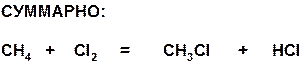
Таким образом, можно сказать, что атомы хлора (или метильные радикалы) являются катализатором реакции замещения, поскольку ускоряют процесс, но сами при этом не расходуются. Атомы хлора называют носителями цепи, а две стадии развития цепи повторяются многократно: атом хлора, образовавшийся на второй стадии развития цепи вновь взаимодействует с новой молекулой метана (смотри первую стадию развития цепи). Таким образом, хлорирование метана – цепной радикальный процесс.
24. Какие соединения относят к классу алкенов?
Ответ: Алкенами называются углеводороды (соединения, состоящие из углерода и водорода), которые в своей структуре содержат одну двойную углерод-углеродную связь С=С. Считается, что одна из этих связей (более прочная) является σ-связью (сигма-связью), а другая (более слабая) – π-связью (пи-связью). Общая формула алкенов СnH2n. Простейший представитель алкенов – молекула этилена:
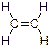
25. Назовите следующие соединения по систематической номенклатуре IUPAC:
А) 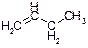
ОТВЕТ: Бутен-1. Пояснение: Название алкенов строится путем замены окончания «ан» в соответствующем алкане на окончание «ен». В нашем случае, поскольку соединение содержит четыре последовательно связанные атома углерода, то основой названия является слово «бутен» (соответствующий алкан - бутан). Однако необходимо также указать положение двойной связи. Для этой цели, атомы углерода нумеруются начиная с того конца молекулы, к которому ближе двойная связь. В нашем случае двойная связь находится между первым и вторым углеродными атомами. В названии отражают место, где начинается двойная связь, то есть первый атом углерода и название соединения: бутен-1.
Б) 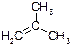
ОТВЕТ: 2-метилпропен-1. Пояснение: выбирают самую длинную углеродную цепь и нумеруют с того конца, к которому ближе связь С=С. Указывают наличие заместителя (в данном случае метильной группы) при втором атоме углерода. Название этого соединения – 2‑метилпропен-1 – отражает тот факт, что оно может быть получено заменой атома водорода в молекуле пропена при центральном (втором) углеродном атоме на метильную группу.
В) 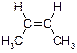
Ответ: цис-бутен-2. Пояснение: смотри предыдущие примеры. Приставка цис в данном случае обозначает, что бутен-2 способен существовать в виде двух пространственных изомеров: цис и транс. В нашем случае речь идет о цис-изомере, поскольку метильные группы находятся по одну сторону от двойной связи.
Г) 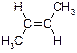
Ответ: транс-бутен-2. Пояснение: В этом случае речь идет о транс-изомере, поскольку метильные группы находятся по разные стороны от двойной связи.
26. Поясните, как Вы понимаете тот факт, что бутен-2 способен существовать в виде цис и транс-изомеров?
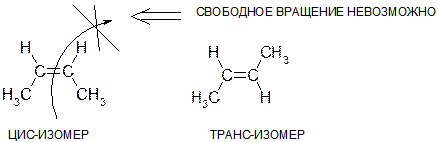
Ответ: Центральные атомы углерода связаны двойной связью, относительно которой невозможно свободное вращение. Поэтому цис-изомер не может свободно проходить в транс-изомер. Существуют два совершенно различных вещества – цис-бутен-2 и транс-бутен-2, в которых метильные группы по-разному расположены относительно двойной связи.
27. Какие реакции наиболее характерны для алкенов? Приведите несколько примеров.
Ответ: Алкенам наиболее характерны реакции присоединения. Типичным примером является реакция каталитического гидрирования, когда алкен CnH2n превращается в алкан CnH2n+2 за счет присоединения молекулы водорода Н2.
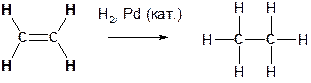
В таких реакциях происходит разрыв сравнительно слабой π-связи, при этом к каждому из атомов углерода присоединяется по одному атому водорода, чтобы углерод оставался четырехвалентным.
Аналогично происходит присоединение галогенов, к примеру, брома Br2:
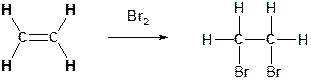
ПОЯСНЕНИЕ: Суть реакций присоединения к алкенам заключается в том, что в двойной связи С=С происходит разрыв более слабой π-связи, и к каждому из атомов углерода присоединяется одновалентный атом (типа H, Cl, Br) или одновалентный остаток (типа ОН). Все остальные связи, которые были в исходном алкене остаются незатронутыми и сохраняются в продукте реакции. Ниже изображена упрощенная схема, иллюстрирующая протекание реакций присоединения по двойной углерод-углеродной связи алкенов.

28. Приведите структурные формулы продуктов следующих реакций, приведите названия образующихся продуктов:
ОТВЕТЫ:
А) 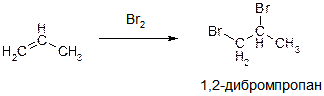
Б) 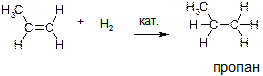
В) 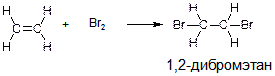
Г) 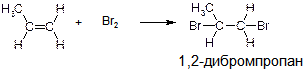
ПОЯСНЕНИЕ: РОВНО ЭТА ЖЕ РЕАКЦИЯ НАПИСАНА В ПРИМЕРЕ «А». ТО, что исходная молекула написана чуть иначе ничего не меняет. В обоих случаях исходным веществом является пропен, а продуктом – 1,2-дибромпропан.
Д) 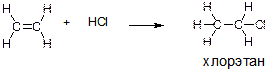
Е) 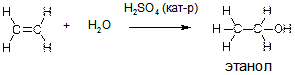
ПОЯСНЕНИЕ: РЕАКЦИЯ ПРИСОЕДИНЕНИЯ ВОДЫ К АЛКЕНАМ НОСИТ НАЗВАНИЕ «РЕАКЦИИ ГИДРАТАЦИИ».
Ж) 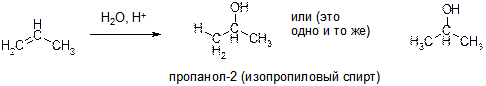
ПОЯСНЕНИЕ: Для реакций алкенов (с несимметрично замещённой двойной связью) с водой и галогеноводородами (H2O, HCl, HBr) необходимо решить: к которому из атомов C присоединится H, а к которому - OH или галоген? Чаще всего можно воспользоваться правилом Марковникова и присоединить атом H к тому атому углерода двойной связи, который связан с большим количеством атомов водорода (наиболее «гидрогенизированный»)

З) 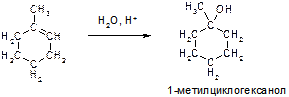
Пояснение: реакция гидратации, подчиняется правилу Марковникова.
И) 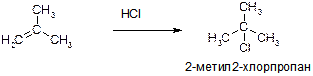
Пояснение: реакция протекает в соответствии с правилом Марковникова.
К) 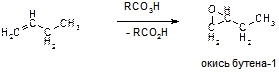
Пояснение: реакция эпоксидирования алкенов по Прилежаеву, происходящая при действии надкислот (RCO3H). Продуктами реакции являются эпоксиды – соединения, содержащие трехчленный цикл.
Л) 
Пояснение: реакция протекает по правилу Марковникова.
М) 
Пояснение: Присоединение бромистого водорода (HBr) может быть проведено против правила Марковникова, если проводить реакцию в присутствии органической перекиси (ROOR). Это явление названо «эффект Караша» по имени изучившего его ученого. Таким образом, присоединение бромоводорода может быть проведено как по так и против правила Марковникова в зависимости от условий проведения реакции (сравни с предыдущим примером). При этом образуются изомерные продукты.
Н) 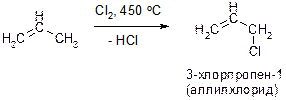
Пояснение: Эта реакция не является типичной для алкенов реакцией присоединения. По сути, эта реакция представляет собой реакцию замещения (аналогично алканам) атома водорода на атом хлора (в качестве побочного продукта образуется хлороводород). 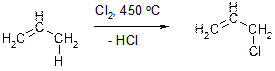 Причиной того, что идет реакция замещения, а не более характерная для алкенов реакция присоединения, являются условия процесса: очень сильное нагревание (450 оС).
Причиной того, что идет реакция замещения, а не более характерная для алкенов реакция присоединения, являются условия процесса: очень сильное нагревание (450 оС).
О) 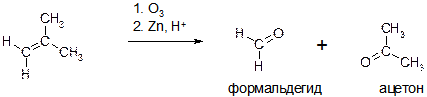
Пояснение: Реакция «восстановительного» озонолиза, приводит к фрагментации («разрезанию») молекулы алкена по месту двойной связи (С=С). Продуктами являются соответствующие карбонильные соединения (альдегиды и кетоны).
29. Приведите структурные формулы продуктов следующих реакций, приведите названия образующихся продуктов:
ОТВЕТЫ:
А) 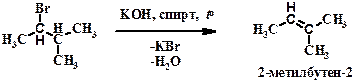
Пояснение: Реакция дегидрогалогенирования (отщепления галогеноводорода) под действием щелочи. В данном случае отщепляется HBr, при этом за счет взаимодействия бромоводорода с гидроксидом калия образуются КBr и Н2О, которые и указаны в качестве выделяющихся неорганических продуктов.
Реакция отщепления (элиминирования) является реакцией, обратной реакции присоединения к двойной углерод-углеродной связи алкенов. В данном случае от каждого из двух соседних углеродных атомов отщепляется одновалентный атом (H и Br), при этом между двумя атомами углерода формируется дополнительная связь (π-связь), так что в продукте эти атомы связаны не одинарной, а двойной связью.
Реакция подчиняется правилу Зайцева: водород отщепляется от менее гидрогенизированного углеродного атома. Иными словами, в вышеприведенной реакции есть два альтернативных варианта отщепления атома водорода, но реализуется отщепление атома водорода от третичного атома углерода (менее гидрогенизированного). 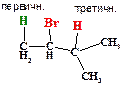
Б) 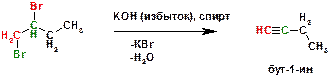
Пояснение: Реакция дегидрогалогенирования (отщепления галогеноводорода) под действием щелочи. Под действием избытка щелочи отщепляется два моль HBr и формируется тройная связь (за счет формирования двух π-связей).
В) 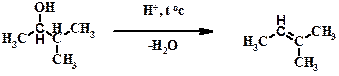
Пояснение: реакция дегидратации, является реакцией, обратной реакции присоединения воды к алкенам (реакции гидратации). От одного атома углерода отщепляется спиртовая группа (ОН), а от соседнего – атом водорода (Н). Реакция подчиняется правилу Зайцева: водород отщепляется от менее гидрогенизированного атома углерода (то есть преимущественно от третичного).
Г) 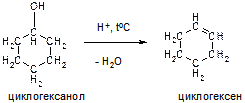
Пояснение: реакция дегидратации (смотри выше).
Д) 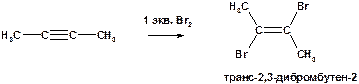
Пояснение: реакция присоединения по тройной связи, полностью аналогична реакции присоединения брома (Br2) к алкенам. Особенность состоит в том, что при присоединении 1 эквивалента Br2 образуется ненасыщенное соединение (содержит двойную связь С=С), которое может вступать во взаимодействие со вторым молем брома. Особенностью реакции является образование транс-изомера (процесс анти-присоединения).
Е) 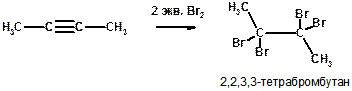
Пояснение: при действии двух эквивалентов брома (то есть двух молей брома на один моль субстрата) происходит разрыв двух π-связей, поэтому в продукте центральные атомы углерода связаны не тройной, а одинарной связью. Чтобы эти атомы углерода, оставались четырехвалентными к каждому из них присоединяется по два атома брома.
Эту реакцию можно пояснить и иначе. Сравните ее с предыдущей, где присоединяется 1 моль брома. Образующийся после присоединения 1 моль Br2 транс-дибромид вступает во взаимодействие со вторым молем брома с образованием конечного продукта 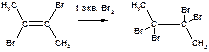
Ж) 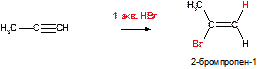
Пояснение: реакция присоединения. Выполняется правило Марковникова: водород присоединяется к более гидрогенизированному атому углерода.
З) 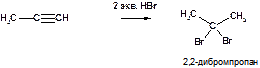
Пояснение: Образующееся после присоединения 1 моль HBr соединение (смотри предыдущую реакцию) является ненасыщенным (так как содержит двойную связь С=С), а потому может вступать во взаимодействие со вторым молем HBr, причем реакция опять подчиняется правилу Марковникова.
И) 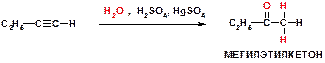
Пояснение: Реакция гидратации алкинов (РЕАКЦИЯ КУЧЕРОВА). Катализируется серной кислотой и солями ртути. Подчиняется правилу Марковникова, поэтому водород присоединился к крайнему (а не центральному) атому углерода. Протекает несколько отлично от других реакций (обсужденных выше): рвется сразу две π-связи, причем к крайнему атому присоединяется два одновалентных атома водорода, а к центральному – один двухвалентный атом кислорода (суммарно присоединилась Н2О).
К) 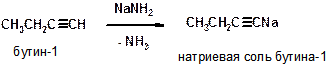
Пояснение: Реакция, отражающая слабый кислотные свойства терминальных алкинов (то есть содержащих тройную связь на конце молекулы). Для получения солей необходимо действие более сильных оснований, чем щелочи (KOH, NaOH), к примеру, таких, как амид натрия NaNH2. Амид-анион (NH2-) отрывает протон (Н+) от молекулы алкина (кислотно-основное взаимодействие). При том образуется малодиссоциированное вещество – молекула аммиака (NH3).
K) 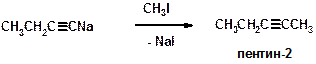
Пояснение: применение ацетиленидов щелочных металлов в синтезе алкинов. Реакция относится к реакциям нуклеофильного замещения: иодид-анион вытесяется другим нуклеофилом: ацетиленид-анионом.
Л) 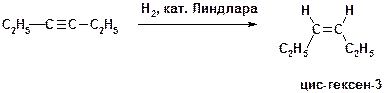
Пояснение: Реакция каталитического гидрирования. Реакция может быть проведена путем присоединения лишь одного эквивалента водорода (H2) при использовании специальных катализаторов, например, катализатора Линдлара. Продуктом является алкен с цис-конфигурацией двойной связи (син-присоединение водорода).
М) 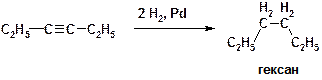
Пояснение: Если использовать обычные катализаторы (на основе палладия, платины, никеля), то реакцию не удается остановить на стадии присоединения одного эквивалента водорода, поскольку образующийся алкен подвергается дальнейшему гидрированию.
Н) 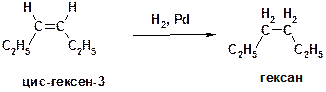
Пояснение: реакция каталитического гидрирования алкена (ненасыщенного соединения), ведущая к образованию алкана (насыщенного соединения) с тем же углеродным скелетом. Реакция сопровождается разрывом сравнительно слабой π-связи.
О) 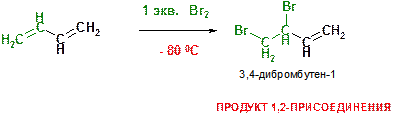
Пояснение: При пониженной температуре сопряженные диены (каковым является бутадиен-1,3) вступают в обычную реакцию присоединения по связи С=С. Поскольку обе двойные связи в молекуле бутадиена идентичны, то вне зависимости от того, по какой из них произошло присоединение образуется 3,4-дибромбутен-1. Этот продукт также называют продуктом 1,2-присоединения, так как атомы галогена присоединились к соседним атомам углерода.
П) 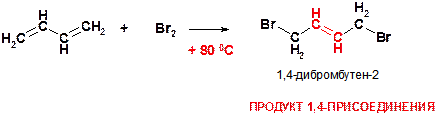
Пояснение: При повышенной температуре сопряженные диены (каковым является бутадиен-1,3) вступают в реакцию 1,4-присоединения по сопряженной диеновой системе. Образующийся продукт также называют продуктом 1,4-присоединения, так как атомы галогена присоединились к крайним (то есть первому и четвертому) атомам углерода диеновой системы. При этом, чтобы присоединиться к первому атому углерода должна разорваться одна π-связь, а для присоединения к другому крайнему атому углерода – должна разорваться другая π-связь. Таким образом, в образующемся продукте нет обоих π-связей, которые присутствовали в исходной молекуле. Зато π-связь формируется между центральными атомами углерода, чтобы они сохраняли свою нормальную валентность – четыре (при ее отсутствии они бы оставались трехвалентными).
Р) 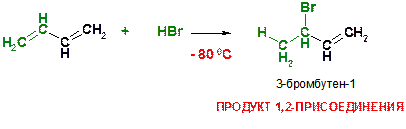
Пояснение: При пониженной температуре реализуется процесс 1,2-присоединения (смотри выше). В данном случае для правильного написания продукта необходимо применить правило Марковникова: атом водорода присоединяется к крайнему атому углерода, поскольку тот образует целых две связи С‑Н (то есть более гидрогенизирован).
С) 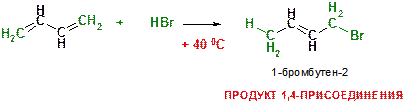
Пояснение: При повышенной температуре реализуется процесс 1,4-присоединения (смотри выше).
Т) 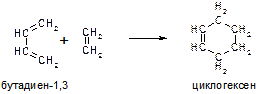
Пояснение: реакция Дильса-Альдера, диен реагирует с алкеном (диенофилом) с образованием циклогексена или его производного.








