57 Колонные экстракторы (полые, насадочные, тарельчатые, роторно-дисковые, с пульсацией потоков)
1) полые
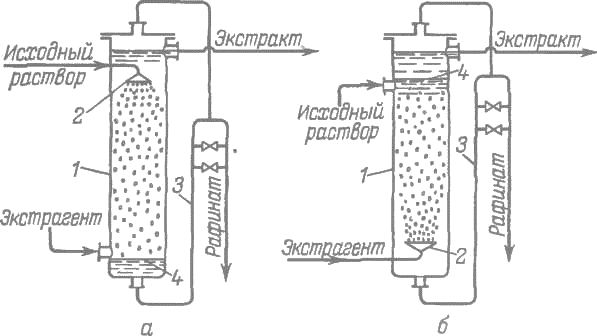
Рис. 18-16. Полые (распылительные) колонные экстракторы:
а -с распылением тяжелой фазы; б—с распылением легкой фазы; 1—экстракторы; 2-разбрызгиватели; 3 гидрозатворы; 4-поверхности раздела фаз
Они представляют собой полые колонны 1 с устройствами 2 для диспергирования тяжелой (рис. 18-16,а) или легкой (18-16,б) фаз (исходного раствора или экстрагента). Сплошная фаза перемещается противотоком дисперсной. Капли диспергированной жидкости, пройдя сквозь столб сплошной фазы, коалесцируют и выходят из колонны. Тяжелая фаза уходит через гидрозатвор 3, с помощью которого регулируют уровень раздела фаз в колонне.
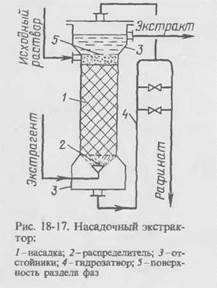 2) Насадочные абсорберы
2) Насадочные абсорберы
В качестве насадки 1 часто используют кольца Рашига, а также и насадки других типов. Насадку располагают на опорных решетках секциями, между которыми происходит перемешивание фаз. Одну из фаз диспергируют с помощью распределительного устройства 2 в потоке сплошной фазы (исходный раствор). Разделение фаз в насадочных колоннах происходит в отстойных зонах 3, часто имеющих больший диаметр, чем диаметр экстрактора, для лучшей сепарации фаз.
3) Из тарельчатых в промышленности наибольшее применение нашли ситчатые экстракторы (рис. 18-18).
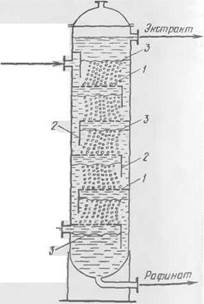
Рис 18-18 Экстрактор с ситчатыми тарелками
1 Тарелки, 2 перетоки тяжелой фазы с тарелки на тарелку, 3-границы расслаивающихся фаз
В этих аппаратах одна из жидких фаз многократно диспергируется и коалесцирует, проходя через большое число сверленых или штампованных отверстий в тарелке 1.
В ситчатых экстракторах сплошная фаза течет вдоль тарелки 1 и перетекает с тарелки на тарелку через переливные устройства 2. После взаимодействия со сплошной фазой капли коалесцируют и образуют слой легкой фазы под каждой вышерасположенной тарелкой. Если диспергируется тяжелая фаза, то слой этой жидкости образуется над тарелками. Эти слои, которые называют подпорными, обеспечивают секционирование колонны по высоте и перетекание сплошной фазы только через переливные устройства. Кроме того, эти слои создают гидростатический напор, необходимый для преодоления сопротивления отверстий тарелки, вследствие чего жидкость, проходя через отверстия тарелки, вновь диспергируется.
4) Роторно - дисковые
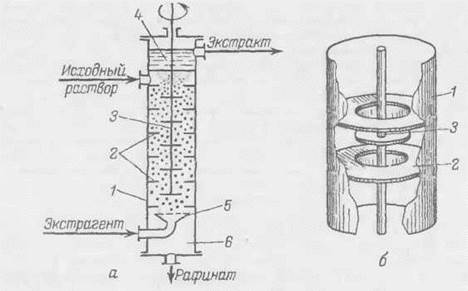
Рис. 18-19. Роторно-дисковый экстрактор (я) и один из вариантов его секции (б):
1 - колонна; 2 - кольцевые перегородки; 3 - вал ротора с плоскими дисками; 4,6- отстойные зоны соответственно для легкой и тяжелой фаз; 5-распределитель легкой фазы
В этом экстракторе на равном расстоянии друг от друга укреплены неподвижные кольцевые перегородки 2 (статор), делящие колонну на ряд секций небольшого объема. По оси колонны 1 на валу 3 располагаются гладкие горизонтальные диски (ротор). При вращении вала с дисками под действием сил трения и центробежных сил возникает движение сплошной фазы к стенкам аппарата, достигнув которых, жидкость движется вверх и вниз вдоль стенки и отражается кольцами статора. На это движение жидкости накладывается осевое. Диспергируемая распределителем 5 легкая фаза (экстрагент) движется противотоком к сплошной.
В результате в каждом секции возникают тороидальные замкнутые потоки сплошной фазы, приводящие к интенсивному перемешиванию фаз. В отстойных зонах 4 и 6 фазы разделяются и затем выходят из аппарата.
5) Пульсационные
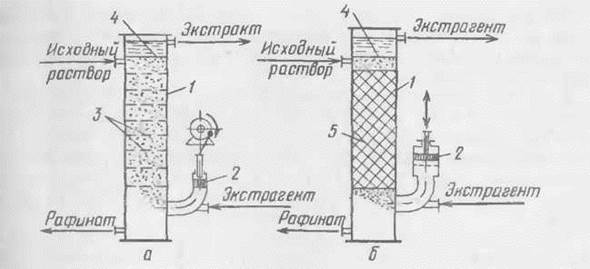
Рис. 18-20. Пульсационные экстракторы с тарелками (а) и насадкой (б):
1-колонны, 2- поршневые пульсаторы; 3-тарелки: 4-поверхности раздела фаз в отстойных зовах; 5-насадка
Применяют два основных способа сообщения пульсаций жидкостям. По первому способу пульсации в колонном экстракторе генерируются наружным механизмом (пульсатором) гидравлически, по второму-посредством вибрации перфорированных тарелок, укрепленных на общем штоке, которому сообщается возвратно-поступательное движение.
58. Кристаллизация, основные понятия. Стадии процесса.
Кристаллизацией называют выделение твердой фазы в виде кристаллов главным образом из растворов и расплавов. Кристаллы представляют собой однородные твердые тела различной геометрической формы, ограниченные плоскими гранями. Каждому химическому соединению обычно соответствует одна или несколько кристаллических форм, отличающихся положением и числом осей симметрии. Явление образования нескольких кристаллических форм у данного химического соединения носит название полиморфизма. Кристаллы, включающие молекулы воды, называют кристаллогидратами, причем в зависимости от условий проведения процесса кристаллизации одно и то же вещество может кристаллизоваться с разным числом молекул воды.
В химической технологии процессы кристаллизации широко используют для получения в чистом виде различных веществ. Осуществляемое в промышленном масштабе одновременное получение большого числа кристаллов носит название массовой кристаллизации.
Массовую кристаллизацию обычно проводят из водных растворов, понижая растворимость кристаллизуемого вещества за счет изменения температуры раствора или удаления части растворителя. В ряде случаев кристаллизацию ведут из растворов органических веществ (спиртов, эфиров, углеводородов и др.).
Кристаллизацию из расплавов осуществляют путем их охлаждения.
Кристаллы можно получать также возгонкой и последующим охлаждением образующегося пара при температуре ниже температуры «тройной» точки.
В производственных условиях процесс кристаллизации состоит из следующих операций: собственно, кристаллизации, отделения кристаллов от маточных растворов, перекристаллизации (в случае необходимости), промывки и сушки кристаллов.
59. Физические основы процесса кристаллизации, мера стабильности пересыщенного раствора, равновесие при кристаллизации
Для веществ с положительной растворимостью, она увеличивается с увеличением температуры, а с отрицательной – растворимость с ув Т уменьшается. Раствор, находящийся в равновесии с тв фазой, называется насыщенным. При некоторых условиях, концентрация вещества может быть больше его растворимости – такие растворы называют пересыщенными. Они не стабильны и легко переходят в насыщенное состояние, при этом из раствора выделяется тв фаза – кристаллы. Для того чтобы они были крупными, кристаллизацию необходимо вести из метастабильной области, то есть из растворов с умеренной степенью пересыщения.
60. Скорость кристаллизации, влияние различных факторов на скорость процесса.
На скорость кристаллизации оказывает влияние ряд факторов: степень пересыщения раствора, его температура, образование зародышей кристаллов, интенсивность перемешивания, наличие примесей и др. При массовой кристаллизации из растворов возникновение кристаллических зародышей и рост из них кристаллов протекают одновременно, что затрудняет изучение кинетики процесса.
Образование зародышей. Зародыши, или центры кристаллизации, образуются в пересыщенных или переохлажденных растворах самопроизвольно. По современным воззрениям, зародыши возникают за счет образования ассоциаций частиц при столкновении в растворе отдельных ионов (молекул) растворенного вещества и постепенно достигают субмикроскопических размеров. Зародыши находятся в подвижном равновесии с раствором и видимой кристаллизации не происходит. Такой скрытый период начала кристаллизации называют индукционным. В зависимости от природы растворенного вещества и растворителя, степени пересыщения, наличия примесей индукционный период может продолжаться от нескольких секунд до нескольких месяцев Его можно сократить путем внесения в пересыщенный раствор кристалликов растворенного вещества — «затравки». Начало массовой видимой кристаллизации соответствует моменту нарушения подвижного устойчивого равновесия между зародышем и раствором.
Скорость образования зародышей может быть увеличена путем повышения температуры, перемешивания раствора, внешних механических воздействий (встряхивание, удары, трение и др.). Большое влияние на процесс образования зародышей могут также оказывать шероховатость стенок кристаллизатора, материал мешалки, присутствие в растворе твердых тел с большой поверхностью (ленты, нити и др.).
Рост кристаллов. Кристалл растет на сформировавшемся, достигшем критической величины зародыше. Он обладает большой поверхностной энергией, за счет которой адсорбируются все новые частицы растворенного вещества. Адсорбировать частицы из раствора могут также твердые частицы другого обладающего соответствующей поверхностной энергией вещества. Они становятся, таким образом, центрами кристаллизации. В последнем случае процесс носит название кристаллизации на подложке.
Рост кристаллов происходит одновременно по всем его граням, однако при различных линейных скоростях роста отдельных граней. Одни из них исчезают, другие — развиваются, что приводит к изменению внешнего вида кристалла.
Предложено несколько теорий роста кристаллов: По диффузионной теории, например, растворенное вещество первоначально диффундирует из глубины раствора через ламинарный пограничный подслой у поверхности кристалла, затем подведенное вещество как бы встраивается в тело кристалла.
Толщина ламинарного подслоя вблизи поверхности кристалла зависит от интенсивности перемешивания раствора. На неподвижных кристаллах в неподвижном растворе толщина ламинарного подслоя δ равна 20 — 150 мкм, в сильно перемешиваемых растворах δ → 0.
При большой скорости процесса встраивания кристаллизуемого вещества рост кристалла будет определяться молекулярной диффузией вещества через пленку раствора у поверхности кристалла; напротив, при низкой скорости встраивания решающей будет скорость встраивания.
Диффузионная теория роста кристаллов не объясняет ряд явлений, происходящих при кристаллизации (различная скорость роста граней, дефекты, слоистость и пр.). Согласно этой теории, процессы растворения и кристаллизации обратимы, однако доказано, что это не так. Часто при одинаковых значениях движущей силы (разности концентраций) рост кристаллов протекает гораздо медленнее, чем растворение.
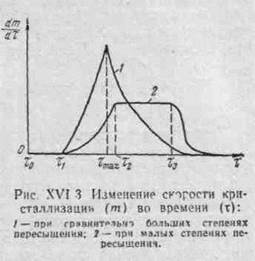 Скорость кристаллизации не является постоянной. Она изменяется во времени в зависимости от условий кристаллизации в широких пределах. Вначале скорость равна нулю (период индукции), потом достигает "кратковременного максимума и снова уменьшается до нуля (рис.). При сравнительно большой степени пересыщения раствора наблюдается резкий максимум скорости (кривая 1). При малой степени пересыщения или наличии тормозящих кристаллизацию примесей период индукции достаточно велик и на кривой 2 наблюдается горизонтальный участок τ2 — τ3, т. е. максимальная скорость в течение некоторого времени имеет постоянное значение.
Скорость кристаллизации не является постоянной. Она изменяется во времени в зависимости от условий кристаллизации в широких пределах. Вначале скорость равна нулю (период индукции), потом достигает "кратковременного максимума и снова уменьшается до нуля (рис.). При сравнительно большой степени пересыщения раствора наблюдается резкий максимум скорости (кривая 1). При малой степени пересыщения или наличии тормозящих кристаллизацию примесей период индукции достаточно велик и на кривой 2 наблюдается горизонтальный участок τ2 — τ3, т. е. максимальная скорость в течение некоторого времени имеет постоянное значение.
Температура кристаллизации в общем оказывает положительное влияние на скорость роста кристаллов. При более высокой температуре снижается вязкость раствора и, следовательно, облегчается диффузия. Однако в большей степени влияние температуры отражается на увеличении числа зародышей, что, как известно, приводит к образованию более мелких кристаллов. При положительной растворимости с повышением температуры кристаллизации уменьшается степень пересыщения раствора, что, в свою очередь, вызывает снижение движущей силы процесса.
61. Свойства кристаллов и влияние условий кристаллизации на свойства.
Основные факторы:
1. Форма кристаллов. Определяется природой кристаллизуемого вещества и зависит от наличия примесей в растворе. Более правильная форма получаются кристаллы при свободном их обтекании раствором. При большой скорости суспензии, ребра кристаллов стираются.
2. Размер кристаллов: более крупные кристаллы получаются при медленном их росте и наибольших степенях пресыщения раствора. Влияет перемешивание раствора, которое облегчает диффузионный перенос вещества к граням кристалла и способствует образованию зародышей. На размер сказывается наличие ПАВ (уменьшают или наоборот) Получают крупные кристаллы введением в раствор затравочных кристаллов и вывод мелких фракций.
3. Фракционный состав. Уменьшение количества мелких фракций за счет изменения Т и С раствора.
4. Степень чистоты продукта. Зависит от условий кристаллизации и от дальнейших операций (фильтрование и т.д.) Загрязнение из-за содержания примесей, попадают в кристалл с маточным раствором или адсорбируются его гранями.
62. Способы кристаллизации (изотермический, изогидрический, комбинированные)








