Оценивание неопределенности измерений коэффициента поправки титрованного раствора
Исходные данные:
- Объект измерений – раствор серной кислоты концентрации моль/дм3
- Измеряемая величина – коэффициента поправки 0,1 моль/дм3 раствора серной кислоты
- Единицы измерений – безразмерная величина
- Методика измерений – ГОСТ 25794.1 83 «Реактивы. Методы приготовления титрованных растворов для кислотно-основного титрования»
- Метод измерений – титриметрический по безводному углекислому натрию
Этап 1. Составление функции измерений
Значение оценки коэффициента поправки 0,1 моль/дм3 раствора серной кислоты Ki, при единичном определении рассчитывается по формуле:

где m – масса навески безводного углекислого натрия, г;
P – чистота реактива безводного углекислого натрия, P = 1;
M – молярная масса эквивалента безводного углекислого натрия, г/моль;
с – заданная молярная концентрация серной кислоты в 0,1 моль/дм3 растворе серной кислоты, с = 0,1 моль/дм3, рассматривается как постоянная и не учитывается при расчете неопределенности измерений коэффициента K;
V – объем 0,1 моль/дм3 раствора серной кислоты, израсходованный на титрование, см3.
1000 – коэффициент перехода единицы измерения объема см3 в дм3.
Значение оценки коэффициента K вычисляется как среднее арифметическое трех повторных определений коэффициента поправки раствора серной кислоты по формуле:

где F – поправочный коэффициент, учитывающий расхождение между результатами повторных определений коэффициента поправки раствора серной кислоты, F = 1.
Расхождение между результатами трех повторных определений коэффициента поправки раствора серной кислоты не должно превышать значения 0,001, установленного ГОСТ 25794.1 (п. 1.11).
Этап 2. Анализ входных величин
2.1 Масса навески безводного углекислого натрия, m
Значение массы навески безводного углекислого натрия, m, г, определяется как разность показаний весов при взвешивании стаканчика с навеской установочного вещества и пустого стаканчика. При выполнении измерения были получены следующие значения выходной величины для трех повторных определений коэффициента поправки: m1 = 0,1648 г; m2 = 0,1643 г; m3 = 0,1649 г.
Стандартная неопределенность измерений массы навески установочного вещества, u(m), г, оценивается на основании информации о пределах допускаемой погрешности используемых весов ВСЛ-200/0,1А ± Δm = ± 0,001 г в диапазоне измерений от 0,01 до 50 г, и дискретности отсчета весов d = 0,0001 г, установленных в технической документации на весы. В предположении прямоугольного распределения вероятностей значений погрешности и дискретности в границах ± Δm и ± d/2 соответственно и учитывая двойное взвешивание (пустого стаканчика и стаканчика с навеской установочного вещества) стандартная неопределенность u(m) рассчитывается по формуле:
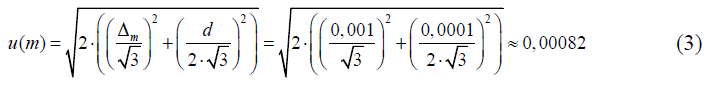
2.2 Чистота реактива безводного углекислого натрия, P
Значение оценки величины P принимается равным 1.
Стандартная неопределенность измерений степени чистоты реактива углекислого натрия u(P) оценивается на основании информации о том, что согласно ГОСТ 83-79 «Реактивы. Натрий углекислый. Технические условия» массовая доля углекислого натрия в реактиве безводного углекислого натрия составляет не менее 99,8 %. Неопределенность измерений u(P) рассчитывается исходя из отклонения значения чистоты реактива от 1 в предположении прямоугольного распределения величины Р в границах ± (1 – 0,998) по формуле:

2.3 Молярная масса эквивалента безводного углекислого натрия, M
Значение оценки величины M, г/моль, определяется как произведение фактора эквивалентности безводного углекислого натрия fэ = 1/2 на молярную массу установочного вещества M0, г/моль, по формуле:
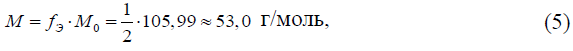
где молярная масса безводного углекислого натрия (Na2CO3) рассчитывается на основании значений атомных масс натрия, углерода и кислорода A, взятых из таблиц атомных масс IUPAC (//www.sbcs.qmul.ac.uk/iupac/AtWt/), и количества атомов этих элементов в молекуле безводного углекислого натрия n (ANa ≈ 22,98976928, Aс = 12,011, A0 = 15,999, nNa= 2, nс = 1, n0 = 3):
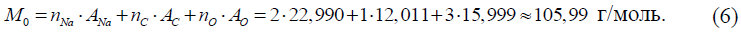
Стандартная неопределенность измерений молярной массы эквивалента безводного углекислого натрия, u(M), г/моль, определяется на основании возможных разбросов значений атомных масс углерода и кислорода ΔА = Amax – Amin и неопределенности последней цифры атомной массы натрия ΔA, а также количества атомов этих элементов в молекуле безводного углекислого натрия n. Данные по разбросам значений атомных масс углерода и кислорода и неопределенности последней цифры атомной массы натрия выбираются из таблиц атомных масс IUPAC (//www.sbcs.qmul.ac.uk/iupac/AtWt/). Стандартная неопределенность значений атомных масс химических элементов рассчитывается в предположении прямоугольного распределения вероятностей атомных масс элементов в границах ± ΔА/2 (для углерода и кислорода) и в границах ± ΔA (для натрия). Неопределенность для вклада атомов одного элемента рассчитывается умножением стандартной неопределенности атомной массы элемента на количество атомов элемента. Стандартная неопределенность измерений молярной массы эквивалента безводного углекислого натрия, u(M), г/моль, определяется по формуле:
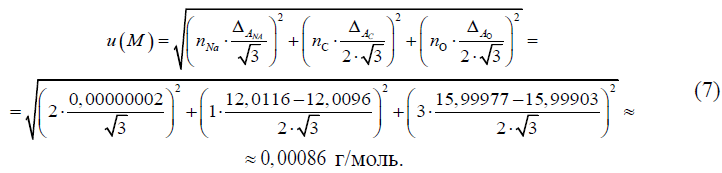
2.4 Объем раствора серной кислоты, израсходованный на титрование, V
Значение оценки величины V, см3, определяется по шкале бюретки номинальной вместимостью 25 см3 2-го класса точности по ГОСТ 29251-91 «Посуда лабораторная стеклянная. Бюретки. Часть 1. Общие требования». При выполнении измерения были получены следующие значения выходной величины для трех повторных определений коэффициента поправки: V1= 31,1 см3; V2= 31,0 см3; V3= 31,1 см3.
Стандартная неопределенность измерений объема 0,1 моль/дм3 раствора серной кислоты, израсходованного на титрование, u(V), см3, состоит из следующих основных вкладов:
- стандартная неопределенность, обусловленная погрешностью измерения объема сливаемой жидкости используемой бюретки, u(VΔ), см3;
- стандартная неопределенность, обусловленная ценой наименьшего деления шкалы используемой бюретки, u(Vc), см3;
- стандартная неопределенность, обусловленная отличием температуры, при которой проводятся измерения, от температуры, при которой нормируется погрешность измерения объема сливаемой жидкости бюретки, u(Vt), см3.
Стандартная неопределенность u(VΔ), см3, рассчитывается на основании информации о пределах погрешности измерения сливаемой жидкости бюреткой ± ΔV = 0,1 см3, установленных ГОСТ 29251 в предположении треугольного распределения погрешности в установленных пределах по формуле:
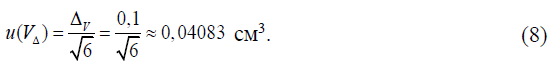
Стандартная неопределенность u(Vc), см3, рассчитывается на основании информации о цене наименьшего деления шкалы используемой бюретки см3, в предположении прямоугольного распределения вероятностей цены деления в пределах ± dV/2 по формуле:
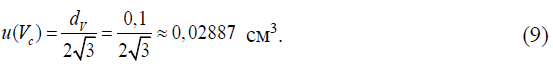
Стандартная неопределенность u(Vt), см3, рассчитывается в предположении прямоугольного распределения исходя из возможных пределов изменения объема жидкости при условии колебания температуры в лаборатории при измерении в пределах (20 ± 5) °С (Δt = 5 °С) и коэффициента объемного расширения жидкости kV, ºС-1, равного 0,00021 ºС-1 для воды (основное вещество в растворе) по формуле:
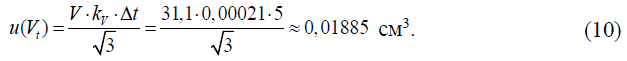
Примечание – Для оценивания стандартной неопределенности u(Vt) используется измеренное значение объема раствора серной кислоты, пошедшего на титрование, полученное для первой навески безводного углекислого натрия.
Суммарная стандартная неопределенность измерений объема 0,1 моль/дм3 раствора серной кислоты, израсходованного на титрование, u(V), см3 вычисляется путем суммирования стандартных неопределенностей перечисленных выше вкладов по формуле:
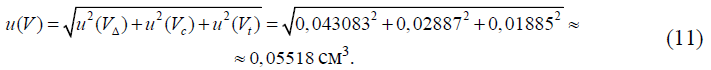
2.5 Поправочный коэффициент, учитывающий расхождение между результатами повторных определений коэффициента поправки раствора серной кислоты, F
Значение оценки величины F принимается равным 1.
Стандартная неопределенность измерений поправочного коэффициента, учитывающего расхождение между результатами повторных определений коэффициента поправки раствора серной кислоты, u(F), определяется на основании установленного ГОСТ 25794.1 (п. 1.11) допускаемого расхождения между результатами повторных определений коэффициента поправки r = 0,001, которое рассматривается как предел повторяемости согласно СТБ ИСО 5725-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике». С учетом того, что за результат измерения принимается среднее арифметическое трех определений, стандартная неопределенность u(F) определяется по формуле:
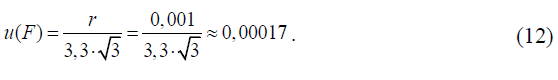
Этап 3. Анализ корреляций
Все входные величины рассматриваются как некоррелированные, поскольку получены независимо друг от друга в различных экспериментах.
Этап 4. Оценка измеряемой величины
Значения коэффициента поправки раствора серной кислоты при i-ом определении согласно формуле (1) составляют:

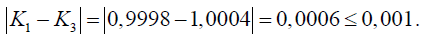
Максимальное расхождение между результатами трех определений не превышает допускаемого значения, установленного ГОСТ 25794.1:
Значение коэффициента поправки раствора серной кислоты определяется по формуле (2) на основании результатов параллельных определений, которые рассчитываются по формуле (1):
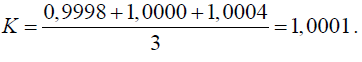
Коэффициент поправки вычисляют с точностью до четвертого десятичного знака. Полученное значение коэффициента поправки раствора серной кислоты удовлетворяет требованию ГОСТ 25794.1 (п. 1.11) о том, что значение коэффициента поправки должно соответствовать диапазону .








