Работа № 6. Определение константы диссоциации слабой кислоты и константы гидролиза соли
Цель работы – определение физико-химических констант электролитов: константы диссоциации уксусной кислоты и константы гидролиза уксуснокислого натрия.
Оборудование
1. рН-метр (рН-340) с датчиком.
2. Четыре стеклянные колбочки.
3. Мерные цилиндры.
Последовательность выполнения работы
Опыт 1.
1. Приготовить в четырех колбах по 30 мл раствора уксусной кислоты СН3СООН разной концентрации (см. табл.), разбавляя дистиллированной водой исходный раствор – О,1 н СН3СООН.
2. Измерить рH растворов на рН-метре (описание прилагается к прибору).
3. Полученные результаты оформить в таблицу.
| Концентрация СН3СООН С, г-экв/л) | 0,1 н | 0,05 н | 0,025 н | 0,0125 н |
| pH | ||||
| lgC | ||||
| pK |
5. Построить график зависимости рН от логарифма концентрации, отложив по оси абсцисс логарифм концентрации кислоты, а по оси ординат − значения рН. Провести экстраполяцию (продление) полученной прямой на ось ординат. Отрезок, отсекаемый прямой на оси ординат,
соответствует значению 1/2 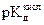 .
.
6. Рассчитать 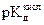 по уравнению
по уравнению
рН = 1/2 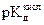 - 1/2 lgС
- 1/2 lgС
для всех концентраций, найти ее среднее значение и сравнить со значением 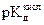 , полученным графически. Определить
, полученным графически. Определить 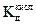 .
.
Опыт 2
1. Для определения константы гидролиза ацетата натрия СН3СООNa приготовить по 30 мл растворов соли разной концентрации (согласно табл. 6.2), разбавляя дистиллированной водой исходный раствор 0,1 н СН3СООNa.
2. Измерить рН растворов на рН-метре.
3. Полученные результаты записать в таблицу
| Концентрация CH3COONa С, г-экв/л | 0,1 н | 0,05 н | 0,025 н | 0,0125 н |
| pH | ||||
| lgC |
4. По данным таблицы построить график, отложив по оси ординат рН, а по оси абсцисс lgC. проведя экстраполяцию полученной прямой на ось ординат. Отрезок, отсекаемый прямой на оси ординат, соответствует значению 14 – 1/2 lgКГ.
5. Определить Кг и сравнить значение Кг с рассчитанной по формуле
Кг = К Н2О/ 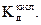 Величину
Величину 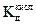 взять из предыдущего опыта,
взять из предыдущего опыта,
а К Н2О = 10-14.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ
1. Дайте определение константы диссоциации электролита. В чем заключается ее физический смысл? Обоснуйте влияние различных факторов на величину константы диссоциации.
2. Пользуясь законом разведения, рассчитайте степень диссоциации 0,01 М раствора HF , если константа диссоциации 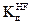 = 10-2.
= 10-2.
3. Дайте определение рН раствора и рассчитайте, чему равен рН 0,001 н раствора КОН (α = 1).
4. Какие химические процессы подразумевают, применяя термин «гидролиз солей»? Какие соли дают при гидролизе кислую, а какие щелочную среду?
5. Напишите в ионной и молекулярной форме уравнения реакций гидролиза раствора соли Na2CO3.








