Разработка технических средств
измерения концентрации хлора в воде
Отчет по практическим работам к дисциплине
«Нестандартные средства измерений»
| ПР 200100.000 О |
обозначение документа
Студент группы ИИТ–92 А.А. Назьмов
и.о. фамилия
Руководитель доцент, к.т.н. А.А. Чепуштанов
должность, ученая степень и.о. фамилия
Барнаул 2012
Содержание
1 Теоретическая часть. 3
2 Разработка технического задания. 6
3 Функциональная структура средства измерения. 7
Проектирование – это процесс создания описания, необходимого для создания еще не существующего объекта, на основе первичного описания этого объекта и алгоритма его функционирования. Проектирование включает в себя комплекс работ по изысканию, исследованию, расчетам и конструированию, имеющих цель получения описания для создания нового изделия.
Проектирование технического объекта связано с созданием, преобразованием и представлением в принятой форме образа этого объекта. Проектирование начинается при наличии задания на проектирование, являющимся исходным описанием объекта. Результатом проектирования служит комплект документации, содержащей достаточные сведения для изготовления объекта.
Разработка технических средств измерений представляет собой процесс создания новых образцов устройств, приборов и аппаратов, удовлетворяющих заданным требованиям. Этот процесс связан с решением схемотехнических, конструкторских и технологических задач.
1 Теоретическая часть
Контроль за концентрацией хлора и его производных имеет важное значение для управления процессом обеззараживания питьевых и сточных вод.
Хлор является одним из биогенных элементов и неотъемлемых компонентов тканей растений и животных, несмотря на то, что содержание его в живых организмах предельно мало. Потребность человека в хлоре покрывается за счет продуктов питания, в основном в виде хлорида натрия и хлорида калия. В организме хлор является осмотически активным веществом плазмы лимфы, крови, спинномозговой жидкости, а также принимает непосредственное участие в водно-солевом обмене и способствует удержанию воды в тканях. Однако избыток хлора весьма опасен для здоровья. Максимальная концентрация хлора в воздухе производств, помещений не должна превышать 1 мг/м3. Производство любых хлоросодержащих соединений относится к производствам с вредными условиями труда.
В растительном мире значение хлора не менее велико – хлор позитивно воздействует на поглощения корнями кислорода и необходим для его образования в процессе фотосинтеза. В малых дозах хлор способствует развитию растений. Разработаны специальные механизмы и приборы для измерения контроля концентрации хлора в растворах, в частности, и воде.
Концентрация – величина, характеризующая количественный состав раствора.
Таблица 1 – Зависимость плотности растворов H2SO4 от её массовой доли в водном растворе при 20° C
| ω, % | 5 | 10 | 15 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 95 |
| ρ H2SO4, г/мл | 1,032 | 1,066 | 1,102 | 1,139 | 1,219 | 1,303 | 1,395 | 1,498 | 1,611 | 1,727 | 1,814 | 1,834 |
Объёмная доля – отношение объёма растворённого вещества к объёму раствора. Объёмная доля измеряется в долях единицы или в процентах.
Объёмная доля ν  , определяется по формуле:
, определяется по формуле:
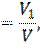
где V1 – объём растворённого вещества, л;
V – общий объём раствора, л.
Кондуктометр – прибор для измерения электропроводности электролитов (водных и неводных растворов, коллоидных систем, расплавов, твёрдых веществ). Кондуктометрический анализ основан на изменении концентрации вещества или химического состава среды в межэлектродном пространстве
Кондуктометры являются необходимым оборудованием для предприятий государственного экологического контроля, которые осуществляют наблюдение за состоянием вод и окружающей среды.
Помимо этого, кондуктометры различных модификаций используются в промышленности.
Кондуктометры используются в промышленности для измерения концентрации:
– хлора в воде;
– нефтепродуктов, жиров и НПАВ (неионогенные поверхностно–активные вещества) в воде;
– нефтепродуктов, жиров и НПАВ в природных объектах;
– нефти в кернах и шламе;
– мышьяка;
– азота и углерода.
Различают контактную и бесконтактную кондуктометрия в зависимости от наличия или отсутствия контакта между электролитом и входными цепями измерительного прибора. Наиболее распространены контактный низкочастотный и бесконтактный высокочастотный методы.
Контактные методы.
Измерения проводят с помощью контактных ячеек. При этом используют электроды из Pt, Ti, нержавеющей стали и др. Для измерения растворов с высокой концентрацией электролита (10–2-10–3 М) применяют платинированные электроды с развитой поверхностью.
В прямой кондуктометри непосредственно определяют концентрацию электролита по электропроводности его раствора (если между этими величинами имеется линейная зависимость). Метод применяется главным образом для анализа разбавленных растворов. В случае концентрирированных растворов необходимо строить градуировочные графики. Определение веществ в присутствии других электролитов возможно, если концентрации последних постоянны. На методе прямой кондуктометрия основаны конструкции солемеров и др. кондуктометрических устройств, позволяющих определять олеум, а также различных соли в минеральной, речной и морской водах, физиологических жидкостях и др.
Контактные методы отличаются высокой точностью. Они применяются не только для химанализа, но и для изучения кинетики реакций, определения констант диссоциации (ассоциации) электролитов, растворимости осадков, коэффициентов диффузии и т.д.
2 Разработка технического задания
Название прибора: кондуктометр
Основные технические характеристики
Таблица - 1 Основные технические характеристики
| Диапазон измерения | |
| погрешность | |
| питание | |
| время измерения |
Таблица - 2 Конструктивные требования.
| Вес | » 1 кг |
| Габариты | Датчик: 0,02х0,02х0,01 м Прибор 0,15х0,1х0,03 м |
| Тип | Переносной |
Условия эксплуатации:
Температура: 0° - 70°
Гарантий срок службы: 3 года
Поверка и градуировка прибора производится при изготовлении.
Ориентировочная стоимость при массовом производстве 4000 – 7000 руб.
3 Функциональная структура средства измерения
Для измерения концентрация хлора в воде был выбран кондуктометрический контактный метод.
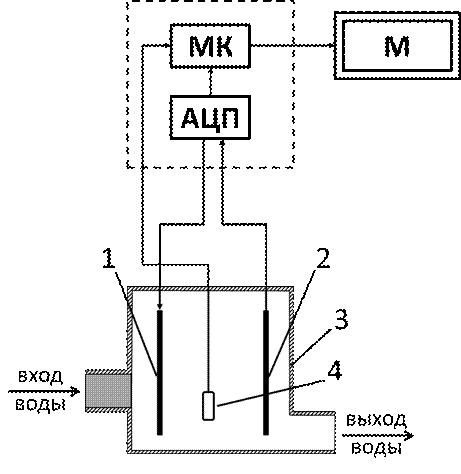
Кондуктометрический метод анализа основан на измерении электропроводности растворов электролитов, в которых перенос тока происходит за счет движения ионов. Электропроводность характеризует суммарную концентрацию ионов в растворе. Зависимость электропроводности от концентрации носит сложный характер: с увеличением концентрации электропроводность раствора сначала увеличивается, а затем уменьшается. Поэтому для каждого кондуктометрического концентратомера установлены свои пределы измерений в единицах электропроводности (См/см) или концентрации (г/л). Эти параметры вычисляются опытным путем после сбора тестового образца прибора. В состав прибора входит базовая (вычислительная) часть, монитор и электродный датчик. Рассмотрим схему строения прибора (рисунок 1).
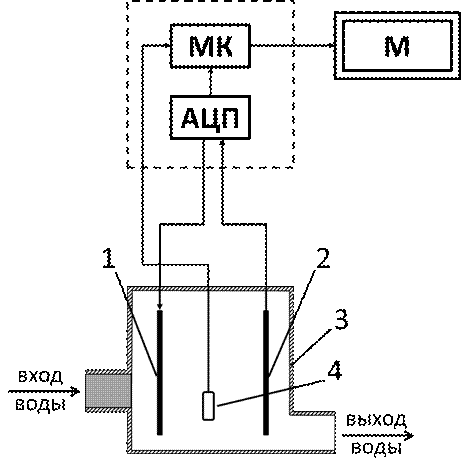
Условные обозначения:
АЦП – аналогово–цифровой преобразователь;
МК – микроконтроллер;
М – монитор;
1– катод (графитовый стержень);
2–анод (графитовый стержень);
3– корпус электродной ячейки датчика;
4 – термометр.
Рисунок 1 - Функциональная схема прибора
Описание составляющих частей схемы:
АЦП – Аналого-цифровой преобразователь преобразовывает аналоговые значения, с электродов в цифровые и передает их для дальнейшей обработки в МК.
МК – Микроконтроллер, схема в задачи, которой входит сравнение полученных данных (вычитание из первоначального напряжения полученного) и совершение поправок по определенной схеме.
М – Монитор, предназначен для вывода конечной информации.
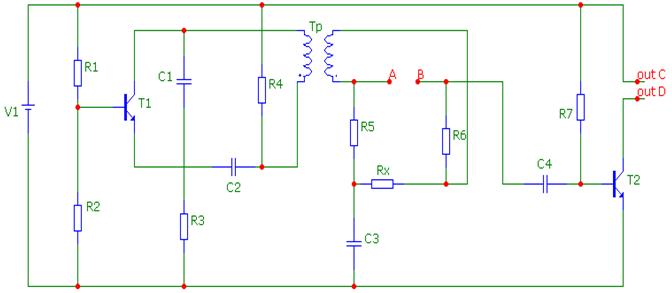
Электродный датчик концентратомера (рисунок 1) представляет собой двухэлектродную ячейку, через которую непрерывно протекает анализируемый раствор. Для характеристики воды необходимо знать удельную электропроводность λ, которая относится к единице длины проводника (в нашем случае – к 1 см слоя воды). Значение λ измеряется в мкСм/см. Через внешние электроды пропускается переменный (а не постоянный во избежание электролиза и поляризации) ток частотой 100 Гц. Изменение напряжения между электродами (анодом и катодом) будет зависеть от электропроводности анализируемого раствора, т.е. от его концентрации. Зависимость электропроводимости воды от содержания растворенного NaCl при 20° С рассчитывается данным методом:
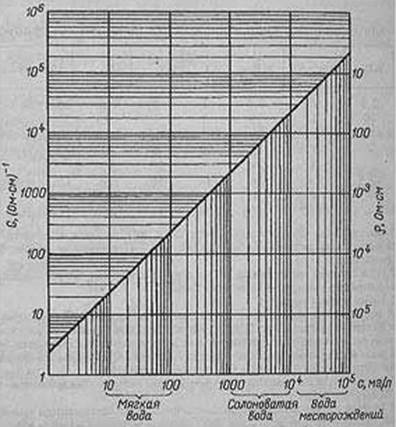
Рисунок 1 – Зависимость проводимости воды от содержания растворенного NaCl при 20° С
Согласно графику зависимости проводимости воды от содержания растворенного NaCl (рисунок 2), каждый 1 мг/л NaCl обеспечивает удельную электропроводность раствора, приблизительно равную 2,3 мкОм/cм.
Следовательно концентрацию хлора в воде при 20°С можно определить по формуле:
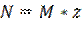
| (1) |
Напряжение, подаваемое на первый электрод и получаемое на втором электроде, измеряется при помощи АЦП, оба значения передаются на микроконтроллер (МК) для вычисления разницы между ними.
Микроконтроллер, зная изменение напряжения, вычисляет концентрацию раствора при 20°С и принимает поправку согласно таблице температур (таблица 1):
Таблица 3 - Коэффициент температуры по отношению к 20о С
| Температура воды в оС | Коэффициент температуры по отношению к 20о С | Температура воды в оС | Коэффициент температуры по отношению к 20о С |
| 15 | 1,132 | 23 | 0,937 |
| 16 | 1,095 | 24 | 0,919 |
| 17 | 1,071 | 25 | 0,901 |
| 18 | 1,046 | 26 | 0,840 |
| 19 | 1,023 | 27 | 0,810 |
| 20 | 1,000 | 28 | 0,790 |
| 21 | 0,979 | 29 | 0,770 |
| 22 | 0,958 | 30 | 0,750 |
Результат выводится на монитор.

.
 |

1 – катод (графитовый стержень);
2 –анод (графитовый стержень);
3 – корпус электродной ячейки датчика;
4 – термометр.










