Определение средней длины свободного пробега и эффективного диаметра молекул воздуха
Лабораторная работа 1.10
Определение средней длины свободного пробега и эффективного диаметра молекул воздуха
Молекулы газа движутся хаотически, сталкиваются друг с другом и со стенками сосуда.
|
|
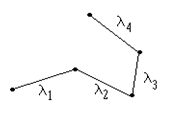
Расстояние, проходимое молекулой между двумя последовательными соударениями, называется длиной свободного пробега l .
На длине свободного пробега молекула движется равномерно и прямолинейно.
Среднее расстояние, проходимое молекулой между двумя последовательными соударениями, называется средней длиной свободного пробега < l >
Оно равно
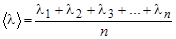 .
.
Чтобы найти среднюю длину свободного пробега, нужно расстояние, пройденное молекулой за единицу времени (т.е. среднюю скорость молекулы <V>), разделить на число столкновений Z за единицу времени:
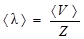 . (1)
. (1)
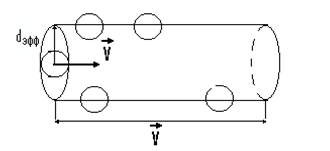
Найдем Z , считая, что все молекулы, кроме одной, покоятся, а единственная молекула движется по оси цилиндра. За единицу времени она столкнется со всеми молекулами, находящимися внутри цилиндра радиусом r , равным эффективному диаметру dэфф молекулы газа и длиной, равной скорости молекулы.
|
|
Поэтому число столкновений в единицу времени определится числом молекул, которые окажутся внутри этого цилиндра. Число столкновений в единицу времени Z равно произведению концентрации n на объем цилиндра:
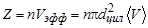 ,
,
где <V> - средняя скорость молекулы. По построению она равна длине цилиндра. Если считать, что остальные молекулы тоже двигаются, то в расчеты достаточно добавить поправочный коэффициент 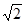 . Тогда окончательно получим:
. Тогда окончательно получим:
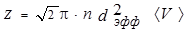 , (2)
, (2)
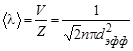 . (3)
. (3)
У воздуха при нормальных условиях (t=0 0С или T=273 К, давление Р=105 Па, что соответствует нормальному давлению 760 мм рт. ст.), средняя скорость - 447 м/с, число молекул в единице объема - 1025 в 1 м3 , средняя длина свободного пробега - 60 ×10-9 м, число столкновений в 1 секунду 1,8 ×108 раз, эффективный диаметр молекулы составляет 3×10-10 м .
Средняя длина свободного пробега обратно пропорциональна давлению газа (см формулу 3), давление газа пропорционально концентрации n молекул газа (p = nkT), и если <l>, согласно (3), обратно пропорциональна концентрации n, то, следовательно, и обратнопропорциональна p.
2. Рассмотрим теперь понятие эффективного диаметра молекулы.
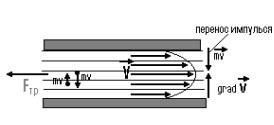
Между молекулами любого вещества одновременно действуют силы взаимного притяжения и отталкивания. Они называются силами молекулярного взаимодействия и имеют электрическое происхождение, поскольку ядра и электроны соседних молекул испытывают электрические силы отталкивания и притяжения. Именно силы межмолекулярного взаимодействия определяют характер теплового движения молекул твердых, жидких и газообразных тел.
|
|
В газах силы притяжения между молекулами не могут преодолеть силы отталкивания, и молекулы разлетаются во все стороны, занимая весь объем сосуда, в котором находится газ. Газы не имеют определенного объема и формы и легко сжимаются под действием внешнего давления. При столкновениях молекулы приближаются друг к другу на расстояние r =10-10 м между их центрами. На этом расстоянии силы отталкивания резко возрастают за счет перекрытия их электронных оболочек (сила отталкивания носит квантовый характер и поэтому растет значительно быстрее электрической силы притяжения). Действие сил отталкивания приводит к такому же результату, как и столкновение молекул - молекулы отталкиваются друг от друга.