7. Поверхностные явления и адсорбция
1. Адсорбция
Процесс самопроизвольного концентрирования газов или растворенных веществ на поверхности раздела фаз называют адсорбцией. В зависимости от природы контактирующих фаз различают адсорбцию на границах: газ - твердое тело, газ – жидкость, жидкость - твердое тело и жидкость - жидкость.
Еще в 1785 г русский ученый Т.Е. Ловиц открыл способность угля поглощать растворенное вещество. С тех пор изучению явлений адсорбции было посвящено много работ, среди которых первостепенное значение имеют работы русских ученых: академика Н.Д. Зелинского, предложившего уголь в качестве универсального средства защиты от газообразных отравляющих веществ; М.С. Цвета, разработавшего хроматографический метод разделения веществ по их адсорбционной способности; академика К.К. Гедройца, создавшего учение о поглотительной способности почв; академика М.М. Думанского, разработавшего методику получения активных адсорбентов. Очень много для разработки теории и практики адсорбции сделали зарубежные ученые Гиббс, Ленгмюр, Фрейндлих, Поляни, Бранауэр и др.
Адсорбция является следствием снижения ненасыщенности молекулярных, атомных или ионных сил на поверхности раздела фаз и обусловлена накоплением вещества, снижающего свободную поверхностную энергию. Адсорбция – процесс самопроизвольный, т.к. в результате процесса адсорбции происходит уменьшение свободной поверхностной энергии, а по второму закону термодинамики такие процессы являются самопроизвольными.
Вещества, которые адсорбируются, называют адсорбатами (иногда - адсорбтивами), а вещества, которые адсорбируют на своей поверхности - адсорбентами.
В зависимости от характера сил, действующих между частицами (молекулы, атомы, ионы) адсорбата и адсорбента, различают физическую или ван-дер-ваальсову адсорбцию и химическую или хемосорбцию.
Природу адсорбции можно установить, исследовав её кинетику и энергетику. Действительно, физическая адсорбция происходит под влиянием относительно слабых межмолекулярных сил сцепления (сил Ван-дер-Ваальса) и по своей природе аналогична процессам конденсации паров адсорбата, теплота её близка к теплотам конденсации и составляет 10 - 50 кДж/моль. Поэтому при увеличении температуры физическая адсорбция уменьшается.
Хемосорбция связана с перекрыванием электронных орбиталей частиц адсорбата и адсорбента, т.е. вызывается их химическим взаимодействием, не приводящим, однако, к образованию объемной фазы. Теплота хемосорбции соизмерима с теплотами химических реакций и составляет обычно 60 - 600 кДж/моль. Химическая адсорбция с увеличением температуры увеличивается.
Адсорбция представляет собой обратимый процесс. Процесс, обратный адсорбции, называется десорбцией.
Различают молекулярную и ионную хемосорбцию в зависимости от того, что адсорбируется – молекулы или ионы вещества. В свою очередь, ионная адсорбция делится на обменную и адсорбцию потенциалопределяющих ионов.
Обменная адсорбция. Обменная адсорбция протекает на границе твердое тело / раствор электролита и состоит в том, что адсорбент и раствор обмениваются между собой катионами или анионами в эквивалентных количествах, благодаря чему принцип электронейтральности раствора электролита и адсорбента остается ненарушенным.
Основными факторами обменной адсорбции, определяющими ее специфичность, являются: наличие двойного электрического слоя на поверхности твердого адсорбента, валентность, величина радиуса и степень гидратации ионов раствора электролита.
Обменная адсорбция протекает несколько медленнее, чем обычная.
Для уяснения процесса обменной адсорбции можно рассмотреть процесс образования двойного электрического слоя при взаимодействии частицы хлористого серебра с раствором хлорида калия. Ионы хлора, сталкиваясь с частицами [AgCl]n будут соединяться с ионами серебра, образуя прочно удерживаемый слой С1- ионов, тем самым заряжая поверхность частицы. Такие ионы получили название потенциалопределяющих, а т.к. присоединившиеся С1- -ионы увеличивают свою концентрацию, т.е. адсорбируются на поверхности, то такой вид адсорбции называется адсорбцией потенциалопределяющих ионов.
Адсорбированные С1--ионы заряжают частицу отрицательно, и под действием электростатических сил притяжения будет увеличиваться количество К+-ионов, прилегающих к поверхности частицы. Другими словами, будет происходить адсорбция противоионов под действием электростатических сил. Так как К+-ионы могут быть заменены другими ионами такого же знака, взаимодействующими с частицей лишь электростатически, такие ионы называются обменными, адсорбция их - обменной.
Таким образом, обменная адсорбция происходит в процессе обмена ионов двойного электрического слоя адсорбента и ионов раствора. Схематически это можно представить следующими уравнениями:
Адсорбент-½Н+ + Na+ + Cl- à Адсорбент-½Na+ + H + +Cl-
Адсорбент+ ½OH- + Na+ + Cl- à Адсорбент+½Cl- + Na+ + OH -
Из приведенной схемы видно, что в ходе адсорбции ионов может изменяться рН среды (в раствор переходят H+ или OH- ионы), раствор приобретает кислую или щелочную реакцию, такой вид адсорбции называется гидролитический.
Так как обменная адсорбция является химической, то обмен ионов происходит в строго эквивалентных соотношениях.
Обменные ионы на твердой поверхности обладают определенной величиной и знаком заряда, поэтому, чтобы не нарушался двойной электрический слой (ДЭС), обменными ионами из раствора, могут быть только ионы одного и того же знака. При этом не должна изменяться и величина заряда поверхности. Таким образом, обменная адсорбция может быть только анионообменной или катионообменной.
Явления обменной адсорбции играют важную роль в процессах, происходящих в почвах. Обменным комплексом почв является почвенный поглощающий комплекс (ППК), состоящий из коллоидных частиц, заряженных отрицательно. Обменными ионами почвы являются катионы. Важнейшие свойства почвы: водопроницаемость, влагоемкость, набухаемость, структура, рН почвенного раствора и др. – определяются составом адсорбированных ионов. Например, почвы, содержащие в составе обменных катионов значительное количество ионов натрия, приобретают особые, так называемые, “солонцовые свойства”. Они отличаются высокой дисперсностью, плотным сложением, высокой щелочностью, повышенной набухаемостью и вязкостью, малой водопроницаемостью. Эти почвы трудно обрабатываются и, несмотря на большой запас питательных веществ, мало плодородны. Если же в состав обменных катионов почвы входят преимущественно ионы кальция, то такие почвы обладают хорошей структурой, малой распыленностью, хорошей водо- и воздухопроницаемостью. Эти почвы относятся к наиболее плодородным. Примером почв с большим содержанием обменного кальция и прекрасными физико-химическими свойствами являются черноземные почвы.
Ионообменные процессы в почвах можно представить следующей схемой:
[ППК]-2Na+ + Са2+ + SO42- = [ППК]- Cа2+ + Na2SO4
Б.П. Никольский и Е.Н. Гапон предложили уравнение, описывающее обменную адсорбцию:
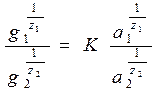
Здесь g1 и g2 – количество г-моль (г-экв) адсорбированных и десорбированных ионов единицей массы адсорбента, а1 и а2 – активности обменивающихся ионов в растворе при равновесии; z1 и z2 – заряд ионов, К – константа данного адсорбционного процесса.
Явление адсорбции находит широкое применение в промышленности и сельском хозяйстве. Так, на активированном угле производят адсорбционную очистку (рафинирование) сиропа сахарозы. Именно силы адсорбции удерживают ионы минеральных удобрений (К+, РО4-3 и т.п.) и молекулы (мочевины) в почве. Адсорбция мочевины физическая, молекулы её слабо удерживаются почвой. Поэтому мочевину, чтобы её не вынесло весенним паводком, вносят обычно весной. Калийные удобрения можно вносить в почву и осенью, так как адсорбция ионов К+ вызывается химическими силами (ионные связи) и она прочная.
В общем случае адсорбция является функцией давления Р (для газов) или концентрации С (для жидких растворов) и температуры, т.е. изображается плоскостью в координатах Г = f(C,T). Обычно один из параметров поддерживают постоянным и адсорбцию графически изображают в виде кривых.








