Химические свойства белков. Качественные реакции белков.
· Денатурация
· Гидролиз
· Биуретовая реакция
· Ксантопротеиновая реакция
· Качественное определение серы в белках
Как мы уже убедились, возможно существование огромного множества различных белков. В зависимости от строения аминокислотных остатков и их последовательности в полипептидной цепи свойства белков могут существенно различаться. Например, белок куриного яйца альбумин растворяется в воде, в то же время белки кератины, входящие в состав волос и ногтей, нерастворимы в воде.
Рассмотрим химические свойства белков.
- Денатурация
При нагревании, под действием сильных кислот или оснований, солей тяжелых металлов и некоторых других реагентов происходит необратимое осаждение (свертывание) белков, называемое денатурацией.
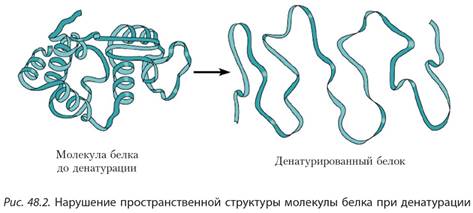
Легкость денатурации многих белков очень затрудняет их изучение.
!!! При денатурации происходят изменения во вторичной и третичной структурах белка, а первичная структура сохраняется. При этом их биологические функции полностью теряются.
Денатурация имеет не только отрицательные стороны. Вспомните хотя бы сваренные вкрутую яйца (свертывание белка). Похожим образом сворачивается белок молока — казеин (так получают творог, богатый белком пищевой продукт).
Большинство белков свертывается при температуре до 100о. Именно поэтому все живое гибнет в огне, практически все — при кипячении в воде. В привычной для нас форме невозможна жизнь на «горячих» планетах Солнечной системы — Меркурии и Венере.
- Гидролиз
Под действием ферментов, а также водных растворов кислот или щелочей происходит разрушение первичной структуры белка в результате его гидролиза по пептидным связям. Гидролиз приводит к образованию более простых белков и аминокислот.
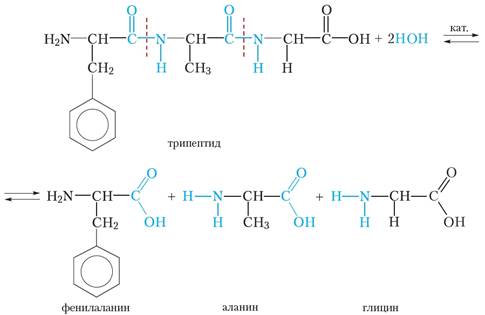
Одно из важнейших химических свойств белков — реакции гидролиза. В присутствии природных катализаторов (ферментов) или сильных кислот молекулы воды расщепляют полимерную белковую молекулу до аминокислот: 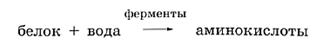
Именно такой процесс протекает при переваривании белковой пищи.
Гидролиз — основа процесса пищеварения.
В организм человека ежедневно должно поступать с пищей 60—80 г белка. В желудке под действием ферментов (из группы пептидаз) и соляной кислоты белковые молекулы распадаются на «кирпичики»-аминокислоты. Попадая в кровь, они разносятся по всем клеткам организма, где участвуют в строительстве собственных белковых молекул, свойственных только данному виду.
Белки играют ключевую роль почти во всех структурах живых организмов и происходящих в них процессах.
Белки дают две качественные (цветные) реакции.
1. Биуретовая реакция.
При действии на белки свежеполученного осадка гидроксида меди (II) в щелочной среде возникает фиолетовое окрашивание (рис. 1).
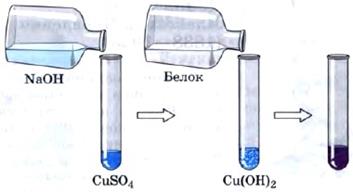
Рис. 1.
Биуретовая реакция
2. Ксантопротеиновая реакция.
При действии на белки концентрированной азотной кислотой образуется белый осадок, который при нагревании желтеет, а при добавлении водного раствора аммиака становится оранжевым (рис. 2).
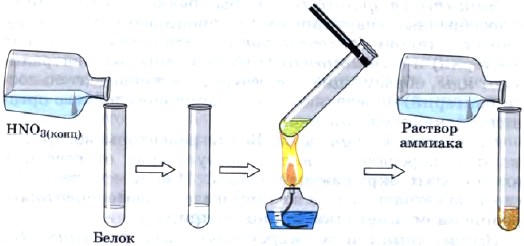
Рис. 2.
Ксантопротеиновая реакция
Качественное определение серы в белках.
При горении белков ощущается характерный запах «жженого рога или перьев». В этом легко убедиться, если поджечь шерстяную нитку или пучок волос. В значительной степени этот запах определяется содержанием в белках серы.
ДЗ:
1. Напишите уравнение реакции гидролиза вещества, формула которого:
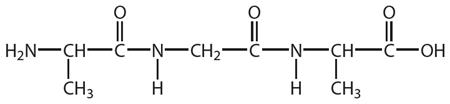
2. Все ли белки будут гореть с характерным запахом «жженого рога или перьев»? Почему и Какие?








