Реакции обнаружения хромат - иона СrO 42-
1.  Нитрат свинца (II) Pb(NO 3 ) 2 образует с хромат - ионами осадок желтого цвета:
Нитрат свинца (II) Pb(NO 3 ) 2 образует с хромат - ионами осадок желтого цвета:
Pb(NO3)2 + К2СrO4 → PbCrO4↓ + 2KNO3
Pb2+ + CrO42- → PbCrO4↓
Осадок растворяется в азотной кислоте и щелочах:
PbCrO4↓ + 2HNO3 → Pb(NO3)2 + H2CrO4
мешающие ионы: Ba2+, Hg2+, Bi3+, Ag+ и др.
2. 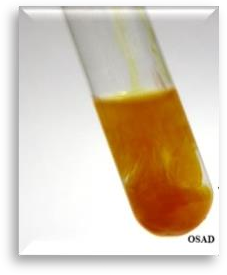 Нитрат серебра AgNO 3 при взаимодействии с хроматами щелочных металлов образует кирпично-красный осадок хромата серебра Ag2CrO4:
Нитрат серебра AgNO 3 при взаимодействии с хроматами щелочных металлов образует кирпично-красный осадок хромата серебра Ag2CrO4:
2AgNO3 + K2CrO4 → Ag2CrO4↓ + 2KNO3
2Ag+ + CrO42- → Ag2CrO4↓
Осадок растворим в азотной кислоте и растворе аммиака, но не растворяется в уксусной кислоте:
Ag2CrO4↓ + 2HNO3 → 2AgNO3 + H2CrO4 Ag2CrO4↓ + 4NH4OH → [Ag(NH3)2]2CrO4 + 4H2O
мешающие ионы: Ba2+, Hg2+, Bi3+ и др.
3. Пероксид водорода в кислой среде окисляет дихромат – ионы Cr2O72- до надхромовой кислоты синего цвета:

| 7 2 2 2 6 2 |
К2Сr2O7 + 4Н2O2 + H2SO4 → 2H2CrO6 + K2SO4 + 3Н2O Cr2O 2- + 4Н O + 2Н+ → 2Н СrO + 3Н O
4. Реакция с кислотами: в кислой среде образуется дихромат – ион Cr2O72-, раствор из желтого становится оранжевым:
2К2СrO4 + 2НCl → К2Сr2O7 + 2KCl + Н2O
Тест для закрепления материала
1. Какие из перечисленных анионов относятся к I аналитической группе:
1) PO3−; SO2−; CO2−
 4 3 3
4 3 3
2) CrO2−; Cl−; NO−
4 2
3) Cl−; Br− ; S2−
4) NO−; NO−; SO2−
2 3 4
2. Какой раствор является групповым реагентом анионов I аналитической группы:
1) NaOH
2) H2SO4
3) BaCl2
4) HCl
3. Цвет осадка, образующегося в результате реакции:
BaCl2 + Na2SO4 → BaSO4 ↓ + 2NaCl
1) черный
2) белый
3) кирпично-красный
4) желтый
4. Какой из осадков не растворяется в уксусной кислоте:
1) BaCO3
2) BaHPO4
3) BaC2O4
4) BaCrO4
5. Продукты реакции взаимодействия сульфата натрия с ацетатом свинца:
1) PbSO4 + 2NaCl
2) PbSO3 + 2NaCl
3) PbSO4 + 2CH3COONa
4) Na2PbO2 + Na2SO4 + H2O
6. Какая реакция сопровождается обесцвечиванием раствора:
1) реакция сульфид-иона с разбавлением минеральными кислотами
2) реакция сульфит-иона с раствором йода
3) реакция сульфат-иона с ацетатом свинца
4) реакция фосфат-иона с нитратом серебра
7. Цвет осадка, образующегося в результате реакции:
𝐍𝐚𝟑𝐏𝐎𝟒 + 𝟑𝐀𝐠𝐍𝐎𝟑 → 𝐀𝐠𝟑𝐏𝐎𝟒 ↓ + 𝟑𝐍𝐚𝐍𝐎𝟑
1) желтый
2) кирпично-красный
3) белый
4) белый творожистый осадок
8. Какой химической формуле соответствует белый кристаллический осадок:
1) Ag3PO4 ↓
2) MgNH4PO4 ↓
3) BaCrO4 ↓
4) AgI ↓
9. Какой осадок растворяется в избытке реактива:
1) Ag2S2O3 ↓
2) BaSO4 ↓
3) Ba(BO2)2 ↓
4) BaCO3 ↓
10. В какой цвет окрасится куркумовая бумага, смоченная тетраборатом натрия с несколькими каплями соляной кислоты при высушивании:
1) черный цвет
2) желтый цвет
3) розовый цвет
4) оранжевый цвет








