Задание творческого уровня.
1. Огнев Н. Повесть « Дневник Кости Рябцева».
…Сегодня Черная Зоя сдавала экзамен за октябрь Алмакфишу и вдруг как шлепнется в обморок. Ну, теперь этим никого не удивишь. Сейчас же опрыскали водой, дали понюхать нашатырю, и она встала.
ВОПРОС: Какое вещество называется нашатырем?
Что дают нюхать человеку, потерявшему сознание?
ОТВЕТЫ:
1. Нашатырь – техническое название хлорида аммония NH 4 CL .Это кристаллическая соль, без запаха, применяемая в паяльном деле, для изготовления сухих элементов в химических производствах. В качестве лекарственного средства при обмороке применяют нашатырный спирт - 10% водный раствор аммиака. Выделяющийся из раствора газообразный NH3 раздражает нервные окончания верхних дыхательных путей и рефлекторно возбуждает центральную нервную систему - пострадавший приходит в сознание. Вдыхать NH3 рекомендуют также при отравлениях некоторыми газообразными ядовитыми веществами.
3.Физические свойства
Все водородные соединения неметаллов образованы ковалентными полярными связями, имеют молекулярное строение и при обычных условиях является газами, кроме воды (жидкость).
Для водородных соединений неметаллов характерно различное отношение к воде. Метан и силан в ней практически нерастворимы. Аммиак при растворении в воде образует слабое основание – гидрат аммиака NH3 ∙ Н2О.
При растворении в воде сероводорода, селеноводорода, теллуроводорода, а также галогеноводородов образуются кислоты с той же формулой, что и сами водородные соединения: H2S, H2Se, H2Te, HF, HCI, HBr, HI.
Если сравнить кислотно –основные свойства водородных соединений, образованных неметаллами одного периода, например второго (NH3, H2O, H F) или третьего (PH3, H2S, HCI), то можно сделать вывод о закономерном усилении их кислотных свойств и соответственно ослаблении основных. Это, очевидно, связано с тем, что увеличивается полярность связи Э-Н (где Э – неметалл).
4.Химические свойства: кислотно-основные и восстановительные.
а) Водород проявляет свойства восстановления при взаимодействии с неметаллами, некоторыми оксидами и солями:
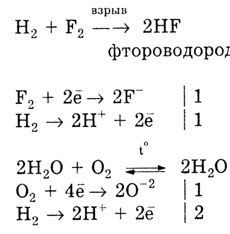
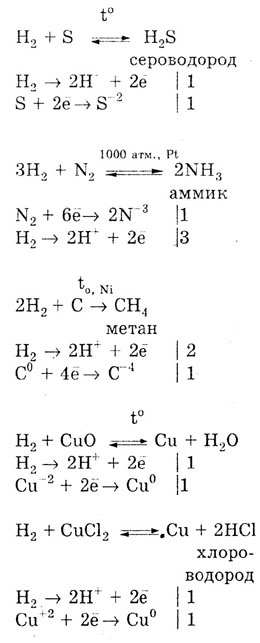 б) Окислительные свойства водород проявляет только при взаимодействии со щелочными и щелочноземельными металлами, образуя гидриды — твердые вещества белого цвета:
б) Окислительные свойства водород проявляет только при взаимодействии со щелочными и щелочноземельными металлами, образуя гидриды — твердые вещества белого цвета:
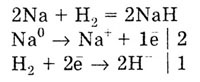
|
Кислотные свойства определяются способностью вещества диссоциировать с образованием катиона водорода.
Основные свойства определяются способностью вещества присоединять катион водорода на неподеленную электронную пару.
? Как изменяются и почему кислотно-основные свойства водородных соединений неметаллов в периоде и в группе. ( в периоде увеличиваются кислотные свойства, т.к. увеличивается полярность связи Э-Н и «+» заряд ядра; в группе кислотные свойства усиливаются, т.к. длина связи Э-Н увеличивается, прочность ее уменьшается, диссоциация происходит легче).
?А вода? Какими свойствами обладает: основными или кислотными? Ваши предположения…
( амфотерность воды можно доказать: а) ее взаимодействием как с кислотными, так и с основными оксидами.)
? запишите уравнения этих реакций;
Разбираем сущность некоторых реакций с точки зрения процессов окисления и восстановления:
CH4 + 2O2 → CO2 + 2H2O
S + 6HNO3 → H2SO4 + 6NO2 + 2H2O
6P + 5KClO3 → 5KCl + 3P2O5
Cl2 + H2O → HCl + HClO
H2 + CuO → Cu + H2O
CH4 + Cl2 → CH3Cl + HCl
5.Значение некоторых водородных соединений неметаллов в жизни природы и хозяйственной деятельности человека
Мета́н (лат. Methanum) — простейший углеводород, бесцветный газ (в нормальных условиях) без запаха, химическая формула — CH4. Малорастворим в воде, легче воздуха. При использовании в быту, промышленности в метан обычно добавляют одоранты (обычно тиолы) со специфическим «запахом газа».
Накапливаясь в закрытом помещении, метан взрывоопасен. Обогащение одорантами делается для того, чтобы человек вовремя заметил утечку газа.
Взрывоопасен при концентрации в воздухе от 4,4 % до 17 %. Наиболее взрывоопасная концентрация 9,5 %. Является наркотиком; действие ослабляется ничтожной растворимостью в воде и крови.
Аммиак - NH3, нитрид водорода, бесцветный газ с резким запахом, температура плавления –80° С, температура кипения – 36° С, хорошо растворяется в воде, спирте и ряде других органических растворителей. Синтезируют из азота и водорода. В природе образуется при разложении азотсодержащих органических соединений.
Резкий запах аммиака (запахнашатырного спирта и мочи
) известен человеку с доисторических времен, так как этот газ образуется в значительных количествах при гниении, разложении и сухой перегонке содержащих азот органических соединений, например мочевины или белков. Не исключено, что на ранних стадиях эволюции Земли в ее атмосфере было довольно много аммиака. Однако и сейчас ничтожные количества этого газа всегда можно обнаружить в воздухе и в дождевой воде, поскольку он непрерывно образуется при разложении животных и растительных белков. На некоторых планетах Солнечной системы ситуация иная: астрономы считают, что значительная часть масс Юпитера и Сатурна приходится на твердый аммиак.Вода — бинарное неорганическое соединение с химической формулой Н₂O. Молекула воды состоит из двух атомов водорода и одного — кислорода, которые соединены между собой ковалентной связью.
Сероводород – (серни́стый водоро́д, сульфи́д водоро́да, дигидросульфи́д) — бесцветный газ со сладковатым вкусом, имеющий запах протухших куриных яиц. Бинарное химическое соединение водорода и серы. Химическая формула — H2S. Плохо растворим в воде, хорошо — в этаноле. Ядовит. При больших концентрациях взаимодействует со многими металлами. Огнеопасен. Концентрационные пределы воспламенения в смеси с воздухом составляют 4,5—45 % сероводорода. Используется в химической промышленности для синтеза некоторых соединений, получения элементарной серы, серной кислоты, сульфидов. Сероводород также используют в лечебных целях, например, в сероводородных ваннах.
Диборан – химическое соединение водорода и бора с формулой B₂H₆. Был впервые синтезирован в XIX веке. Представляет собой бесцветный газ с запахом тухлых яиц. Диборан - очень ядовитый бороводород.
Силан – (кремневодороды, гидриды кремния) — соединения кремния с водородом. Источник чистого кремния для микроэлектронной промышленности.








