Тема: «Основы качественного анализа. Биогенные элементы, биологическая роль, применение в медицине».
1. Актуальность темы:
Для студента-медика представляет существенный интерес специфическая биологическая роль каждого элемента в организме человека. Недостаток или избыток в организме ионов макро- и микроэлементов вызывает нарушение протекания различных физиологических процессов и приводит к патологическим состояниям.
В медицине широко применяется ряд лекарственных средств, в состав которых входят биогенные элементы. Приобретенные знания о биологической роли элементов и их соединений, о применении лекарственных препаратов на основе биогенных элементов в медицинской практике необходимы будут студентам при изучении курсов биологической химии, фармакологии, нормальной и патологической физиологии и т.д.
2. Цель обучения:
Знать особенности строения атомов s-, р- и d-элементов и взаимосвязь с их свойствами, биогенную ролью элементов и применение в медицине лекарственных препаратов на основе их соединений. Уметь выполнять качественные реакции на катионы биогенных элементов в растворе.
3. Вопросы для обсуждения:
|
- Значение методов качественного анализа в медицине и других областях практической деятельности (санитарно-гигиенической практике).
- Классификация химических элементов, содержащихся в организме человека (органогены, «металлы жизни», макро-, микро-, ультрамикроэлементы).
- Макро- и микроэлементы в организме человека (суточное поступление, среднее содержание). Биологическая роль макро- и микроэлементов. Применение соединений макро- и микроэлементов в современной медицине.
- Взаимосвязь между содержанием биогенных элементов в организме человека и местом обитания. Связь эндемических заболеваний с особенностью биогеохимических провинций.
4. Вспомогательный материал:
4.1. Основы качественного анализа
Научные исследования и практика показали необходимость проведения качественного анализа веществ и их смесей. На основании анализа мочи, крови, желудочного сока можно получить данные, которые облегчают распознать заболевание, дают возможность следить за течением болезни. При помощи качественного анализа разрешается вопрос о пригодности медицинских препаратов для лечебных целей.
Качественный анализ (определение количественного состава вещества, т.е. установление количества химических элементов, ионов, атомов, атомных групп, молекул в анализируемом веществе, смеси веществ).
В химических методах качественного анализа используют характерные качественные аналитические реакции, для которых присущи определенные внешние проявления: образование в растворах цветных осадков, изменение цвета раствора или сплава, выделение газообразных продуктов без запаха или с определенным запахом и т.д. Вещество, которое используют для проведения качественной реакции, называют реагентом.
При выполнении качественного анализа нужна определенная масса пробы. В зависимости от величины взятой для анализа пробы методы разделяют на: макро-, полумикро-, микро- методы качественного анализа.
В макроанализе используют 0,5-1,0 г вещества или 20-50 мл раствора. Анализ выполняют в обычных пробирках, химических стаканах, колбах, осадки отделяют фильтрованием через бумажные фильтры.
В микроанализе используют 0,010-0,001 г вещества или 0,05-0,5 мл раствора, реакции выполняют капельным или микрокристаллическим методом.
Полумикроанализ занимает промежуточное место между макро- и микро- методами. Для анализа, как правило, используют от 0,01 до 0,10 г сухого вещества.
Аналитические реакции выполняют с помощью капельниц. Отделение твердой и жидкой фаз проводят с помощью центрифуги. В аналитической практике используют чаще полумикрометод.
Аналитические реакции (химическое превращение анализируемого вещества при действии аналитического реагента с образованием продуктов с заметными аналитическими признаками) выполняют «сухим» и «мокрым» способом.
В первом случае исследуемую пробу и аналитический реагент берут в твердом состоянии и подвергают нагреванию при высокой температуре.
К таким способам относятся:
ü Реакция окрашивания пламени. Соли некоторых металлов на платиновом стержне вносят в ту часть пламени спиртовки, которая не светится и наблюдают окрашивание пламени в характерный цвет.

ü Спекание с некоторыми сухими реагентами (Nа2CO3, KClO3, KNO3) для получения характерных окрашенных продуктов.
Реакции, выполняемые «сухим» способом, носят вспомогательный характер.
Основными реакциями в качественном анализе являются реакции выполненные «мокрым» способом (в растворе). Они должны сопровождаться внешним эффектом: изменение окраски раствора, образование или растворение осадка, выделение газа.

4.2. Химические элементы в организме человека.
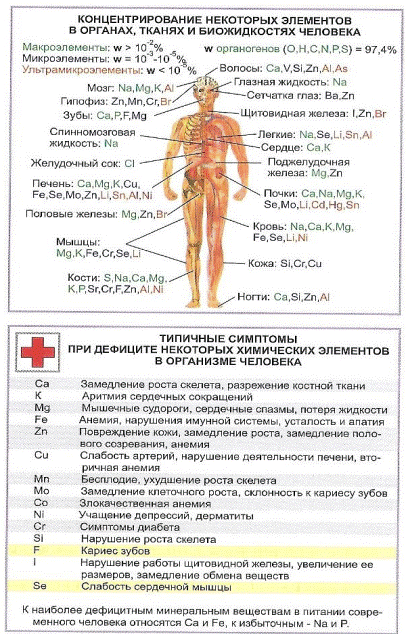
5. Выполнить тестовые задания (письменно):
| 1. | Какие химические свойства обуславливают использование KMnO4 в медицине как антисептика? | |
| А | способность к полной диссоциации на ионы | |
| В | отсутствие гидролиза | |
| С | восстанавливающие свойства | |
| D | окислительные свойства | |
| 2. | Какой элемент входит в состав основных антиоксидантных соединений и усиливает иммунную защиту? | |
| А | Co | |
| В | Se | |
| С | Zn | |
| D | Cr | |
| 3. | При недостатке этого элемента развивается синдром нарушения толерантности к глюкозе, сопутствующего сахарному диабету: | |
| А | Со2+ | |
| В | Са2+ | |
| С | Сr2+ | |
| D | Ni2+ | |
| 4. | Недостаток ионов Са в организме при нарушении кальциевого обмена в организме человека приводит к развитию: | |
| А | дисбактериоза | |
| В | диабета | |
| С | рахита | |
| D | анемии | |
| 5. | Обмен этого элемента тесно связан с обменом кальция. Он является основой скелета человека и животных, зубов. Это элемент: | |
| А | N | |
| В | P | |
| С | O | |
| К | ||
| 6. | При недостатке этого элемента развивается злокачественная анемия (анемия Аддисон-Бирмера): | |
| А | Cu2+ | |
| В | Са2+ | |
| С | Сr2+ | |
| D | Со2+ | |
| 7. | Какой из ионов вызывает торможение центральной нервной системы: | |
| А | I- | |
| В | Br - | |
| С | F- | |
| D | Мо2+ | |
| 8. | Недостаток иона железа (II) в организме приводит к развитию: | |
| А | дисбактериоза | |
| В | диабета | |
| С | рахита | |
| D | анемии | |
| 9. | Порошок этого вещества применяется наружно в виде мазей и присыпок, при лечении кожных заболеваний (себорреи). Он входит в состав аминокислоты цистеин. Это: | |
| А | N | |
| В | S | |
| С | C | |
| D | К | |
| 10. | Ион, принимающий участие в построении эпителиальной и соединительной тканей: | |
| А | Са2+ | |
| В | Аl3+ | |
| С | Zn2+ | |
| D | Fe3+ | |
| 11. | Центральный ион – комплексообразователь молекулы хлорофилла: | |
| А | Cu2+ | |
| В | Ca2+ | |
| С | Mg2+ | |
| D | Zn2+ | |
| 12. | Концентрация этого элемента в организме в организме человека около 10%, в земной коре – 1%. Он связующий элемент между цепями ДНК и вторичной структуры белков: | |
| А | S | |
| В | H | |
| С | N | |
| D | О | |
| 13. | Ионы этого элемента в зависимости от концентрации, блокируют или обеспечивают нервно-мышечную передачу, они угнетают центр дыхания, а также сосудодвигательный центр, благодаря чему снижают артериальное давление. Это - ион: | |
| А | Co2+ | |
| В | Mg2+ | |
| С | P5+ | |
| D | Na+ | |
| 14. | Ион какого элемента, участвует в биосинтезе половых гормонов (тестостерона) и регулирует функцию половых желез: | |
| А | I- | |
| В | Сl- | |
| С | Br- | |
| D | F- | |
| 15. | Для нормального процесса кроветворения необходимо присутствие трех элементов: | |
| А | Fe, Zn, Co | |
| В | Co, Fe, Cr | |
| С | Fe, Co, Cu | |
| D | Cu, Mo, Fe | |
| 16. | Питьевая сода (NaHCO3) используется для полоскания горла в виде 2% раствора. Сколько грамм соды нужно растворить в стакане воды (200 мл) для приготовления данного раствора. | |
| А | 4,0 г. | |
| В | 4,1 г. | |
| С | 2 г. | |
| D | 20 г. | |
| 17. | Какой ион принимает участие в процессе переноса кислорода к органам и тканям? | |
| А | Cr3+ | |
| В | Fe3+ | |
| С | Cd2+ | |
| D | Fe2+ | |
| 18. | Какой из катионов является комплексообразователем в молекуле гемоглобина? | |
| А | Fe3+ | |
| В | Co3+ | |
| С | Hg2+ | |
| D | Fe2+ | |
| 19. | Заболевание “Эндемический зоб” наблюдается при недостатке в организме элемента: | |
| А | Br | |
| В | I | |
| С | Cl | |
| D | F | |
| 20. | Какой из катионов является комплексообразователем в молекуле витамина В12? | |
| А | Fe3+ | |
| В | Co2+ | |
| С | Mg2+ | |
| D | Zn2+ |








