Примеры дисперсных систем
| Дисперсионная среда | Дисперсная фаза | Примеры некоторых природных и бытовых дисперсных систем |
| Газ | Газ | Всегда гомогенная смесь (воздух, природный газ) |
| Жидкость | Туман, попутный газ с капельками нефти, карбюраторная смесь в двигателях автомобилей (капельки бензина в воздухе), аэрозоли | |
| Твердое вещество | Пыли в воздухе, дымы, смог, самумы (пыльные и песчаные бури), аэрозоли | |
| Жидкость | Газ | Шипучие напитки, пены |
| Жидкость | Эмульсии. Жидкие среды организма (плазма крови, лимфа, пищеварительные соки), жидкое содержимое клеток (цитоплазма, кариоплазма) | |
| Твердое вещество | Золи, гели, пасты (кисели, студни, клеи). Речной и морской ил, взвешенные в воде; строительные растворы | |
| Твердое вещество | Газ | Снежный наст с пузырьками воздуха в нем, почва, текстильные ткани, кирпич и керамика, поролон, пористый шоколад, порошки |
| Жидкость | Влажная почва, медицинские и косметические средства (мази, тушь, помада и т. д.) | |
| Твердое вещество | Горные породы, цветные стекла, некоторые сплавы |
| Дисперсные системы | Вид дисперсной системы, ее обозначение. | Примеры дисперсных систем | |
| Дисперсионная фаза | Дисперсионная среда | ||
| Твердое тело | Газ (г) | Аэрозоль (т/г) | Пыль, дым, хлопья снега |
| Жидкость (ж) | Суспензии (т/ж) Коллоидные растворы (т/ж) Истинные растворы (т/ж) | Глина, зубная паста, губная помада. Раствор яичного белка, плазма крови, спиртовая вытяжка хлорофилла, кремниевая кислота. Растворы солей, щелочей, сахара. | |
| Твердое тело (т) | Твердые растворы (т/т) | Сплавы, минералы, цветные стекла. | |
| Жидкость | Газ (г) | Аэрозоль (ж/г) | Туман, облака, моросящий дождь, струя из аэрозольного баллончика. |
| Жидкость(ж) | Эмульсия (ж/ж) Истинные растворы (ж/ж) | Молоко, масло, майонез, крем, мази, эмульсионные краски. Нисшие спирты +вода, ацетон + вода. | |
| Твердое тело (т) | Твердая эмульсия (ж/т) | Жемчуг, опал. | |
| Газ | Газ (г) | Дисперсной системы не образуется | |
| Жидкость (ж) | Пена (г/ж) | Пена газированной воды, мыльная пена, взбитые сливки, взбитый крем, пастила. | |
| Твердое тело (т) | Твердая пена (г/т) | Пенопласт, пенобетон, пеностекло, пемза, лава. | |
Дисперсные системы изучает специальный раздел химии – коллоидная химия. Мы будем знакомиться в основном с третьей группой – истинными растворами.
Растворы — гомогенные (однородные) системы переменного состава, которые содержат два или несколько компонентов.
По агрегатному состоянию растворы подразделяются:
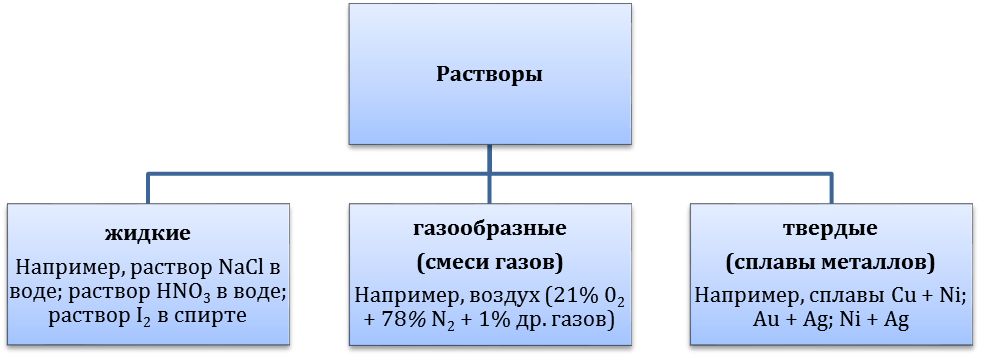
Наиболее распространены жидкие растворы. Они состоят из растворителя (жидкости) и растворенных веществ (газообразных, жидких, твердых):
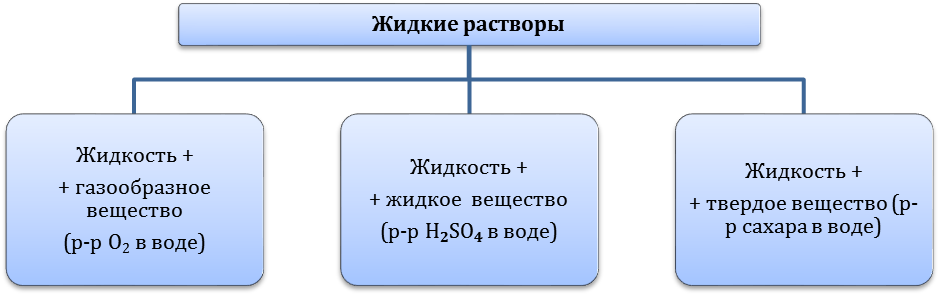
Жидкие растворы могут быть водные и неводные. Водные растворы — это растворы, в которых растворителем является вода. Неводные растворы — это растворы, в которых растворителями являются другие жидкости (бензол, спирт, эфир и т. д.).
На практике чаще применяются водные растворы.
Растворение веществ (образование растворов).
Растворение — сложный физико-химический процесс, который включает несколько стадий:
1. Разрушение кристаллической решетки растворенного вещества.
Рассмотрим растворение хлорида калия в воде.

Например, при внесении в воду кристалликов хлорида калия с их поверхности постепенно начинают отрываться ионы К+ и Сl-.
Причиной этого являются собственные колебательные движения частиц и притяжение со стороны молекул растворителя.
2. Постепенный переход частиц, образующих кристалл, в раствор.
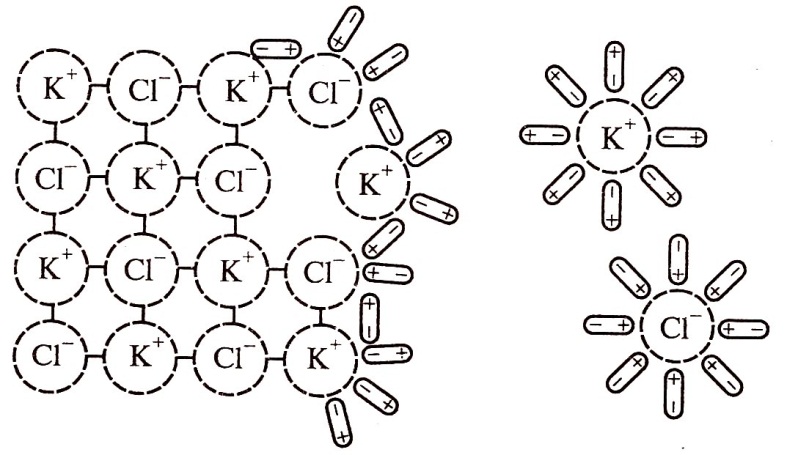
Рис. 1. Схема разрушения кристаллической решетки хлорида калия в воде
3. Распределение частиц, перешедших в раствор, по всему объему растворителя.
Растворы, компонентами которых являются ионы, называются ионными (растворы электролитов, так как они проводят электрический ток). Растворы, компонентами которых являются электро-нейтральные частицы, называются молекулярными (растворы неэлектролитов).
Долгое время считалось, что растворитель — это среда, химически инертная по отношению к растворенному веществу. То есть между частицами растворителя и частицами растворенного вещества отсутствует межмолекулярное взаимодействие, как и в обычных механических смесях.
Данная теория получила название физической теории растворов. Основоположниками физической теории являлись Якоб Г. Вант-Гофф (1885 г.) и Сванте А. Аррениус (1883 г.).
Классификация дисперсных систем
По величине частиц веществ, составляющих дисперсную фазу, дисперсные системы делятся на грубодисперсные (взвеси) с размерами частиц более 100 нм и тонкодисперсные (коллоидные растворы или коллоидные системы) с размерами частиц от 100 до 1 нм. Если же вещество раздроблено до молекул или ионов размером менее 1 нм, образуется гомогенная система – раствор. Она однородна, поверхности раздела между частицами и средой нет.
Дисперсные системы и растворы очень важны в повседневной жизни и в природе. Судите сами: без нильского ила не состоялась бы великая цивилизация Древнего Египта; без воды, воздуха, горных пород и минералов вообще бы не существовала живая планета – наш общий дом – Земля; без клеток не было бы живых организмов и т.д.
Грубодисперсные системы
Взвеси
Взвеси – это дисперсные системы, в которых размер частицы фазы более 100 нм. Это непрозрачные системы, отдельные частицы которых можно заметить невооруженным глазом. Дисперсная фаза и дисперсная среда легко разделяются отстаиванием, фильтрованием. Такие системы разделяются на:
1. Эмульсии (и среда, и фаза – нерастворимые друг в друге жидкости). Из воды и масла можно приготовить эмульсию длительным встряхиванием смеси. Это хорошо известные вам молоко, лимфа, водоэмульсионные краски и т.д.
2. Суспензии (среда – жидкость, фаза – нерастворимое в ней твердое вещество). Чтобы приготовить суспензию , надо вещество измельчить до тонкого порошка, высыпать в жидкость и хорошо взболтать. Со временем частица выпадут на дно сосуда. Очевидно, чем меньше частицы, тем дольше будет сохраняться суспензия. Это строительные растворы, взвешенный в воде речной и морской ил, живая взвесь микроскопических живых организмов в морской воде – планктон, которым питаются гиганты – киты, и т.д.
3. Аэрозоли взвеси в газе (например, в воздухе) мелких частиц жидкостей или твердых веществ. Различаются пыли, дымы, туманы. Первые два вида аэрозолей представляют собой взвеси твердых частиц в газе (более крупные частицы в пылях), последний – взвесь капелек жидкости в газе. Например: туман, грозовые тучи – взвесь в воздухе капелек воды, дым – мелких твердых частиц. А смог, висящий над крупнейшими городами мира, также аэрозоль с твердой и жидкой дисперсной фазой. Жители населенных пунктов вблизи цементных заводов страдают от всегда висящей в воздухе тончайшей цементной пыли, образующейся при размоле цементного сырья и продукта его обжига – клинкера. Дым заводских труб, смоги, мельчайшие капельки слюны, вылетающих изо рта больного гриппом, также вредные аэролози. Аэрозоли играют важную роль в природе, быту и производственной деятельности человека. Скопление облаков, обработка полей химикатами, нанесение лакокрасочных покрытий при помощи пульверизатора, лечение дыхательных путей (ингаляция) – примеры тех явлений и процессов, где аэрозоли приносят пользу. Аэрозоли – туманы над морским прибоем, вблизи водопадов и фонтанов, возникающая в них радуга доставляет человеку радость, эстетическое удовольствие.
Для химии наибольшее значение имеют дисперсные системы, в которых средой является вода и жидкие растворы.
Природная вода всегда содержит растворенные вещества. Природные водные растворы участвуют в процессах почвообразования и снабжают растения питательными веществами. Сложные процессы жизнедеятельности, происходящие в организмах человека и животных, также протекают в растворах. Многие технологические процессы в химической и других отраслях промышленности, например получение кислот, металлов, бумаги, соды, удобрений, протекают в растворах.
Тонкодисперсные системы








