Тема 16. Неметаллы
Урок № 16.1. Обзор неметаллов
Урок № 16.2. Свойства и применение важнейших неметаллов.
Цель урока - дать общую характеристику неметаллов, актуализировать знания учащихся о физических свойствах неметаллов, о типах кристаллических решеток; развивать умения применять знания, сравнивать и делать выводы; воспитывать химическую аккуратность по отношению к окружающей среде.
Тип урока - изучение нового материала.
Планируемые результаты
Личностные
- проявление эмоционально-ценностного отношения к учебной проблеме;
- проявление творческого отношения к процессу обучения.
Метапредметные
Познавательные:
- умение находить сходство и различие между объектами, обобщать полученную информацию;
- умение вести наблюдение;
- умение прогнозировать ситуацию.
Регулятивные:
- умение выполнять учебное задание в соответствии с целью;
- умение соотносить учебные действия с известными правилами;
- умение выполнять учебное действие в соответствии с планом.
Коммуникативные:
- умение формулировать высказывание;
- умение согласовывать позиции и находить общее решение;
- умение адекватно использовать речевые средства и символы для представления результата.
Предметные:
-умение характеризовать физические и химические свойства неметаллов;
- умение характеризовать аллотропные видоизменения неметаллов;
- умение распознавать вещества;
Формы организации деятельности: групповая, индивидуальная, парная.
Методы обучения: частично - поисковый, личностно-ориентированное обучение.
Ход урока:
Вступление учителя : «Впервые облако хлора появилось над полем сражения у Ипра. Англичане были совершенно не подготовлены и не защищены от бесшумной смерти, которая неслась на них 22 апреля 1915 года. Результат этой газовой атаки был ужасен: из строя выведено 15000 человек, из которых 5000 погибло. Фронт на протяжении 8 км был прорван. Возникла необходимость срочно найти защиту от нового вида оружия. Такой защитой явился предложенный в 1915 году Н. Д. Зелинским противогаз с активным углем, который хорошо поглощал отравляющие вещества в парообразном и газообразном состоянии.
Современная химия вовлекает в круг своих исследований вещества, ранее считавшиеся опасными и ядовитыми. Так, например, важнейшим достижением последнего времени является использование фтора для создания ракетного топлива, в котором окислителем служит фтор, а горючим – водород; их теплотворная способность превышает теплотворную способность всех других видов топлив».
Вопрос: Как вы думаете, о чем пойдет речь сегодня на уроке? Ребята отвечают
Итак, тема урока «Общая характеристика неметаллов» Запись на доске.
Учитель: в процессе изучения химии вы уже познакомились со многими элементами неметаллами и их соединениями. Из известных на сегодняшний день химических элементов 22 относятся к неметаллам. Хотя число элементов неметаллов относительно невелико, они входят в состав практически всех органических и неорганических веществ. Вспомните, что самыми распространёнными элементами в земной коре являются неметаллы кислород и кремний.
Неметаллы расположены в основном в правом верхнем углу ПС, условно ограниченном диагональю бор-астат. Самым активным является фтор.
2. Особенности строения атомов неметаллов.
Во внешнем электронном слое атомов неметаллов находится от трёх до восьми электронов.
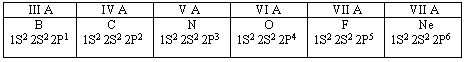
Для атомов неметаллов, по сравнению с атомами металлов характерны:
- меньший атомный радиус;
- четыре и более электрона на внешнем энергетическом уровне.
Отсюда и такое важнейшее свойство атомов неметаллов – тенденция к приёму недостающих до 8 электронов, т.е. окислительные свойства. Качественной характеристикой атомов неметаллов, т.е. своеобразной мерой их неметалличности, может служить электроотрицательность, т.е. свойство атомов химических элементов поляризовать химическую связь, оттягивать к себе общие электронные пары. Электроотрицательность – мера неметалличности, т.е. чем более электроотрицателен данный химический элемент, тем ярче выражены неметаллические свойства.
3. Кристаллическое строение неметаллов-простых веществ. Аллотропия.
Если металлы – простые вещества образованы за счет металлической связи, то для неметаллов – простых веществ характерна ковалентная неполярная химическая связь. В отличие от металлов неметаллы – простые вещества, характеризуются большим многообразием свойств. Неметаллы имеют различное агрегатное состояние при обычных условиях:
- газы – H2, O2, O3, N2, F2, Cl2;
- жидкость – Br2;
- твердые вещества – модификации серы, фосфора, кремния, углерода и др.
Гораздо богаче у неметаллов и спектр цветов: красный – у фосфора, красно-бурый – у брома, желтый – у серы, желто-зеленый – у хлора, фиолетовый – у паров йода. Элементы – неметаллы более способны, по сравнению с металлами, к аллотропии.
Способность атомов одного химического элемента образовывать несколько простых веществ называется аллотропией, а эти простые вещества – аллотропными видоизменениями или модификациями.
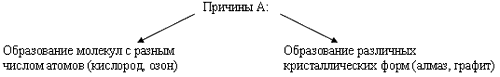
5. Физические свойства неметаллов.
- Ковкость отсутствует
- Блеска нет
- Теплопроводность (только графит)
- Цвет разнообразный: желтый, желтовато-зеленый, красно-бурый.
- Электропроводность (только графит и черный Фосфор.)
- Агрегатное состояние:
- газообразное(H2, O2, Cl2 ,F2, O3)
- твердое (Р, С)
- жидкое (Br2)
6. Химические свойства неметаллов.
Неметаллы в химических реакциях могут быть восстановителями и окислителями (фтор, кислород.)
- Неметаллические свойства элементов усиливаются в периодах и ослабевают в подгруппах с увеличением порядкового номера элемента.
- Высшие кислородные соединения неметаллов имеют кислотный характер (кислотные оксиды и гидроксиды).
- Атомы элементов-неметаллов способны как принимать электроны, проявляя окислительные функции, так и отдавать их, проявляя восстановительные функции.
В качестве закрепления заполните таблицу на основании текста параграфа
ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ НЕМЕТАЛЛОВ
| Общая характеристика | ||
| 1 | Общее количество элементов неметаллов | |
| 2 | Положение в ПСХЭ | |
| 3 | Элементы относящиеся к неметаллам | |
| 4 | Группы неметаллов | |
| 5 | Количество электронной на внешнем энергетическом уровне | |
| 6 | Самый электроотрицательный неметалл | |
| 7 | Распространенность в природе | |
Рефлексия: Ребята, поделись своими эмоциями по уроку, что было понятно, что было трудно или легко на уроке, интересен ли вам был урок?








