Для оценки насыщения эритроцитов гемоглобином рассчитывают цветной показатель (ЦП).
Hb больного Эритроциты больного
ЦП = -------- --------- : -------------------------------
Нb норма Эритроциты в норме
В норме ЦП должен быть равным 0,9-1,0 (нормохромия).
Цветной показатель используется для оценки типа анемий. Если при анализе ЦП увеличен - гиперхромная анемия, при которой снижение эритроцитов компенсируется увеличением их насыщения гемоглобином, при уменьшении ЦП - гипохромная анемия.
О дыхательной, газотранспортной функции крови (Нb эритроцитов) судят по величине ее емкости, насыщения и сродству. Емкость – это способность крови связывать максимальное количество транспортируемых газов (O2, СO2, СО). Ее величина зависит от количества эритроцитов и Нb в крови, в норме она равна 93–97 %. Насыщение – способность крови связывать реальное (фактическое) количество газов. В частности, артериальная кровь насыщается кислородом на 73–78 %, венозная – примерно на 55 %. Сродство Нb крови к газам в процессе жизни и в различных отделах кровеносного русла существенно меняется.
Эритропоэз – образование зрелых эритроцитов благодаря процессам деления, дифференцировки и созревания клеток эритроидного (миелоидного) ряда. Происходит в красном ростке миелоидной ткани костного мозга. Он регулируется сложными и разнообразными нервно-гормонально-гуморальными механизмами при превалирующем влиянии гуморальных факторов. Среди последних центральное место занимают:
§ образующиеся в почках, печени и селезенке эритропоэтины (резко влияющие на образование, пролиферацию и дифференцировку эритропоэтинчувствительных клеток),
§ стимуляторы и ингибиторы эритропоэтинов,
§ продукты распада эритроцитов,
§ гипоксемия различного генеза,
§ факторы Касла (витамин В12 и гастромукопротеин),
§ гормоны (тестостерон, АКТГ, кортизол, ТТГ, тироксин, СТГ, эстрогены),
§ витамины (В12, фолиевая кислота, аскорбиновая кислота, В6, В2),
§ макро- и микроэлементы (железо, цинк, кобальт и др.).
В регуляции эритропоэза важное место также принадлежит нервным механизмам (с участием коры больших полушарий, гипоталамуса, симпатического и парасимпатического отделов вегетативной нервной системы), осуществляющих преимущественно рефлекторное нервно-трофическое влияние не только на органы кроветворения, кроворазрушения и кроводепонирования, но и на активность эндокринных регуляторных структур, а также на исполнительные органы и системы (выделения, пищеварения, кровообращения, дыхания, детоксикации, иммунную и др.), участвующие в эритропоэзе и эритродиерезе.
Малокровие (анемия) – снижение числа эритроцитов в крови и (или) уменьшение содержания в них гемоглобина. Причинами малокровия является плохое питание, инфекционные заболевания, кровопотери, авитаминозы, злокачественные опухоли, недостаток железа в пище, например, при вегетарианском питании. Обычно малокровие излечимо.
Средства, влияющие на эритропоэз Для стимуляции эритропоэза при анемиях применяют рекомбинантный эритропоэтин человека — эпоэтин-α и эпоэтин-β. Он синтезируется в клетках млекопитающих, в которые встроен ген, кодирующий эритропоэтин человека. По биологическим и иммунологическим свойствам он идентичен эритропоэтину человека, выделяемому из мочи. Этот препарат оказывает выраженный эффект при анемии, обусловленной хроническими заболеваниями почек.
Для лечения анемий, в зависимости от их этиологии, применяют различные антианемические препараты, влияющие на эритропоэз. Так, например, для лечения железодефицитных анемий используют препараты железа для внутреннего применения (железа глюконат, сульфат, фумарат) и парентерального введения (железа гидроксид ), а также аскорбиновую кислоту, улучшающую всасывание железа, препараты, содержащие кобальт (коамид), последний способствует усвоению организмом железа. Для лечения В12-дефицитной анемии применяют витамин В12 (цианокобаламин), для лечения анемии, вызванной дефицитом фолиевой кислоты, — фолиевую кислоту.
Лейкоциты.
Количество лейкоцитов - это показатель, характеризующий защитные силы организма - у здорового взрослого человека колеблется от 4000 до 9000 в 1 мкл или (4–9) × 109 в литре крови. Количество лейкоцитов в крови определяется активностью следующих процессов: лейкопоэза, разрушения лейкоцитов, их депонирования и выброса из депо, регулируемых нервно-гуморально-гормональными механизмами.
На уровень лейкоцитов в крови влияют многие факторы: сезон года, время суток, погодно-климатические условия, прием пищи, возраст, мышечная активность, эмоциональное состояние, беременность, а также различные патогенные факторы, особенно те, которые вызывают болезнь организма. Увеличение лейкоцитов в крови больше нормы (> 4–9 × 109) называется лейкоцитозом, снижение меньше нормы (< 4–9 × 109) – лейкопенией.
Ряд физиологических состояний характеризуется развитием как лейкоцитоза (мышечная работа, прием пищи, эмоциональное напряжение, беременность, роды), так и лейкопенией (сон).
Функции лейкоцитов
1) Транспортная – все лейкоциты осуществляют транспорт антител (АТ), антигенов, токсинов, бактерицидных веществ, гормонов и др. ФАВ.
2) Триггерная (пусковая) – моноциты, нейтрофилы, лимфоциты запускают различные эволюционно выработанные физиологические процессы: воспаление, лихорадка, заживление и другие.
3) Защитная – все лейкоциты. Они ответственны за:
Обеспечение специфического иммунитета:
а) гуморального – выработка антител (В-лимфоциты с участием моноцитов и Т-лимфоцитов)
б) клеточного – отторжение трансплантата (происходит с участием Т-лимфоцитов и моноцитов);
Обеспечение неспецифического иммунитета путем:
а) фагоцитоза – макрофаги (моноциты, гистиоциты), микрофаги (нейтрофилы, эозинофилы, базофилы, тромбоциты),
б) связывания, транспортировки и разрушения токсических и различных инородных веществ – все лейкоциты,
в) выработки бактерицидных веществ – нейтрофилы, Т-лимфоциты, моноциты,
г) продукции различных интерферонов, в т.ч. противовирусного белка – лимфоциты, моноциты, нейтрофилы,
д) синтеза различных интерлейкинов, в т.ч. эндопирогенов, – моноциты, лимфоциты;
Защитную функцию осуществляет и гемостаз. При повреждении стенок он ограничивает кровопотери путем как закрытия телами форменных элементов крови дефектов в стенках сосуда, так и активизацией свертывающей системы крови (преимущественно тромбоциты). Поддерживает кровь в жидком состоянии и ограничивает тромбообразование путем активизации противосвертывающей системы крови (базофилы, тромбоциты) и фибринолитической системы крови (эозинофилы).
4). Регуляторно -трофическая – практически все лейкоциты. Они ответственны за:
§ повышение функциональной активности клеток, тканей, органов, систем;
§ активацию репаративных процессов (репаративной регенерации, восстановления поврежденных клеточных структур);
§ активацию лейкопоэза – продукты распада и метаболизма лейкоцитов;
§ повышение двигательной, фагоцитарной, адгезивной активностей лейкоцитов – продукты распада и метаболизма лейкоцитов;
§ выработку ФАВ – гепарина, гистамина (в основном, базофилами);
§ адсорбцию, перенос и инактивацию ФАВ (например, гистамина эозинофилами).
Лейкоциты подразделяются на гранулоциты и агранулоциты.
Гранулоциты называются так потому, что в их цитоплазме определяются гранулы. Образуются гранулоциты в миелоидной ткани красного костного мозга. Диаметр гранулоцитов колеблется от 8 до 14 мкм. Они составляют в среднем более 60 % всех лейкоцитов крови.
Общая продолжительность жизни гранулоцитов составляет от 1 до 2–4 дней, редко больше, а внутрисосудистая – от 0,3 до 0,5–1 суток.
В зависимости от тинкториальных свойств гранул (их способности окрашиваться кислыми, основными или теми и другими красками) клетки делятся на: нейтрофилы, эозинофилы, базофилы. Все гранулоциты обладают свойством выходить через стенку капиллярных сосудов в ткани (т. е. эмигрировать); двигаться в сторону распадающихся клеток, токсинов, микробов, антигенов (т.е. обладают положительным хемотаксисом); окружать, захватывать и переваривать инородные частицы (т.е. обладают свойством фагоцитоза), т.к. содержат большое количество разных ферментов (протеаз, пептидаз, диастаз, липаз, дезоксирибонуклеаз).
Фагоцитарная активность разных гранулоцитов различна: нейтрофилы > эозинофилы > базофилы.
Около 50 % гранулоцитов свободно циркулируют в крови, а около 50 % их находится в пристеночном (т. е. временно депонированном) состоянии (в капиллярах легких, кожи, пищеварительных и др. органов). Однако основная масса лейкоцитов депонирована в синусах костного мозга (где их содержится 10 × 1012, что во много раз превышает количество лейкоцитов, находящихся в крови). Интенсивность лейкопоэза достаточно высокая. В частности, из 1 миелобласта приблизительно за 130 ч образуется 16 миелоцитов. При прекращении митоза лейкоцитарных клеток, в костном мозге имеющихся гранулоцитов хватает для обеспечения функций организма только на несколько дней.
Гранулоциты, как и все лейкоциты, имеют очень много различных рецепторов, реагирующих на соответствующие ФАВ, а также связывающих антигены.
Нейтрофилы образуются в красном костном мозге от родоначальной клетки миелоидного ряда. После их образования они задерживаются в синусах костного мозга в течение 3–4 дней, где окончательно дозревают. В депо (синусах костного мозга, селезенке, печени, адгезирование на стенках сосудов) количество нейтрофилов в 10–20 раз больше, чем в циркулирующей крови. Время циркуляции в крови составляет, как правило, от 8–12 до 20–24 ч. После этого они элиминируют в ткани, где функционируют от 1 до 2–4 дней и обратно в кровь не поступают (т. е. не рециркулируют). Нейтрофилы могут выделяться в просвет пищеварительного тракта, воздухоносных путей, полость рта, носоглотки, мочевых путей, а также на слизистые глаз и кожу, где выполняют свои защитные функции. Разрушаются нейтрофилы преимущественно в легких и тканях пищеварительного тракта.
В норме в крови определяется 54–73 % нейтрофилов, которые имеют различную степень зрелости. В зависимости от этого выделяют следующие формы нейтрофилов – юные или метамиелоциты, палочкоядерные и сегментоядерные (процентное содержание которых составляет соответственно 0,5–1%, 3–6%, 51–67%). Протоплазма зрелых (сегментоядерных) нейтрофилов содержит мелкую облигатную зернистость, ядра состоят из 3–4 сегментов. Диаметр клеток составляет 9–12 мкм. У женщин и других лиц, имеющих две Х-хромосомы 7 из 500 клеток имеют половой хроматин (тельца Барра) в виде барабанных палочек (выросты сегментов ядра округлой формы длиной 1,5–2 мкм).
Количество нейтрофилов в крови постоянно колеблется. Оно днем больше, ночью меньше; в горизонтальном положении тела меньше, чем в вертикальном. Физическое, психоэмоциональное напряжение, различные виды стресса сопровождаются увеличением количества нейтрофилов в крови (нейтрофилией).
Нейтрофилы относятся к микрофагам, которые обладают большой двигательной активностью и способностью к хемотаксису (сближению с объектом фагоцитоза), опсонизации (опознании объекта фагоцитоза) и фагоцитозу (поглощению и перевариванию чужеродных объектов, в том числе микроорганизмов). Благодаря высокой активности ферментов, главным образом, гидролитических, лизоцима, лактоферрина, биооксидантов – перекиси водорода, супероксиданиона и других обеспечивается как внутриклеточное (благодаря эндоцитозу), так и внеклеточное (благодаря экзоцитозу) бактерицидное и бактериостатическое действие. Помимо этого нейтрофилы способны выделять в окружающую среду различные ФАВ (тромбопластин, плазминоген, протеиназы, гемостатический белок и многие другие). Нейтрофилы получают энергию всеми известными способами. Обладают большой способностью к анаэробному гликолизу, хотя для них характерны и окислительное фосфорилирование и пентозофосфатный шунт.
Эозинофилы образуются в костном мозге от родоначальной клетки миелоидного ряда. Время созревания от миелобласта до недостаточно зрелого эозинофила составляет 24 часа. За 3–4 суток нахождения клеток в костном мозге они дозревают, приобретают способность к амебовидному движению и фагоцитозу. После чего выходят в кровь, где циркулируют около 10 часов. Затем эмигрируют в ткани. В крови эозинофилов содержится 2–4%. Размер клеток составляет 12–14 мкм. Ядро чаще имеет 2–3 сегмента. Цитоплазма заполнена большим количеством крупных красных гранул, внешне напоминающих икринки кетовой икры.
Количество эозинофилов в крови колеблется в течение суток (утром и днем их меньше, ночью больше). Эти дневные колебания существенно зависят от суточной биоритмики глюкокортикоидных гормонов.
Эозинофилы обладают фагоцитозом, но он значительно слабее, чем у нейтрофилов. Способны связывать, транспортировать и инактивировать гистамин. Содержат много гистамина, гистаминаз, киназ, профибринолизина.
Эозинофилы повышают активность фибринолитической системы. Количество этих клеток в крови увеличивается при глистных инвазиях и аллергических процессах.
Эозинофилы обладают способностью к аэробному и анаэробному гликолизу и окислительному фосфорилированию.
Базофилы образуются в костном мозге от родоначальной клетки миелоидного ряда. В крови их незначительное (0,5–1%) количество. Представлены клетками небольшого (8–10 мкм) размера, отличающимися от других гранулоцитов наличием крупных, редких, базофильно окрашенных зерен. Ядра зрелых клеток чаще имеют 2–3 сегмента. Время циркуляции базофилов в крови составляет 10–12 часов. Время их жизни в тканях также мало, но все же больше, чем в крови.
Отмечаются суточные колебания содержания базофилов в крови (ночью их больше, утром и днем меньше), что в большей степени определяется суточными колебаниями уровня глюкокортикостероидов, прогестерона, тироксина, а также эстрогенов.
Базофилы содержат и синтезируют гистамин, гепарин и другие ФАВ. И являются переносчиками различных ФАВ. Имеют много рецепторов, реагирующих на ФАВ и связывающих антигены. При дегрануляции базофилов высвобождаются факторы агглютинации тромбоцитов, в итоге активируется свертывающая система крови. Выделяя гепарин базофилы активируют антисвертывающую систему крови. Они ответственны за активацию липолиза. Количество базофилов существенно увеличивается после приема жирной пищи.
Моноциты образуются в костном мозге от родоначальной клетки миелоидного и моноцитарного ряда. В кровь выходят неокончательно созревшими, циркулируя в крови дозревают. В крови содержится 4–8%, это самые большие по размерам клетки крови (12–20 мкм), в которых имеется большое бобовидное ядро, окруженное большой полоской сероголубой цитоплазмы. Относятся к макрофагам, содержат около 20 ферментов и много ФАВ (интерлейкины, лизоцим, фактор роста клеток, фактор активации фибробластов и другие). В различных тканях превращаются в фиксированные макрофаги, гистиоциты, остеокласты соединительной ткани, клетки нейромикроглии. Моноциты отличаются высокой подвижностью, адгезивностью, цитотоксичностью (особенно в отношении опухолевых и чужеродных клеток).
Период пребывания моноцитов в крови составляет около 2–3 суток. В тканях они живут около двух месяцев, иногда в течение многих месяцев и даже лет. В тканях их примерно в 25 раз больше, чем в циркулирующей крови. Наибольшее их количество определяется в легких и селезенке.
Моноциты – многофункциональные жизненно важные клетки организма. Они синтезируют и выделяют во внутренние среды организма различные ФАВ и, прежде всего, интерлейкины: 1, 12, 15; α- и β-интерфероны; факторы роста гепатоцитов, фибробластов; гемопоэтические факторы роста; факторы некроза опухоли и другие.
Моноцитам принадлежит важнейшая роль в обеспечении специфического и неспецифического клеточного и гуморального видов иммунитета, особенно в кооперации с Т- и В-лимфоцитами. Среди клеток крови моноциты занимают центральное положение в обеспечении адаптации и резистентности организма при действии на него разнообразных повреждающих факторов. Последнее достигается, главным образом, благодаря высокой их фагоцитарной, бактерицидной, цитотоксической, цитостатической и другими видами активности. Моноциты принимают участие в регуляции эритро- и лимфопоэза.
Моноциты образуют ограничивающий вал вокруг инородных тел, вокруг очага воспаления, очищают очаг воспаления.
Лимфоциты образуются из клетки-предшественницы лимфопоэза, которая берет свое начало от родоначальной клетки – стволовой клетки костного мозга. Далее лимфоциты образуются не только из лимфоидных клеток белого ростка красного костного мозга, но, главным образом, из лимфоидной ткани (вилочковой железы – тимуса, селезенки, лимфатических узлов, миндалин, пейеровых бляшек, червеобразного отростка - аппендикса).
Различают две основные группы лимфоцитов: Т-лимфоциты (тимус-зависимые) и В-лимфоциты (тимус-независимые).
Т- и В-лимфоциты могут быть нескольких типов:
§ Т-киллеры (цитотоксические клетки, убийцы, лизирующие чужеродные и патологически измененные собственные клетки);
§ Т-хелперы (помощники, способные распознавать антигены и стимулировать В-лимфоциты в сторону повышения последними продукции антител);
§ Т-супрессоры (клетки, угнетающие активность В-лимфоцитов, в частности, приводящие к торможению выработки последними антител);
§ Т-клетки памяти и В-клетки памяти.
По размерам и степени зрелости различают несколько видов лимфоцитов: малый лимфоцит, диаметром 5–8 мкм, средний лимфоцит, диаметром 8–12 мкм, большой лимфоцит, диаметром 12–15 мкм.
По продолжительности жизни в организме эти клетки резко отличаются друг от друга. Различают: короткоживущие клетки (продолжительность жизни колеблется от 1–2 дней до 1–2 недель) и длительноживущие клетки – клетки памяти (продолжительность жизни колеблется от 1 до нескольких лет, десятков лет и даже всей жизни).
Лимфоциты относятся к единственным среди клеток крови, которые постоянно мигрируют между кровью, тканями, лимфой, т. е. неоднократно рециркулируют в организме. Последнее обстоятельство обеспечивает более быстро наступающий и длительно сохраняющийся контакт лимфоцитов с антигенами.
На поверхности лимфоцитов имеется много различных рецепторов, чувствительных к ФАВ, гормонам и антигенам. Под влиянием последних у лимфоцитов может измениться способность к митотическому делению, к синтезу РНК, ДНК, ферментов, белков, лимфокинов.
Т-лимфоциты ответственны, главным образом, за обеспечение клеточного (специфического и неспецифического) иммунитета. В-лимфоциты – за формирование гуморального (специфического и неспецифического) иммунитета. Эти основные популяции клеток крови кооперируются между собой и с макрофагами, и совместно обеспечивают иммунный ответ организма.
Лимфоциты способны синтезировать и выделять во внутреннюю среду организма различные ФАВ и, прежде всего, лимфокины (α- и γ-интерфероны; интерлейкины: 2, 3, 4, 5, 6, 9, 10. 13, 14; лимфотоксины; фактор роста В-лимфоцитов; гемопоэтический фактор роста; онкостатин и другие), обладающие разнообразным физиологическим и метаболическим действием. Лимфокины способны как активировать, так и угнетать функции не только самих лимфоцитов, но и моноцитов, и гранулоцитов, и других клеток организма.
Под термином лейкоцитарная формула понимается процентное соотношение отдельных видов лейкоцитов в крови.
Важное физиологическое и диагностическое значение, помимо общего количества лейкоцитов, имеет именно соотношение отдельных форм (видов) лейкоцитов в крови.
Различают следующие соотношения между различными видами лейкоцитов: соотношение процентное (или относительное) и соотношение абсолютное.
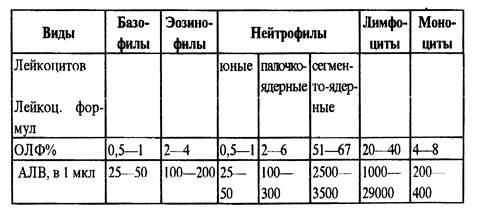
В связи с этим различают относительную и абсолютную лейкоцитарную формулу (соответственно, ОЛФ и АЛФ). У взрослого человека в норме ОЛФ в %, а также АЛФ (при числе лейкоцитов в крови 5×103 в мкл) равна следующим значениям:
Таблица 2
|
Если при анализе лейкоцитарной формулы обнаруживается увеличение молодых форм нейтрофилов - это состояние характеризуется как сдвиг лейкоцитарной формулы влево. Отсутствие молодых форм нейтрофилов или увеличение зрелых форм нейтрофилов - это состояние характеризуется как сдвиг лейкоцитарной формулы вправо. Сдвиг лейкоцитарной формулы влево происходит при острых воспалительных процессах. При аллергиях (бронхиальная астма, сенная лихорадка) и глистных инвазиях наблюдается эозинофилия. Для вялотекущих хронических заболеваний (ревматизм, туберкулез) характерно увеличение количества лимфоцитов (лимфоцитоз).
Лейкоцитарная формула у здорового человека подвержена определенным колебаниям, зависящим от различных внешних и внутренних факторов (сезон года, время суток, погодно-климатическое состояние, магнитные бури, солнечная инсоляция, радиация, возраст, реактивность организма). Однако, более существенные изменения лейкоцитарной формулы с определенными ядерными сдвигами нейтрофилов обнаруживаются в условиях патологии.