Применение CPAP и неинвазивной ИВЛ в терапии РДС новорожденных
В качестве оптимального стартового метода неинвазивной ресираторной поддержки, в особенности после введения сурфактанта и\или после экстубации в настоящее время используется неинвазивная ИВЛ, осуществляемая через назальные канюли или назальную маску. Использование неинвазивной ИВЛ после экстубации в сравнении с СРАР, а так же после введения сурфактанта приводит к меньшей потребности в реинтубации, меньшей частоты развития апноэ (В).
Неинвазивная назальная ИВЛ имеет преимущество перед СРАР в качестве стартовой респираторной терапии у недоношенных с очень и экстремально низкой массой тела.
Показания:
- В качестве стартовой респираторная терапия после профилактического малоинвазивного введения сурфактанта без интубации
- В качестве респираторной терапии у недоношенных после экстубации (в том числе и после использования метода INSURE).
- возникновение апноэ, резистентных к терапии СРАР и кофеином
- Нарастание дыхательных нарушений до 3х и более баллов по шкале Сильвермана и/или увеличение потребности в Fio2 > 0,4 у недоношенных на СРАР.
Противопоказания:
Шок, судороги, легочное кровотечение, синдром утечки воздуха, срок гестации более 35 недель.
Стартовые параметры:
Pip 8-10см Н2О; Peep 5-6 см Н2О;
Частота 20-30 в минуту; Время вдоха 0,7-1,0 секунда; Снижение параметров:
При использовании неинвазивной ИВЛ для терапии апноэ – производится снижение частоты искусственных вдохов.
При использовании неинвазивной ИВЛ для коррекции дыхательных нарушений – производится снижение Pip.
И в том и в другом случае осуществляется перевод с неинвазивной ИВЛ на СРАР с дальнейшим переводом на дыхание без респираторной поддержки.
Показания для перевода с неинвазивной ИВЛ на традиционную ИВЛ:
PaCO2 > 60 мм рт.ст. FiО2 ≥ 0,4
Оценка по шкале Сильверман 3 и более баллов. Апноэ, повторяющиеся более 4 раз в течение часа.
Синдром утечки воздуха, судороги, шок, легочное кровотечение.
При отсутствии в стационаре аппарата неинвазивной ИВЛ в качестве стартового метода неинвазивной респираторной поддержки предпочтение отдается методу спонтанного дыхания под постоянным положительным давлением в дыхательных путях через назальные канюли. У глубоко недоношенных новорожденных использование устройств СРАР с вариабельным потоком имеет некоторое преимущество перед системами с постоянным потоком, как обеспечивающие наименьшую работу дыхания у таких пациентов.
Канюли для проведения СРАР должны быть максимально широкие и короткие (А). Респираторная поддержка методом СРАР у детей с ЭНМТ осуществляется на основании алгоритма, представленного ниже.
Определение и принцип действия. СРАР – continuous positive airway pressure - постоянное (т.е. непрерывно поддерживаемое) положительное давление в дыхательных путях. Препятствует спаданию альвеол на выдохе и развитию ателектазов. Постоянное положительное давление увеличивает функциональную остаточную емкость легких (ФОЕ), снижает резистентность дыхательных путей, улучшает растяжимость легочной ткани, способствует стабилизации и синтезу эндогенного сурфактанта.
Может являться самостоятельным методом респираторной поддержки у новорожденных с сохраненным спонтанным дыханием.
Показания у новорождённых с РДС к поддержке спонтанного дыхания с помощью назального CPAP:
· Профилактически в родильном зале у недоношенных детей с гестационным возрастом 32 недели и менее.
· Оценка по шкале Сильвермана 3 и более баллов у детей гестационного возраста старше 32 недель с самостоятельным дыханием.
К противопоказаниям относят:
Шок, судороги, легочное кровотечение, синдром утечки воздуха.
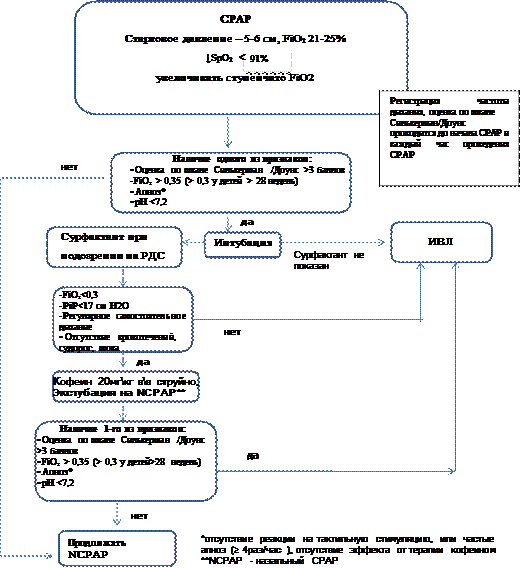
На рисунке (2) представлен алгоритм использования метода СРАР у новорожденных в условиях отделения реанимации и интенсивной терапии новорожденных [26].
|
Рис. 2 Алгоритм применения CPAP в ОРИТН:
 |
Осложнения CPAP.
1. Синдром утечки воздуха.
Профилактикой этого осложнения является как своевременное снижение давления в дыхательных путях при улучшении состояния пациента, так и своевременный переход на ИВЛ при ужесточении параметров СРАР.
2. Баротравма пищевода и желудка.
Редко встречающееся осложнение, возникающее у недоношенных при неадекватной декомпрессии. Использование желудочных зондов с большим просветом позволяет предотвратить данное осложнение.
3. Некроз и пролежни носовой перегородки.
При правильном наложении назальных канюль и правильном уходе это осложнение встречается крайне редко.
Практические советы по уходу за ребенком, находящимся на CPAP и на неинвазивной ИВЛ:
1. Необходимо использовать носовые канюли соответствующего размера для предотвращения потери положительного давления.
2. Шапочка должна закрывать лоб, уши и затылок.
3. Ленточки, фиксирующие носовые канюли, должны крепиться на шапочке сзади- наперед, чтобы было удобнее усиливать или ослаблять крепление.
4. У детей массой тела менее 1000 г. между щекой и фиксирующей лентой необходимо подкладывать мягкую прокладку (можно вату).
5. Канюли должны плотно входить в носовые отверстия и держаться без всякой поддержки. Они не должны давить на носовую перегородку ребенка.
6. В процессе лечения иногда приходится переходить на канюли большего размера в связи с увеличением диаметра наружных носовых ходов и невозможностью поддерживать в контуре устойчивое давление.
7. Нельзя санировать носовые ходы из-за возможной травматизации слизистой и быстрого развития отека носовых ходов. Если в носовых ходах имеется отделяемое, то нужно по 0,3 мл раствора хлорида натрия 0, % влить в каждую ноздрю и санировать через рот. (Для проверки проходимости носовых ходов следует закапать по 1-2 капли раствора хлорида натрия 0, % в каждую ноздрю. При нормальной проходимости физиологический раствор уходит в носоглотку легко, без препятствий.)
8. Температура увлажнителя устанавливается 37о С.
9. Пространство за ушами следует ежедневно осматривать и протирать влажной салфеткой.
10. Пространство около носовых отверстий должно быть сухим во избежание воспаления.
11. Носовые канюли следует менять ежедневно.
12. Камера увлажнителя и контур должны меняться еженедельно.
В качестве простого, но эффективного метода неинвазивной респираторной поддержки, который может являться альтернативой СРАР у недоношенных с легким и среднетяжёлым течением РДС, используется респираторная терапия с помощью высокопоточных назальных канюль. Это устройство представляет из себя контур с назальными канюлями, флоуметром, увлажнителем, баней и блендером. Устройство создает постоянное положительное давление в дыхательных путях за счет высокого потока газовой смеси. Обычно устанавливается скорость потока 2-4 л\минуту детям с ЭНМТ и 4-6 л детям с большей массой тела. Минусом такой системы является с одной стороны риск высокого непреднамеренного Реер (при потоке более 2 л/мин), а с другой – невозможность измерить давление в дыхательных путях у ребенка. В настоящий момент проводятся исследования по уточнению эффективности и безопасности этого метода у недоношенных с течением РДС.
Традиционная ИВЛ:
Задачи традиционной ИВЛ
– протезировать функцию внешнего дыхания,
– обеспечить удовлетворительную оксигенацию и вентиляцию,
– минимизировать поврежение легких
Показание для традиционной ИВЛ:
- Оценка по шкале Сильвермана 3 и более баллов у детей на неинвазивной ИВЛ/СРАР
- Потребность в высоких концентрациях кислорода у новорожденных, находящихся на СРАР/неинвазивной ИВЛ (FiO2 > 0,4)
- Шок, выраженные генерализованные судороги, частые (более четырех в час) апноэ на неинвазивной респираторной терапии, легочное кровотечение.
Проведение ИВЛ у недоношенных с РДС основано на концепции минимальной инвазивности, включающей в себя два положения: первое – использование стратегии «защиты легких», а второе – по возможности быстрый перевод на неинвазивную респираторную терапию.
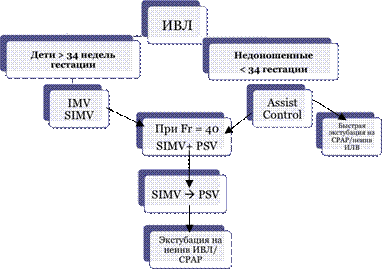
Стратегия «защиты легких» заключается в поддержании альвеол в расправленном состоянии на всем протяжении дыхательной терапии. С этой целью устанавливается Реер 4-5 см Н2О. Второй принцип стратегии «защиты легких» заключается в дотации минимально достаточного дыхательного объема, что предотвращает волютравму. Для этого следует подбирать пиковое давление под контролем дыхательного объема. Для корректной оценки используется дыхательный объем выдоха, так как именно он участвует в газообмене. Пиковое давление у недоношенных новорожденных с РДС подбирается таким образом, чтобы дыхательный объем выдоха был 4-6мл/кг. На рисунке 4 продемонстрирован алгоритм проведения ИВЛ и выбора режима вентиляции в зависимости от гестационного возратса.
Рисунок 4. Алгоритм проведения ИВЛ у новорожденных с РДС
 |
После установки дыхательного контура и калибровки аппарата ИВЛ следует выбрать режим вентиляции.
У недоношенных новорожденных, у которых сохранено самостоятельное дыхание, предпочтительно использовать триггерную ИВЛ, в частности, режим assist/control. В этом режиме каждый вдох будет поддерживаться респиратором. Если самостоятельное дыхание отсутствует, то режим А/С автоматически становится режимом принудительной вентиляции
— IMV при установке определенной аппаратной частоты дыхания.
В редких случаях режим А/С может оказываться избыточным для ребенка, когда несмотря на все попытки оптимизировать параметры, ребенок имеет стойкую гипокапнию в связи тахипноэ. В этом случае можно перевести ребенка в режим SIMV и установить
желаемую частоту респиратора. У новорожденных, родившихся на 35 неделе гестации и более целесообразно использовать режим принудительной вентиляции в остром периоде (IMV) или SIMV, если тахипноэ не выражено.
Имеются данные о преимуществе использования режимов ИВЛ с контролем по объему в сравнении с более распространенными методами ИВЛ с контролем по давлению
[14] (B)
После того как режимы выбраны, до подключения ребенка к аппарату устанавливаются стартовые параметры ИВЛ.
Стартовые параметры ИВЛ у маловесных пациентов: FiO2 – 0,3-0,4 (обычно на 5-10% больше чем при СРАР);
Тin – 0,3-0,4 сек; РееР— +4-5смвод.ст.;
ЧД — В режиме assist/control (A/C) частота дыхания определяется пациентом.
Аппаратная частота устанавливается 30-35 и является лишь страховкой на случай апноэ у пациента.
В режиме SIMV и IMV устанавливается частота физиологическая – 40-60 в минуту. Pip обычно устанавливается в диапазоне 14-20 см вод. ст.
Поток – 5-7 л/минуту при использовании режима «pressure limited». В режиме «pressure control» поток устанавливается автоматически.
После подключения ребенка к аппарату ИВЛ проводится оптимизация параметров:
FiO2 устанавливается таким образом, чтобы уровень сатурации был в пределах 1-
5%. При наличии в аппарате ИВЛ функции автоматического подбора FiO2 в зависимости от уровня сатурации у пациента, ее целесообразно использовать для профилактики гипоксических и гипероксических пиков, что в свою очередь является профилактикой развития бронхолегочной дисплазии, ретинопатии недоношенных, а так же структурных геморрагических и ишемических повреждений головного мозга.
Время вдоха является динамическим параметром. Время вдоха зависит от нозологической формы заболевания, его фазы, частоты дыхания самого пациента и некоторых других факторов. Поэтому при использовании привычной тайм-циклической вентиляции время вдоха желательно устанавливать под контролем графического мониторинга кривой потока (см. рис. 5)
Рис.5
Подбор времени вдоха по кривой потока:
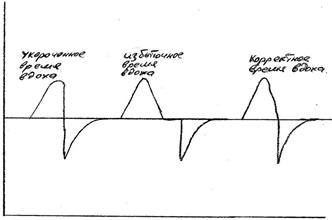 |
Устанавливать время вдоха следует так, чтобы на кривой потока выдох являлся бы продолжением вдоха. Не должно быть паузы вдоха в виде задержки кривой на изолинии, и в то же время выдох не должен начинаться раньше, чем закончится вдох. при использовании вентиляции, цикличной по потоку время вдоха будет определяться самим пациентом в случае наличия у ребенка самостоятельного дыхания. Такой подход имеет некоторое преимущество, так как позволяет организму глубоко недоношенному пациенту самому определять комфортное время вдоха. В этом случае время вдоха будет варьировать в зависимости от частоты дыхания пациента, его инспираторной активности. Вентиляция, цикличная по потоку, может использоваться в ситуациях, когда у ребенка присутствует самостоятельное дыхание, нет выраженной экссудации мокроты и отсутствует склонность к ателектазированию.
При проведении вентиляции, цикличной по потоку, необходимо мониторировать фактическое время вдоха пациента. В случае формирования неадекватно короткого временя вдоха, такой пациент должен быть переведен в режим тайм-циклической ИВЛ и вентилироваться с заданным, фиксированным временем вдоха.
Подбор Pip проводится таким образом, чтобы дыхательный объем выдоха был в диапазоне 4-6 мл/кг. При наличии в аппарате ИВЛ функции автоматического подбора пикового давления в зависимости от дыхательного объема пациента, ее целесообразно использовать у тяжело больных пациентов с целью профилактики ИВЛ ассоциированного повреждения легких.
Синхронизация ребенка с аппаратом ИВЛ
Рутинная медикаментозная синхронизация с респиратором приводит к худшим неврологическим исходам в сравнении с проведением ИВЛ без рутинной медикаментозной седацией (В). В этой связи необходимо стараться синхронизировать пациента с аппаратом ИВЛ адекватным подбором параметров. Подавляющее большинство пациентов, родившихся с экстремально и очень низкой массой тела, при правильно проводимой искусственной вентиляции не требуют медикаментозной синхронизации с аппаратом ИВЛ. Как правило, новорожденный форсированно дышит или «борется» с респиратором, если аппарат ИВЛ не обеспечивает ему адекватную минутную вентиляцию. Как известно, минутная вентиляция равна произведению дыхательного объема на частоту. Таким образом, синхронизировать пациента с аппаратом ИВЛ можно, увеличив частоту респиратора или дыхательный объем (Piр), в случае если последний не превышает 6 мл/кг. Выраженный метаболический ацидоз также может являться причиной форсированного дыхания, что требует коррекции ацидоза, а не седации пациента. Исключением могут являться структурные церебральные повреждения, при которых одышка имеет центральный генез. Если регулировкой параметров не удается синхронизировать ребенка с респиратором, назначают обезболивающие и седативные препараты – морфин, фентанил, диазепам в стандартных дозах. В таблице 5 представлена схематичная регулировка параметров в зависимости от газового состава крови новорожденных.








