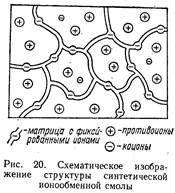
Ионообменная хроматография
В основе метода лежит обратимый стехиометричнский обмен ионов, содержащихся в растворе, на подвижные ионы ионитов (ионообменников).
Разделение смеси ионов связано с неодинаковой способности к обмену.
В ионообменной хроматографии элюент – раствор электролита.
По типу заряда иониты делятся на:
-катиониты
-аниониты
амфолиты – обмен катионов и анионов.

Катионный обмен
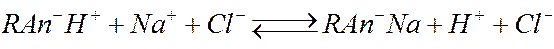
Анионный обмен
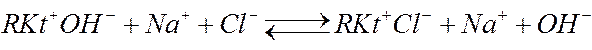
Обменная емкость ионитаz
Полная обменная емкость является постоянной величиной и определяется числом фиксированных групп.
Обменная емкость, определяемая в статических условиях отличается от величины, полученной в динамических условиях.
В динамических условиях ДОЕ (до проскока) и ПДОЕ (по полному прекращению извлечения ионов) 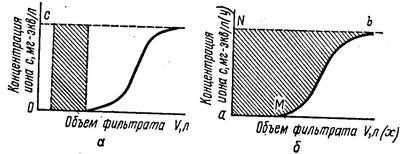
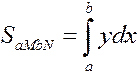
Ионообменное равновесие
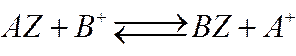
по закону действующих масс
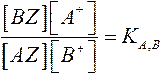
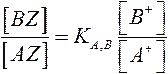
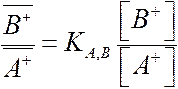
при обмене 2-хвалентного иона
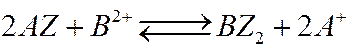
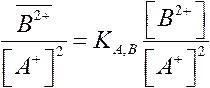
уравнение Никольского
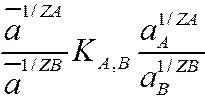 г де
г де 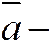 активности в ионите,
активности в ионите,
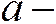 активности в растворе
активности в растворе
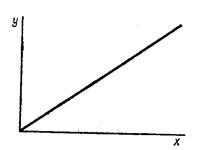 1
1
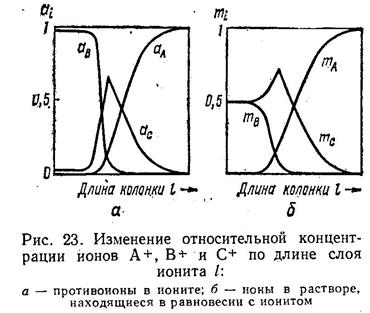
Динамика ионного обмена
Пусть Кав=100 а Кас=1
Методы ионообменной хроматографии
фронтальный
для очистки или извлечения примесей
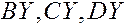
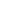
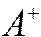 - противоион
- противоион
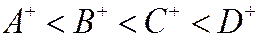
Общая концентрация вытекающего раствора (в эквивалентах) всегда остается постоянной
Вытеснительный
Противоион 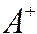
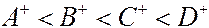
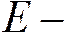 вытеснитель
вытеснитель
Проявительный
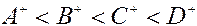
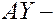 подвижная фаза
подвижная фаза
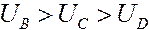
Иониты
1) минеральные иониты – цеолиты
2) синтетические неорганические ионы
а) плавленные пермутиты
б) гелеобразные пермутиты
3) иониты на основе углей
4) иониты на основе синтетических смол
У катионов фиксированные группы
у анионов
Матрица ионита гидрофобна, введение фиксированных ионов означает введение в гидрофобную матрицу гидрофильных групп, вследствие этого матрица приобретает способность к набуханию, смола превращается в полиэлектролит.
В основу классификации ионитов Никольский положил их отношение к
рН – для катионитов
рОН – для анионитов
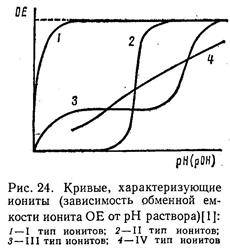

I тип – свойства сильных кислот или сильных оснований
КУ-2, КУ-3, СОВ-2
II тип – свойства слабых кислот и слабых оснований
фиксированные группы –
III тип – смешанного типа
(сильная кислота, слабая кислота)
КУ-1
IV – тип – подобно смеси многих кислот или многих оснований
почвы, гли








