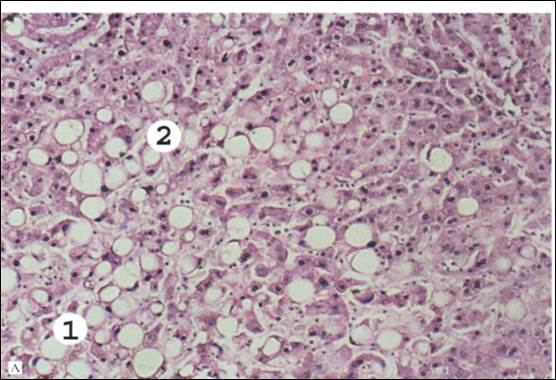
Рис. 1. Белковые гиалиновые капли в эпителии проксимальных извитых канальцев почки.
В цитоплазме клеток эпителия извитых канальцев видны крупные гиалиноподобные капли, окрашенные эозином в розовый цвет (1). Эпителиальные клетки увеличены в объеме, границы нечеткие; просветы канальцев сужены, в них встречаются белковые преципитаты
Гиалиново-капельная дистрофия печени возникает в гепатоцитах при остром алкогольном гепатите (реже при первичном билиарном циррозе, холестазе и некоторых других заболеваниях печени). Гиалиноподобные включения (при исследовании в световом микроскопе напоминают гиалиново-капельную дистрофию, в электронном микроскопе представлены фибриллярным белком), носят название алкогольного гиалина, или телец Мэллори. Эти тельца располагаются обычно перинуклеарно в виде ацидофильных глыбок или сетчатых масс. Основной механизм данной дистрофии- это извращенный синтез. Алкогольный гиалин определяет ряд реакций как в печени, так и за ее пределами, что обусловлено рядом его свойств. Он обладает хемотаксическими свойствами и определяет прежде всего лейкотаксис. Поэтому он окружен, как правило, полиморфно-ядерными лейкоцитами (характерный признак острого алкогольного гепатита).
Алкогольный гиалин оказывает цитолитическое действие на гепатоциты, с чем связано развитие в печени своеобразного «склерозирующего гиалинового некроза», и коллагеностимулирующее действие, определяя хроническое прогрессирующее течение алкогольного гепатита и развитие цирроза печени.
2.1.3. При гидропической дистрофии дистрофии макроскопически органы не изменяются. Микроскопически в цитоплазме клетки появляются вакуоли. Гидропическая дистрофия может завершиться развитием баллонной дистрофии (фокальный колликвационный некроз) и смертью клетки (тотальный колликвационный некроз). Гидропическая дистрофия встречается в основном в печени и почках, иногда в эпидермисе. Гидропическая дистрофия в почках (рис. 2) 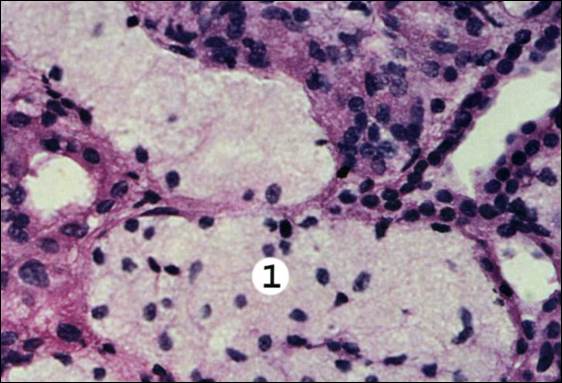
Рис. 2. Гидропическая дистрофия эпителия проксимальных извитых канальцев почки.
Набухание и вакуолизация цитоплазмы клеток эпителия проксимальных извитых канальцев (1). Ядра смещены к базальной мембране клеток, бледно окрашены. Просветы канальцев сужены, отмечается слущивание эпителия.
развивается также при нефротическом синдроме. Гидропическая дистрофия эпителия канальцев почек при нефротическом синдроме возникает при повреждении различных мембранно-ферментных систем, ответственных за реабсорбцию белка и воды.
Гидропическая дистрофия нефроцитов связана с механизмами инфильтрации и декомпозиции системы реабсорции – базального лабиринта, работающего на натрий-калий -зависимых АТФ-азах и обеспечивающего реабсорбцию натрия и воды.
Гидропическая дистрофия печени (рис. 3) возникает при вирусных гепатитах В и С и отражает извращение белково-синтетической функции гепатоцита вследствие репродукции вируса.
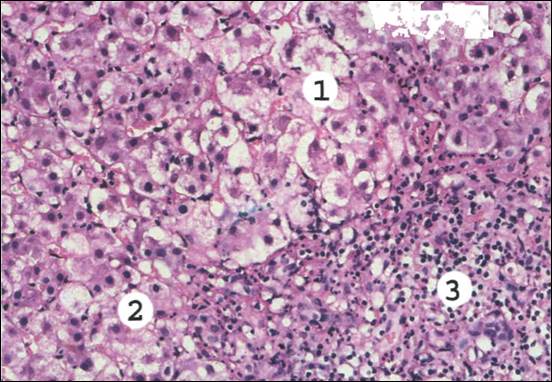
Рис. 3. Острый вирусный гепатит.
Дискомплексация печеночных балок, гепатоциты в состоянии гидропической и баллонной дистрофии (7), местами виден колликваиионный некроз гепатоцитов. Встречаются тельца Каунсильмена (уменьшенные в размерах гепатоциты с эозинофильной цитоплазмой и пикнотичным. ядром) (2). В портальных трактах и дольках небольшой лимфогистиоцитарный инфильтрат
При этом в гепатоцитах образуются крупные светлые капли, часто заполняющие всю клетку (баллонная дистрофия). При оценке гидропической дистрофии гепатоцитов следует руководствоваться морфологическим анализом особенностей функционирования печеночных клеток, обеспечивающих специализированные функции органа.
Известно, что для выполнения белковосинтетической и антитоксической функции гепатоциты детерминированы структурно; темные гепатоциты периферии долек богаты ультраструктурами синтеза, светлые гепатоциты центров долек – ультраструктурами детоксикации и гидролиза.
При воздействии на печень вируса гепатита В избирательно реагируют темные, а токсических веществ – светлые гепатоциты. При этом дистрофия их отражает разные по своей сути процессы: гидропическая дистрофия темных гепатоцитов – извращенную белковосинтетическую функцию, подчиненную репродукции вируса, та же гидропическая дистрофия светлых гепатоцитов – недостаточность системы детоксикации.
Гидропическая дистрофия в эпидермисе может обнаружиться при ожогах и натуральной оспе.
2.1.4. Роговая дистрофия, или патологическое ороговение, характеризуется избыточным образованием рогового вещества в ороговевающем эпителии (рис. 4) (гиперкератоз, ихтиоз) или образованием рогового вещества там, где в норме его не бывает (патологическое ороговение на слизистых оболочках, или лейкоплакия; образование «раковых жемчужин» в плоскоклеточном раке (рис. 5). Процесс может быть местным или распространенным. Причины роговой дистрофии разнообразны: нарушение развития кожи, хроническое воспаление, вирусные инфекции, авитаминозы и др.
Исход может быть двояким: устранение вызывающей причины в начале процесса может привести к восстановлению ткани, однако в далеко зашедших случаях наступает гибель клеток.
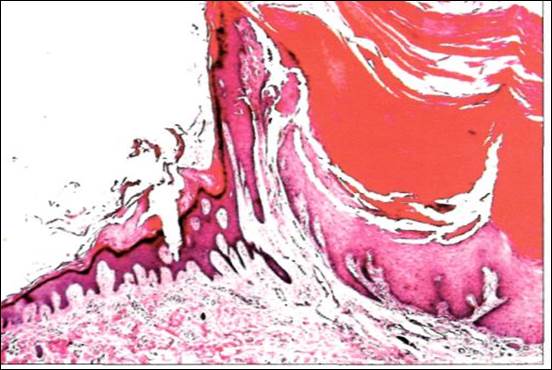
Рис. 4. Кожный рог. Гиперкератоз.
Кожный рог.-это палочковидное образование длиной до 2-3см. Чаще возникает на лице или волосистой части головы
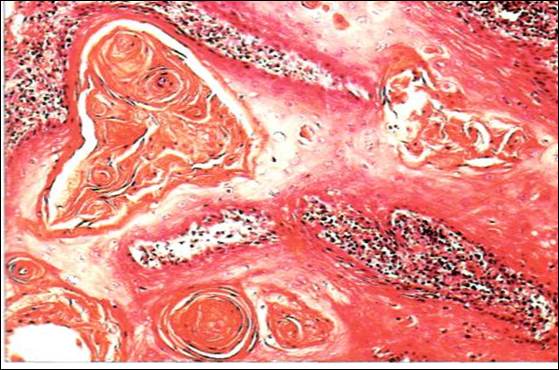
Рис. 5. Плоскоклеточный рак. Раковые жемчужины
Значение роговой дистрофии определяется ее степенью, распространенностью и длительностью. Длительно существующее патологическое ороговение слизистой оболочки" (лейкоплакия) может явиться источником развития раковой опухоли.
Роговые дистрофии подразделяются на наследственные и приобретенные, общие и местные.
К наследственной общей роговой дистрофии относится ихтиоз, который наиболее часто встречается среди группы болезней, протекающих нарушением процессов кератинизации.
Ихтиоз обычный - наиболее часто встречающаяся форма заболевания (рис . 6), наследуется по аутосомно-доминантному типу.
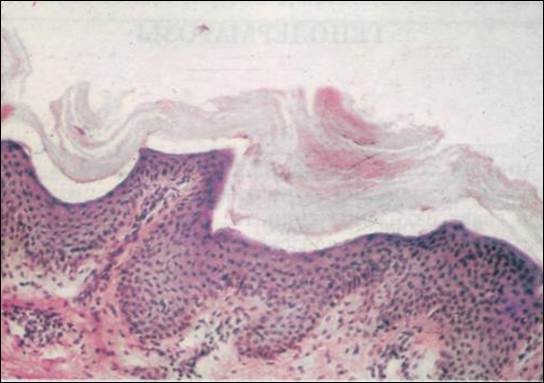
Рис. 6. Ихтиоз обычный.
Гиперкератоз, истончение шиповатого слоя на вершине сосочков дермы, отсутствие зернистого слоя
Клинически обычно проявляется к концу первого года жизни сухостью кожи, фолликулярным кератозом, шелушением с наличием светлых плотно прикрепленных полигональных чешуек, напоминающих "рыбью чешую". Воспалительные явления отсутствуют.
Поражаются преимущественно разгибательные поверхности конечностей, спина, в меньшей степени — живот, в складках кожи изменения отсутствуют.
Врожденный ихтиоз резкой степени, как правило, несовместим с жизнью
Кожа ладоней и подошв из-за усиления папиллярного рисунка и углубления кожных складок выглядит старческой
При микроскопическом исследовании характерны гиперкератоз, истончение или отсутствие зернистого, истончение шиповатого слоев эпидермиса. Гиперкератоз часто распространяется и на устья волосяных фолликулов, что клинически проявляется фолликулярным кератозом.
Шиповатый слой — с признаками небольшой атрофии, состоит из мелких, атрофичных эпителиоцитов или, напротив, крупных клеток с явлениями вакуолизации. В базальном слое иногда увеличено количество меланина.
Ихтиоз, сцепленный с Х- хромосомой. (син. icthyosis nigricans), встречается с частотой 1:6000 улиц мужского пола, тип наследования рецессивный, сцепленный с полом.
Типичная клиническая картина наблюдается только у мужчин. Может существовать с рождения, но чаще появляется в первые недели или месяцы жизни. Кожа покрыта буроватыми, плотно прикрепленными толстыми чешуйками, локализующимися главным образом на передней поверхности туловища, голове, шее, сгибательной и разгибательной поверхностях конечностей. Нередко поражение кожи сопровождается помутнением роговицы, гипогонадизмом, крипторхизмом.
В отличие от обычного ихтиоза отмечается более раннее начало заболевания, отсутствуют изменения ладоней и подошв, поражаются складки кожи, проявления заболевания более выражены на сгибательных поверхностях конечностей и на животе. Как правило, отсутствует фолликулярный кератоз.
Основным гистологическим признаком является гиперкератоз (рис.7) с нормальным или слегка утолщенным зернистым слоем. Роговой слой массивный, сетчатого строения, местами во много раз толще нормального.
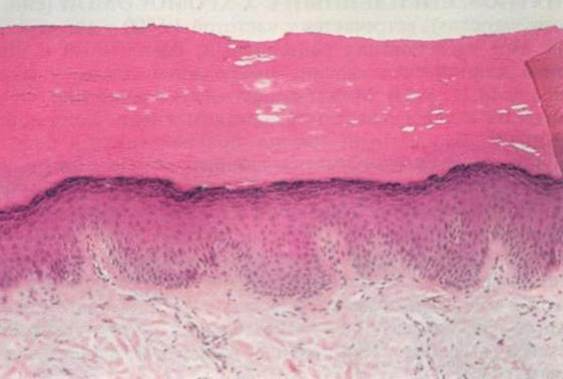
Рис. 7. . Ихтиоз, сцепленный с Х- хромосомой
Выраженный гиперкератоз с нормальным или слегка утолщенным зернистым слоем. Роговой слой массивный, сетчатого строения, местами во много раз толще нормального.
2.2. ЖИРОВАЯ ДИСТРОФИЯ.
Существует два вида жиров. Количество подвижных (лабильных) жиров меняется на протяжении всей жизни человека. Они локализуются в жировых депо. Стабильные (неподвижные) жиры включены в состав клеточных структур и мембран.
Жиры определяются при помощи специальных красителей:
1) Судан – III обладает способностью окрашивать жир в оранжево- красный цвет;
2) Шарлах окрашивает в красный цвет;
3) Судан – IV (осмиевая кислота) окрашивает жир в черный цвет;
4) Нильская голубая имеет метахромазию: она окрашивает нейтральные жиры в красный, а все остальные жиры под ее воздействием приобретают синий или голубой цвет.
Причины жировой дистрофии можно разделить на две основные группы: инфекции и интоксикации. В наше время основным видом хронической интоксикации является алкогольная интоксикация. Нередко могут наблюдаться медикаментозные интоксикации, эндокринные интоксикации – развивающиеся при сахарном диабете.
Паренхиматозная жировая дистрофия наиболее часто встречается в печени, миокарде и почках.
О жировой дистрофии печени, которая по сравнению другими липидозами паренхиматозных органов встречается особенно часто, говорят в тех случаях, когда жир, преимущественно нейтральный, содержит более 50 % гепатоцитов. Выделяют три стадии жировой печени: "чистая" жировая печень, жировая печень с мезенхимальной реакцией, фиброз и цирроз печени.
Непосредственной причиной накопления нейтральных жиров в печени является дезорганизация ферментативных процессов на том или ином этапе обмена липидов, которая проявляется в следующих ситуациях:
1) при чрезмерном поступлении в клетку жирных кислот или повышенном их синтезе в гепатоците, что создает относительный дефицит ферментов;
2) при воздействии на клетку токсичных веществ, блокирующих окисление жирных кислот, синтез апопротеинов;
3) при недостаточном поступлении в гепатоциты аминокислот, необходимых для синтеза фосфолипидов и липопротеидов.
Из сказанного следует, что жировая дистрофия печени может развиваться в следующих случаях:
1) при состояниях, для которых характерен высокий уровень жирных кислот в плазме крови — алкоголизм, сахарный диабет, общее ожирение и др.;
2) при воздействии на гепатоциты токсичных веществ — этанола, четыреххлористого углерода, фосфора и др.;
3) при нарушении питания вследствие недостатка белка в пище (алипотропное ожирение печени) или заболеваний желудочно-кишечного тракта;
4) при генетических дефектах ферментов, участвующих в жировом обмене — наследственные липидозы.
Более подробного рассмотрения заслуживает жировая дистрофия печени при алкоголизме, сахарном диабете и интоксикациях.
Алкоголизм. Установлено, что среди других причин развития жировой печени этанолу отводится от 30 до 50 %. Этанол усиливает мобилизацию жира из депо, увеличивает синтез жирных кислот в гепатоцитах, усиливает этерификацию жирных кислот до триглицеридов, снижает уровень окисления жирных кислот, уменьшает синтез и освобождение липопротеидов, а также проницаемость клеточной мембраны гепатоцита в связи с усилением синтеза и накоплением холестерина.
Отложения жира в алкогольной печени могут быть очаговыми и диффузными. В случае диффузного ожирения алкогольная печень увеличена в размерах, дряблая, охряно-желтая.
При гистологическом исследовании в зависимости от размеров жировых капель различают мелкокапельную, среднекапелъную и крупнокапельную дистрофию гепатоцитов (рис. 8А и 8Б). При крупнокапельной жировой дистрофии — крайнем выражении дистрофии — ядро гепатоцита оттесняется к наружной мембране клетки/Ободок цитоплазмы, свободной от жировых включений, остается структурно и функционально сохранным: при электронной микроскопии органеллы его изменены мало, в нем высоки содержание гликогена, РНК и активность ферментов гликолиза, пентозного шунта, дезаминирования; достаточна и активность сукцинатдегидрогеназы.
Видимо, возможный исход алкогольной жировой печени (алкогольного стеатоза печени) объясняется тем, прекратит ли больной употребление алкоголя или будет продолжать злоупотреблять им. На основании результатов исследования повторных биоптатов печени у больных алкоголизмом показано, что при полной абстиненции жир исчезает из печени через 2—4 нед, а прогрессирование алкогольного стеатоза ведет к формированию цирроза печени, при этом большое значение имеют повторные атаки острого алкогольного гепатита.