Химические свойства глюкозы.
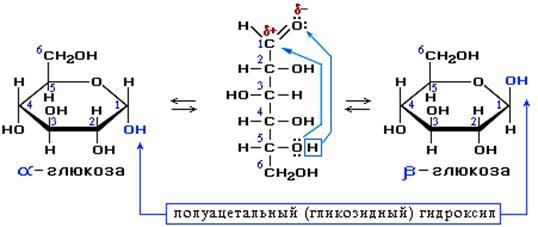
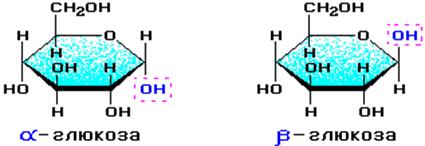
1. В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами - α и β и линейной формой:
2. Реакция комплексообразования с гидроксидом меди (II).
При взаимодействии свежеосажденного гидроксида меди (II) с моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
3. Глюкоза как альдегид.
а) реакция серебряного зеркала.
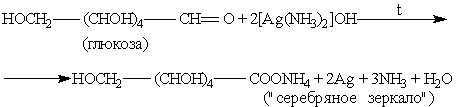
б) реакция с гидроксидом меди ( II ) при нагревании.
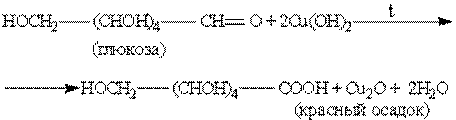
в) Глюкозу можно окислить бромной водой:
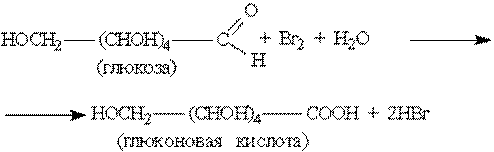
г) Каталитическое гидрирование глюкозы - происходит восстановление карбонильной группы до спиртового гидроксила, получается шестиатомный спирт – сорбит.
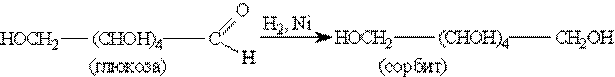
4. Реакции брожения.
а) спиртовое брожение C6H12O6 à 2C2H5OH + 2CO2
этанол
б) молочнокислое брожение
C6H12O6 à 2CH3-CH(OH)-COOH
молочная кислота
в) маслянокислое брожение
C6H12O6 à C3H7COOH + 2CO2 + 2H2O
масляная кислота
5. Реакции образования эфиров глюкозы.
Глюкоза способна образовывать простые и сложные эфиры. Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила:
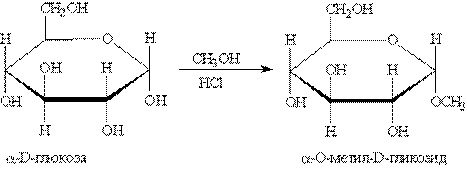
Простые эфиры получили название гликозидов.
В более жестких условиях (например, с CH 3 - I ) возможно алкилирование и по другим оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные эфиры как с минеральными, так и с карбоновыми кислотами, например:
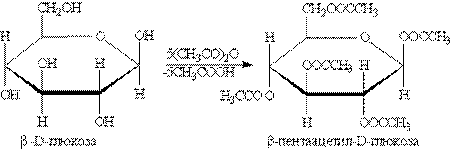
Фруктоза — структурный изомер глюкозы - кетоноспирт:
СН2- СН- СН- СН - С - СН2
| | | | ║ |
OH OH OH OH O OH
Кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза. В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы обусловлены наличием кетонной и пяти гидроксильных групп. При гидрировании фруктозы также получается СОРБИТ.
Дисахариды.
Дисахариды – это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой).
1. Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом.
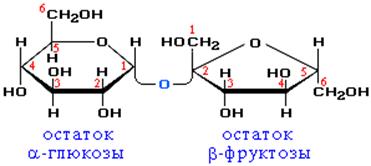
В молекуле сахарозы гликозидный атом углерода глюкозы СВЯЗАН, поэтому она не образует ОТКЫТУЮ (альдегидную) форму.
Вследствие этого сахароза не вступает в реакции альдегидной группы – с аммиачным раствором оксида серебра с гидроксидом меди при нагревании. Подобные дисахариды называют невосстанавливающими , т.е. не способными окисляться.
Сахароза подвергается гидролизу подкисленной водой:
С12Н22О11 + Н2О à С6Н12О6 (глюкоза) + С6Н12О6 (фруктоза)
2. Мальтоза.
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
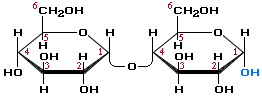
остаток α-глюкозы остаток α-глюкозы
Мальтоза - является восстанавливающим дисахаридом и вступает в реакции, характерные для альдегидов.
3. К восстанавливающим сахаром относятся также целлобиоза 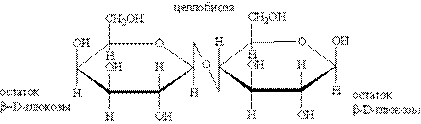
и лактоза:
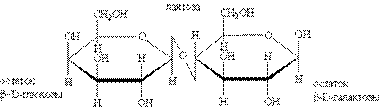
Остальные дисахариды так же могут гидролизоваться.
Полисахариды.
Полисахариды - это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители - крахмал и целлюлоза - построены из остатков одного моносахарида - глюкозы. Крахмал и целлюлоза имеют одинаковую молекулярную формулу: (C6H10O5)n, но совершенно различные свойства. Это объясняется особенностями их пространственного строения.
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы (выделена цветом):
Крахмал.
Крахмалом называется смесь двух полисахаридов, построенных из остатков циклической α-глюкозы.
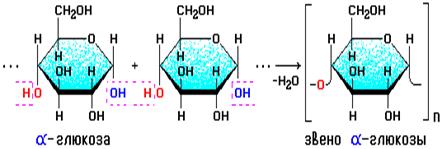
В его состав входят:
· амилоза (внутренняя часть крахмального зерна) – 10-20%
· амилопектин (оболочка крахмального зерна) – 80-90%
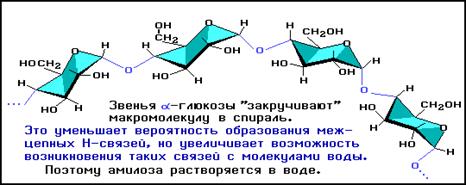 Цепь амилозы включает 200 - 1000 остатков α-глюкозы (средняя мол.масса 160 000) и имеет неразветвленное строение.
Цепь амилозы включает 200 - 1000 остатков α-глюкозы (средняя мол.масса 160 000) и имеет неразветвленное строение.
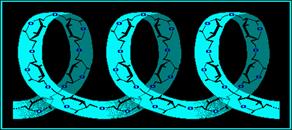
Макромолекула амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев α-глюкозы.
Свойства крахмала:
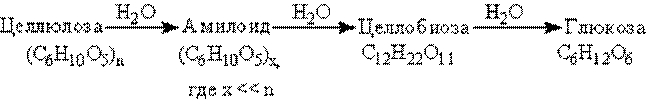
1. Гидролиз крахмала: при кипячении в кислой среде крахмал последовательно гидролизуется.
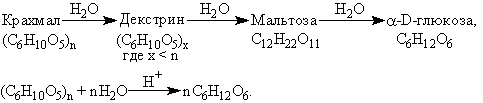
2. Крахмал не дает реакцию “серебряного зеркала” и не восстанавливает гидроксид меди (II).
3. Качественная реакция на крахмал: синее окрашивание с раствором йода.
ЦЕЛЛЮЛОЗА
Целлюлоза (клетчатка) – наиболее распространенный растительный полисахарид. Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
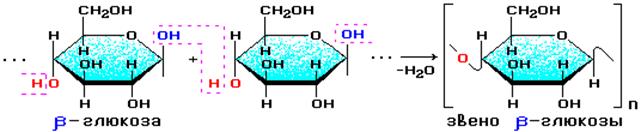
Молекулярная масса целлюлозы - от 400 000 до 2 млн.
СВОЙСТВА ЦЕЛЛЮЛОЗЫ.
1. Образование сложных эфиров с азотной и уксусной кислотами.
а) нитрование целлюлозы. Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
(С6Н7О2(ОН)3)n + 3n HNO3 à 3nH2O + (С6Н7О2(О NO 2 )3) n
целлюлоза азотная кислота тринитрат целлюлозы
(пироксилин)
б) ацилирование целлюлозы. При действии на целлюлозу уксусного ангидрида происходит реакция этерификации, при этом возможно участие в реакции 1, 2 и 3 групп ОН. Получается ацетат целлюлозы - ацетатное волокно.
(С6Н7О2(ОН)3)n +3n(СН3СО)2Оà 3n СН3-СООН + (С6Н7О2(ОСОСН3)3) n
целлюлоза уксусный ангидрид уксусная кислота триацетат целлюлозы
2. Гидролиз целлюлозы.
Целлюлоза, подобно крахмалу, в кислой среде гидролизуется: