Классификация органических соединений по углеродному скелету
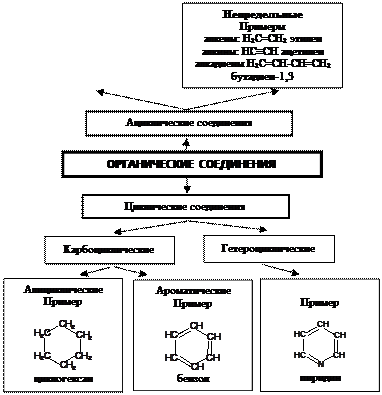 |
Органические соединения, состоящие из двух химических элементов – углерода и водорода, называют углеводородами. Метан СН4 «возглавляет» ряд углеводородов – алканов с линейным и разветвленным строением углеродных цепей, в которых углеродные атомы соединены простыми (одинарными) s-связями. Углеводороды, в которых, кроме s-связей, содержится одна двойная связь (p-связь), называются алкенами. Углеводороды, в которых, кроме s- связей, содержатся две двойные связи (p-связи), – алкадиены.
Т а б л и ц а 14
Классификация органических соединений по функциональным группам (выделены жирным шрифтом)
| Формула | Название класса | Примеры | Название по ИЮПАК* | Тривиальное название |
| R –F, Cl, Br, I | Галогенпроизводные | СНCl3 | трихлорметан | хлороформ |
| R –OH | Спирты | С2Н5ОН | этанол | этиловый спирт |
| RС6Н4 –OH | Фенолы | С6Н5ОН | фенол | фенол |
| R –O– R | Простые эфиры | С2Н5 –О–С2Н5 | диэтиловый эфир, этоксиэтан | серный эфир |
| R –NH2 | Амины | С6Н5NH2 | фениламин | анилин |
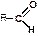
| Альдегиды |
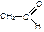
| этаналь | ацетальдегид, уксусный альдегид |
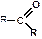
| Кетоны |
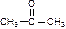
| пропанон, диметилкетон | ацетон |
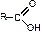
| Карбоновые кислоты |
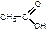
| этановая кислота | уксусная кислота |
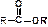
| Сложные эфиры | 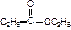
| этилацетат, этилэтаноат | этиловый эфир уксусной кислоты |
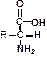
| Аминокислоты |
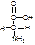
| аминоэтановая кислота | аминоуксусная кислота, глицин |
*) Правила составления названий предложены Международным союзом теоретической и прикладной химии ИЮПАК (International Union Pure and Applied Chemistry).
Существует обширная группа углеводородов – алкинов, содержащих в молекуле одну тройную связь. Среди циклических выделяют ароматические углеводороды, содержащие в молекуле одну или несколько циклических группировок, называемых бензольными кольцами, и циклические углеводороды, содержащие только s-связи (циклоалканы).
Органические соединения, молекулы которых содержат в цикле, наряду с атомами углерода, один или несколько атомов таких элементов, как азот N, кислород О и сера S, относятся к гетероциклическим соединениям. Например, гетероциклические фрагменты входят в состав многих витаминов, антибиотиков.
7.2. Нефть и природный газ
Первичная переработка нефти состоит в дистилляции, т.е. разгонке нефти на отдельные фракции, различающиеся температурой выкипания и составом входящих в состав фракции углеводородов.
Петролейный эфир – жидкая смесь углеводородов, выделяемая из нефти и кипящая при температуре до 40 0С. Смесь содержит в основном пентан С5Н10, гексан С6Н12, а также изомеры этих соединений. Используется петролейный эфир в качестве растворителя органических соединений.
Бензин – смесь углеводородов, выкипающая при разгонке нефти в интервале температур 40 – 185 оС. В бензине содержится до 70% ациклических углеводородов с преимущественным содержанием н-гептана (С7Н16) и изооктана (С8Н18):
СН3–СН2–СН2–СН2–СН2–СН2–СН3
н-гептан
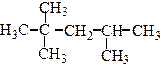
изооктан (2.2,4-триметилпентан)
и углеводородов циклического строения (~30%) с преимущественным содержанием циклогексана и метилциклогексана.
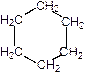
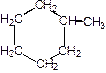
Циклогексан Метилциклогексан
Кроме того, в бензине присутствуют небольшие количества ароматических соединений, главным образом бензол и толуол.
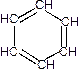
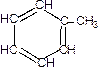
Бензол Толуол
Бензин используется не только в качестве моторного топлива. Часть бензина подвергается пиролизу для получения различных органических соединений, в том числе этилена СН2=СН2. Последний служит исходным продуктом для получения полиэтилена [СН2=СН2]n.
Пиролиз углеводородов осуществляется при высокой температуре без доступа воздуха для получения главным образом непредельных и ароматических углеводородов.
Керосин – смесь алканов и циклоалканов, выделяемая в результате перегонки нефти в интервале температур 110 – 320 оС. В состав керосина входят алканы с преимущественным содержанием углеводородов с длиной цепи от 7 до 13 атомов углерода
СН3–(СН2)n–СН3 (n = 7 – 13),
а также циклоалканы (в основном моно-, би- и полициклические соединения)
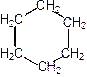
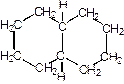 ,
,
Циклогексан Бициклодекан
и бициклические ароматические соединения, например нафталин
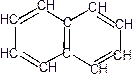 .
.
Нафталин
Керосин используется в качестве ракетного и авиационного топлива, а также для пиролитического получения непредельных углеводородов.
Дизельное топливо – смесь углеводородов, имеющая более высокую температуру выкипания при разгонке нефти (180 – 360 оС). Используется в двигателях внутреннего сгорания.
Отступление. Качество бензина и дизельного топлива оценивается способностью топлива полностью сгорать без детонации (взрывоподобного сгорания, сопровождающегося вибрацией и неустойчивой работой двигателя). Качество бензина оценивается октановым числом. По стандарту октановое число для изооктана (2,2,4-триметилпентана) принято равным 100. Для н-гептана это число равно 0. Чем выше октановое число, тем выше качество бензина. Если бензин сгорает как эквивалентная ему смесь, состоящая из 92% изооктана и 8% гептана, его октановое число равно 92. Более высокого качества бензин имеет октановое число 95.
Для дизельного топлива критерием качества является цетановое число. Оно принято равным 100 для гексадекана СН3(СН2)14СН3 (цетана). В дизельном двигателе топливо впрыскивается в момент, когда воздух сжат до давления порядка 140 атм и нагрелся при сжатии до температуры, при которой впрыск дизельного топлива сопровождается его самовоспламенением и последующим рабочим ходом поршня в блоке цилиндров. Эмпирически установлено, что лучшие характеристики топлива достигаются, когда его сгорание соответствует цетановому числу 45 – искусственной смеси, содержащей 45 % цетана и 55% a-метилнафталина.
Нефтяные масла и смолы – светлые или слегка окрашенные вязкие жидкости выделяются при разгонке нефтяных фракций, кипящих при 300 – 600 оС. Нефтяные масла (их также называют минеральными маслами) содержат смесь высокомолекулярных алканов (парафиновых углеводородов), высокомолекулярных циклоалканов (нафтеновых углеводородов), ароматических углеводородов (би-, три- и полициклических), а также металлов в составе комплексных соединений. Масла служат в основном в качестве смазочных материалов.
Нефтяные смолы существенно отличаются от минеральных масел составом. В смолах содержатся полициклические ароматические соединения, высокомолекулярные алициклические соединения, содержащие в гетероциклах такие функциональные группы, как =N–H, –S–H,
–COOH и др. Нефтяные смолы используются главным образом в качестве добавок к строительным битумам, улучшая их пластичность и адгезионные свойства.
Мазут, гудрон, битум – темно-коричневые массы. Мазут – жидкость, которая используется в основном в качестве топлива для паровых котлов. Мазут содержит нефтяные смолы, асфальтены, карбены, карбоиды и металлы (главным образом V, Ni, Fe), а также серу и азотсодержащие органические соединения.
Гудрон – вязкая жидкость черного цвета или твердая масса, образующаяся в качестве остатка в результате отгонки из нефти углеводородов, выкипающих при температурах до 600 оС (петролейный эфир, бензин, керосин, дизельное топливо, мазут). В гудроне сосредоточены высокомолекулярные алканы, циклоалканы, полициклические ароматические углеводороды и все содержащиеся в нефти металлы. Гудрон используется для пропитки бумажных материалов (пергамин, рубероид). Его применяют также при изготовлении дорожных и строительных битумов.
Битум – дисперсная система, состоящая из твердых частичек дисперсной фазы (асфальтены, рис. 69), распределенных в дисперсионной среде (нефтяные масла и смолы).
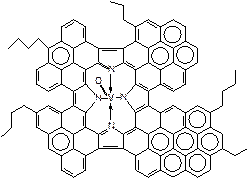
Рис. 69. Структура асфальтена
Асфальтены плавятся при 200 – 300 оС. Однако в среде нефтяных масел и смол черная дисперсная твердая масса (Т/Ж) асфальтенов размягчается уже при температуре 25 – 90 оС. Используется битум в смеси с песком, гравием, щебнем в качестве дорожного покрытия.
Природный газ в химической промышленности используют в качестве сырья для получения синтез-газа:
Т= 800 оС, Ni
СН4(г) + Н2О (г) ® СО(г) + Н2(г),
водорода:
Т= 1000 оС
СН4(г) ® С(т) + Н2(г),
ацетилена:
Т= 1200 оС
СН4(г) ® С2Н2(г) + Н2(г),
этилена:
Т= 500 - 900 оС, Mn-
2СН4(г) ® С2Н4(г) + Н2(г).
7.3. Высокомолекулярные соединения (полимеры)
Название высокомолекулярные соединения или полимеры свидетельствует о том, что соединения имеют большую молекулярную массу порядка 104 – 106 г/моль. Отличает высокомолекулярные соединения сочетание большой массы с цепным строением молекул. Длина макромолекул полимера обычно превосходит их поперечное сечение примерно в 1000 раз.
Цепное строение макромолекул приводит к анизотропии (зависимости свойств тела, в данном случае механических, оптических, электрических и других свойств полимерного вещества, от направления внутри тела). Анизотропия полимеров ярко выражена при получении волокон и пленок, имеющих потребительский спрос.
Уникальные свойства проявляют такие полимерные материалы, как каучук и резина. Они эластичны и проявляют высокую обратимую деформацию при сжатии или растяжении.
Низкомолекулярное вещество, из которого синтезируют полимер, называют мономером.
Полимеры могут иметь линейную структуру или содержать поперечные связи между линейными цепями.
Линейные полимеры при нагревании размягчаются, а при охлаждении затвердевают. Это - термопластичные полимеры, легко поддающиеся формованию, что позволяет получать из них изделия различных форм. Они инертны в агрессивных химических средах, не подвержены коррозии, и многие из них обладают прекрасными электроизоляционными свойствами.
Высокомолекулярные соединения являются основой пластических масс (пластмасс). Пластмассами называют полимерные материалы, формуемые в изделия в пластическом состоянии обычно при повышенной температуре и под давлением. Пластмассы могут содержать твердые или газообразные наполнители – вещества, изменяющие структуру и механические свойства пластмассы. Например, формование полимера со стекловолокном позволяет получить довольно прочный материал - стеклопластик. Использование в качестве наполнителя пузырьков газа позволяет получить легкие пластмассовые изделия – пенопласты.
Основное достоинство пластмасс - возможность изготовления изделий разнообразной, самой сложной формы без каких-либо отходов (литье под давлением или штамповка). К недостаткам следует отнести горючесть, растрескивание под напряжением (нагрузкой) и довольно низкую температуру эксплуатации, часто не выше 100 оС.
Полиэтилен –[СН2=СН2]n– получают в результате радикальной полимеризации этилена при высоком давлении (1000 – 2000 атм) и температуре (200 – 300 оС). В качестве инициаторов полимеризации используют пероксиды. Реакция полимеризации длится обычно 1 – 2 мин и завершается превращением примерно 25% мономера в полимер, который отделяют затем от мономера. Так получают полиэтилен высокого давления:
nСН2=СН2 ® –[СН2=СН2]n–.
Молекулярная масса этилена (мономер) СН2=СН2 равна 28 г/моль. В полиэтилене число повторяющихся структурных звеньев цени (n) колеблется от 3500 до 10 000
[СН2-СН2]n =3500 – 10000
и молекулярная масса соответственно лежит в пределах от 100 000 до 300 000 г/моль.
Для получения полиэтилена низкого давления (р = 15 – 30 атм и Т = 70 – 95 оС) используют катализатор Циглера – Натта, на основе триэтилалюминия (C2H5)3Al и тетрахлорида титана TiCl4, благодаря которому осуществляют ионную полимеризацию этилена.
Полиэтилен широко используют в качестве упаковочного материала. Из него делают пленки для парников, обладающие рядом преимуществ перед силикатным стеклом. Полиэтилен используют для изготовления труб, не поддающихся коррозии, из него делают удобную посуду, в которой хранят агрессивные вещества, его используют в качестве электроизоляционных покрытий, разнообразных пенопластов. Температура эксплуатации изделий обычно не выше 100 оС.
Полипропилен –[СН2=СН−СН3]n – получают полимеризацией пропилена:
nСН2=СН−СН3
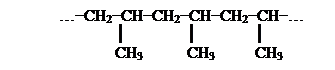 ¯
¯
Полипропилен
Возможно образование макромолекул, в которых элементарные звенья цепи могут выстраиваться в строгом порядке. В этом случае группы СН3 приобретают регулярную пространственную направленность, располагаясь строго по одну сторону от углерод-углеродных связей. Стереорегулярный полипропилен имеет довольно высокую температуру размягчения (около 170 оС), повышенную жесткость и твердость. Благодаря этим свойствам его применяют при изготовлении трубопроводов, химической аппаратуры, высокопрочной изоляции и различных предметов домашнего обихода.
Политетрафторэтилен (тефлон) -[CF2-CF2]n- получают радикальной полимеризацией тетрафторэтилена СF2=CF2:
nCF2=CF2 ® -[CF2-CF2]n-.
Тефлон обладает уникальными свойствами. Он устойчив к действию любых растворителей, имеет необычайно высокую температуру размягчения, равную 327 оС, разложение тефлона идет при 425 оС. Тефлон не горит, на него не действуют концентрированные кислоты и щелочи.
Из тефлона изготавливают листы, пленки, волокна, трубы, шланги, изоляцию для проводов, радио- и электротехнические детали, протезы органов человека, покрытия для химической и металлической посуды. Температура эксплуатации возможна до 260-300 оС.
Поливинилхлорид −[СН2=СНCl]n− получают радикальной полимеризацией винилхлорида СН2=СНCl. Можно получить регулярный полимер («голова – хвост»), образованию которого способствует высокая полярность молекулы винилхлорида:
nСН2=СНCl
¯
…−СН2−СН−СН2−СН−СН2−СН−…
│ │ │
Cl Cl Cl
поливинилхлорид
Поливинилхлорид перерабатывают в винипласт – пластмассу, содержащую красители, воски, наполнители (например, оксид титана TiO2). Винипласт легко подвергается механической обработке. Из него выпускают листы, трубы, плиты. Винипласт легко сваривается, поэтому как конструкционный материал он идет на изготовление химической аппаратуры, покрытие полов, облицовку стен, в качестве тепло- и звукоизоляционного материала, например пенополивинилхлорид. Из прозрачного винипласта изготавливают тару для пищевых продуктов, бутылки.
В виде другого материала – пластиката, в котором используют добавки, снижающие хрупкость поливинилхлорида, он используется для изготовления электропроводов, шлангов, линолеума, плиток для полов, материалов для облицовки стен и обивки мебели, изготовления искусственной кожи. Температура эксплуатации поливинилхлорида не выше 100 оС.
Полистирол −[СН2−СН−С6Н5]n− также, как и предыдущие полимеры получают радикальной полимеризацией мономера – винилбензола, или стирола СН2=СН−С6Н5.








