Каталитические реакции
Каталитическая реакция происходит с более высокой скоростью при введении вещества – катализатора.
Катализатор – химическое соединение, обладающее замечательным качеством. Катализатор участвует в химических превращениях и увеличивает скорость реакции, но после завершения процесса остается в неизменном состоянии и количестве.
В человеческом организме насчитывается несколько тысяч белков – катализаторов (ферментов). Каждый из них катализирует определенную химическую реакцию. Заметим, что при температуре 36.6 – 37.0 0С в человеческом организме протекает с высокой скоростью громадное количество каталитических реакций. Ни один химический реактор, созданный руками человека, не обладает такой уникальностью.
Различают гомогенные и гетерогенные химические реакции. В первом случае реагенты и катализатор находятся в одной фазе. Так осуществляются реакции в растворах. Во втором случае реагенты находятся в жидкой или газовой фазе, а катализатор – твердое вещество.
Рассмотрим гомогенную каталитическую реакцию. Основная причина ускорения химической реакции в присутствии катализатора состоит в том, что он снижает энергию активации реакции (рис. 54).
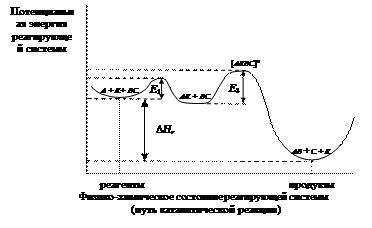
Рис. 54. Энергетический профиль реагирующей системы; Е – активационный барьер; DН r – энтальпия химической реакции
Сравним последовательность превращений без катализатора и с участием катализатора.
Реакция в отсутствии катализатора:
А + ВС ® АВ + С
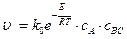
Каталитическая реакция (К – катализатор) может идти в несколько стадий, например
А + К ⇄ АК
АК+ ВС ® АВ+ С + К.
За быстрой обратимой реакцией А + К ⇄ АК следует медленная, реакция АК+ ВС ® АВ+ С + К, ограничивающая скорость всего процесса.
Запишем скорости элементарных стадий каталитической реакции
1) А + К ® АК,
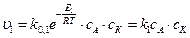 .
.
2) АК ® А + К,
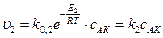 .
.
3) АК+ ВС ® АВ+ С + К,
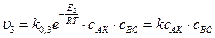 .
.
Энергия активации (Е) некаталитической реакции (рис. 53) существенно выше энергий активации каталитических реакций (рис. 54). Это обстоятельство объясняет высокую скорость каталитической реакции по сравнению с некаталитической.
Лимитирующей стадией каталитической реакции является реакция (3):
АК+ ВС ® АВ+ С + К,
u3 = k3×сАК×сВС. (5.5)
В установившемся стационарном каталитическом процессе скорость образования и расходования промежуточного комплекса АК не меняется
k1сАсК – k2сАК – k3сАКсВС = 0,
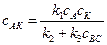 . (5.6)
. (5.6)
Концентрацию комплекса сАК из уравнения (5.6) подставим в уравнение (5.5):
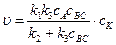 (5.7)
(5.7)
Возможны два предельных варианта течения каталитического процесса. Если скорость разложения промежуточного продукта АК во много раз больше скорости каталитического образования продуктов АВ и С, т.е. k2 >> k3сВС, то уравнение (5.7) примет вид:
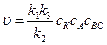 .
.
Примем во внимание, что концентрация катализатора есть величина постоянная, тогда скорость реакции выразится уравнением
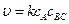 , где
, где 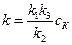 .
.
Если скорость разложения промежуточного продукта АК во много раз меньше скорости каталитического образования продуктов АВ и С, т.е. k2 << k3сВС, то уравнение (5.7) примет вид:
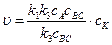 или
или
u = kcA, где k = k1cK.
Полученные уравнения демонстрируют, каким образом скорость реакции зависит от концентрации катализатора.








