Твердые вещества, жидкости и газы
Химия изучает превращения веществ, находящихся в различных агрегатных состояниях.
В отличие от такой микросистемы, как индивидуальный атом, молекула или ион, макросистема представляет собой твердое, жидкое или газообразное тело, состоящее из взаимосвязанных атомов, молекул или ионов. Например, 18 г воды содержат 6.02×1023 молекул Н2О.
Свойства макросистемы не сводятся к сумме свойств атомов, молекул или ионов, входящих в её состав. Нельзя сказать, что изолированная молекула Н2О есть частица твердая, жидкая или газообразная. У нее нет этих свойств. Она не обладает теплопроводностью, теплоемкостью – свойствами, присущими множеству молекул кристалла льда, капле жидкости или пузырьку пара. Но кристалл льда, капля жидкости или пузырек пара «наследуют» химические свойства, проявляемые молекулой воды.
Все химические превращения – это превращения атомов, молекул или ионов, из которых тела состоят.
Атомы, молекулы, ионы обладают способностью взаимодействовать между собой. Благодаря этому свойству они образуют конденсированные продукты, жидкие или твердые. Нет ни одного газа, который при понижении температуры и увеличении давления не переходил бы в конденсированное состояние. Для полноты представлений о строении вещества рассмотрим особенности строения конденсированных сред.
3.1. Модели кристаллических и аморфных веществ
В кристаллическом веществе атомы, ионы или молекулы располагаются в строгом порядке в узлах кристаллической решетки. По типу химической связи и межмолекулярного взаимодействия кристаллические решетки делятся на ковалентные (атомные), ионные, металлические и молекулярные. Мы уже приводили модели ионных и металлических кристаллических веществ. Далее представлены все возможные модели кристаллических веществ, классифицированные по типу химической связи и межмолекулярному взаимодействию.
Кристаллы
Кристаллы с ковалентными связями представляют собой структуры химически связанных атомов. Примером кристалла с ковалентными связями может служить алмаз (рис. 21). Кристаллическая решетка алмаза гранецентрированная кубическая. Кристаллы обычно имеют форму октаэдра, ромбододекаэдра, куба или тетраэдра.
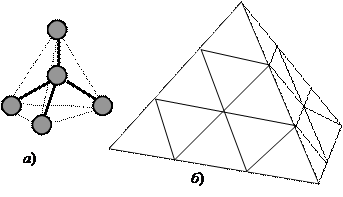 |
Рис. 21. Модель структуры кристалла алмаза: а) фрагмент кристаллической решетки: центральный атом углерода окружен четырьмя равноудаленными атомами углерода, находящимися в углах тетраэдра; б) кристалл, построенный из тетраэдрических фрагментов








