Главное квантовое число ( n ) – параметр, с помощью которого можно вычислить энергию электрона в атоме.
Группа – вертикальный ряд периодической системы, в котором объединены атомы химических элементов с одинаковым числом электронов на внешней орбитали.
Квантовые числа определяют значения физических величин, характеризующих атом, ядро атома, молекулу или элементарные частицы.
Магнитное квантовое число ( ml ) определяет число орбиталей для данного значения орбитального квантового числа l .
Модель есть объект-заменитель объекта-оригинала, сохраняющий некоторые его свойства.
Орбиталь – отрицательно заряженная область атома, в которой вероятность обнаружить движущийся электрон (или электроны) уменьшается по мере удаления от ядра.
Орбитальное квантовое число ( l ) – параметр, с помощью которого можно определить форму орбитали и энергию подуровня.
Период – это горизонтальный ряд элементов, в атомах которых электроны последовательно заполняют ns - и завершают заполнение np -орбиталей.
Периодический закон: свойства элементов и образуемых ими простых и сложных веществ находятся в периодической зависимости от заряда ядра атомов элементов.
Правило Гунда: устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором сумма спиновых чисел максимальна ( å ms = max).
Принцип запрета Паули: на одной орбитали не может быть больше двух электронов, различающихся спиновыми числами ms = + 1/2 и - 1/2.
Принцип наименьшей энергии: электроны заполняют орбитали в порядке возрастания энергии от низшего к высшему энергетическому уровню.
Принцип неопределенности: объект микромира невозможно одновременно с наперед заданной точностью характеризовать координатой и импульсом.
Свойство – это качество, постоянно присущее объекту.
Система есть совокупность взаимосвязанных частей, выделенных из окружающей среды и выступающих по отношению к ней как целое.
Соотношение неопределенности: 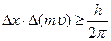 .
.
Спин электрона – собственный момент количества движения электрона. В моделях атомов спин обозначается .
Химия – наука, изучающая состав, свойства и превращения вещества, а также явления, которые сопровождают эти превращения .
Электронное облако характеризует не образ «размытых» в пространстве электронов или электрона, а область вероятного местонахождения электронов относительно ядра.
Ядро атома – микросистема, которая состоит из протонов и нейтронов.








