Литературный обзор по теме:»Проявление синергизма и антагонизма в смешанных растворах ПАВ.Расчет параметров взаимодействия».
РХТУ им. Д.И. Менделеева
Кафедра коллоидной химии
Литературный обзор по теме:»Проявление синергизма и антагонизма в смешанных растворах ПАВ.Расчет параметров взаимодействия».
Выполнил студент 4 курса гр.Тм-44
Умаров В.А.
Проверила Киенская К.И.
Москва 2014
Содержание
Введение …………………………………………………………... 3
1. Литературный обзор ……………………………………………… 5
1.1.Экспериментальная часть(опыт №1) ……………………. 5
1.2. Результаты(опыт №1)……………………. ………………….…. 6
1.3.Экспериментальная часть(опыт №2) ……………………. 10
1.4. Результаты(опыт №2)……………………. …………………….. 10
1.5. Выводы …………………………………………………..…………….. 13
2. Литература ………………………………………………………..……… 14
3. Приложения ……………………………………………………..………. 15
Введение
Актуальность работы. Коллоидно-химические свойства смесей поверхностно-активных веществ (ПАВ) изучаются в последнее время весьма интенсивно. При этом известны случаи как усиления (синергизм), так и ослабления(антагонизм) действия ПАВ в смеси. Благодаря
синергетическому действию компонентов смеси
широко используются во многих технологиях:
· Нанесение покрытий;
· Флотация;
· Нефтедобыча;
· Разработка рецептур косметических средств и др.
Они обеспечивают более высокую эффективность по сравнению с индивидуальными ПАВ.
К настоящему времени достаточно хорошо изучены неаддитивные эффекты в водных растворах бинарных смесей ПАВ при мицеллообразовании и адсорбции компонентов смесей на различных границах раздела фаз(раствор–воздух, раствор-твердое тело). Проявление неаддитивного действия ПАВ принято связывать с наличием избыточного взаимодействия между молекулами(ионами) компонентов смеси, мерой которого является параметр β. В частности, при избыточном (по сравнению с молекулами или ионамиодного сорта) притяжении наблюдается синергизм действия ПАВ в смеси, т.е. какой-либо показатель достигается при меньших концентрациях ПАВ в смеси, чем в растворах чистых компонен тов. В этом случае параметры взаимодействияβ < 0. Известно, что параметр β для разнотипных ПАВ существенно зависит от природы компонентов смеси.
Так в ряду катионное–неионогенное, анионное–неионогенное и катионное–анионное ПАВ β меняется от –1 до –40.
Весьма перспективно использование растворов бинарных смесей ПАВ для регулирования смачивания твердых тел различной природы. Однако
смачивающее действие растворов смесей изучено в меньшей степени по сравнению с другими объемными и поверхностными свойствами смесей.
В ряде работ описано неаддитивное поведение компонентов смесей при смачивании. Оно следует из закона Юнга:
cos θ = (σтг – σтж ) / σжг ,
где θ – равновесный краевой угол, σтг – удельная свободная поверхностная энергия на границе твердое тело–газ, σтж и σжг – межфазное натяжение на
границах твердое тело–жидкость и жидкость–газ соответственно. Неаддитивные эффекты при адсорбции на этих межфазных границах могут привести к неаддитивности при смачивании твердых тел растворами смесей ПАВ. Однако степень проявления указанных эффектов может зависеть от концентрации и соотношения ПАВ в смеси.
Теоретический анализ смачивающего действия растворов бинарных смесей ПАВ по отношению к низкоэнергетическим поверхностям проведен в ра боте, где предложен метод расчета параметров взаимодействия молекул (ионов) компонентов в смешанных адсорбционных слоях на границе низко-
энергетическая поверхность–раствор смеси и состава этих слоев по экспериментальным изотермам поверхностного натяжения σжг и краевых углов θ. Этот подход не исключает измерения краевых углов растворов индивидуальных ПАВ и их смесей. Таким образом, вопрос о прогнозировании смачивающего действия растворов смесей ПАВ по отноше-
нию к твердым поверхностям остается открытым.
Цель работы.
Исследовать смачивающее действие индивидуального ПАВ и смесей ПАВ. Сделать выводы на основе нескольких примеров. А также произвести несколько подсчетов параметров взаимодействия ПАВ между собой и с поверхностью.
1.Литературный обзор
1.1.Экспериментальная часть(опыт №1).
Использованы следующие ПАВ:
· Анионное – додецилсульфат натрия(ДДСН);
· Катионное- цетилтриметиламмоний бромид (ЦТАБ);
· неионогенное – тритон Х-100 (ТХ-100), степень оксиэтилирования n = 10, (“Serva”, Германия, чистота > 99.8%).
Растворы готовили на дистиллированной воде,рН растворов 6,5. Свойства смесей ДДСН/TX-100были исследованы в широкой области концентрацийПАВ с = (10–7–10–1) М. Для смесей ДДСН/ЦТАБ интервал концентраций c = (10–7–10–4) М ограничен,поскольку при общих концентрациях ПАВ с > 10–4происходит разделение фаз с образованием нерастворимых комплексов . Мольная доля ДДСН всмесях составляла α = 0,2; 0,5; 0,8.
Поверхностное натяжение (σжг) измеряли методом Вильгельми (уравновешивание платиновой пластинки) с точностью ±0,5 мН/м и методом максимального давления в пузырьке с точностью 0,5 мДж/м2 при температуре 293К. Значения критической концентрации мицеллообразования (ККМ) для растворов индивидуальных ПАВ и их смесей, полученные по изотермам поверхностного натяжения, хорошо согласуются с литературными данными (табл. 1). По изотермам поверхностного натяжения была рассчитана поверхностная активность индивидуальных ПАВ G = lim (–dσжг/dc)c→0 (табл. 2).
Тефлон марки ТФ-4 использовали в виде пластинок. Гидрофобизованное стекло получали при выдерживании пластинок стекла в парах диметилдихлорсилана в течение 24 ч с последующим промыванием в хлороформе. Образцы стандартизовали по краевым углам натекания (θa) и оттекания (θr) дистиллированной воды, которые составляли 120 и 118° , 104 и 103° для тефлона и гидрофобизованного стекла соответственно.
Краевые углы θ измеряли гониометрически в условиях, близких к равновесным. Точность измерений ±1° . Для каждой концентрации проводили измерения краевых углов 3–5 капель. Среднеквадратичное отклонение ±2°.
1.2.Рузультаты(опыт №1).
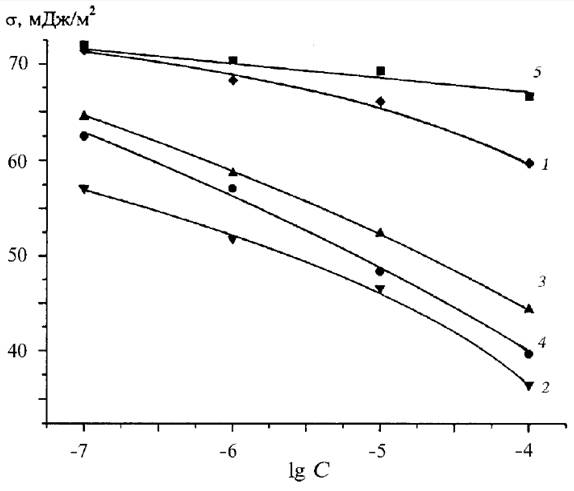
Рис. 1. Изотермы поверхностного натяжения растворов ЦТАБ(1),ДДСН (5) и их смесей при α = 0,2 (2); 0,5 (3) и 0,8 (4)(α – мольная доля ДДСН в смеси)
 |
.
На рис. 1 представлены изотермы поверхностного натяжения σжг для растворов ДДСН, ЦТАБ и их смесей. В исследованном интервале концентраций поверхностное натяжение индивидуальных ПАВ уменьшается незначительно, причем ЦТАБ проявляет большую поверхностную активность по сравнению с ДДСН (табл. 2). Изотермы σжг (с) для растворов смесей ДДСН/ЦТАБ демонстрируют синергизм действия этих ПАВ в отношении снижения поверхностного натяжения во всей области исследованных концентраций: определенное значение поверхностного натяжения для растворов смесей достигается при меньших общих концентрациях ПАВ в смеси, чем в растворах чистых компонентов. Для ДДСН и ТХ-100 синергизм в отношении снижения
поверхностного натяжения не наблюдается (рис. 2).
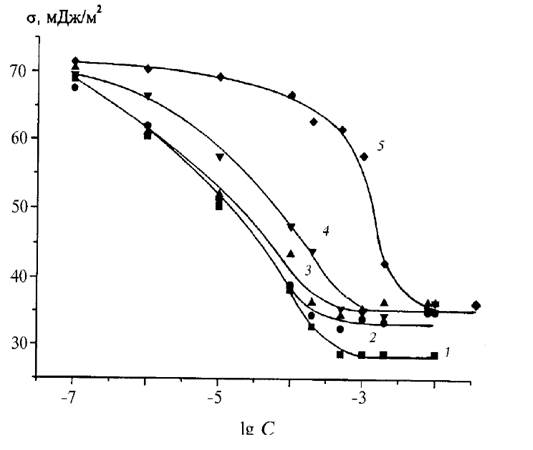
Рис. 2. Изотермы поверхностного натяжения растворов ТХ-100
(1), ДДСН (5) и их смесей при α = 0,2 (2); 0,5 (3) и 0,8 (4) (α – мольная доля ДДСН в смеси).
Зависимости поверхностного натяжения водных растворов от состава смеси (σжг = f(б)) при различных общих концентрациях ПАВ представлены на рис. 3 а, б. компоненты смесей адсорбируются на границе раствор–воздух независимо и поверхностное натяжение смешанного раствора (σmix) : σmix = ασ1 + (1 – α)σ2,где σ1 и σ2 – поверхностное натяжение растворов индивидуальных ПАВ, α – мольная доля ПАВ в смеси. 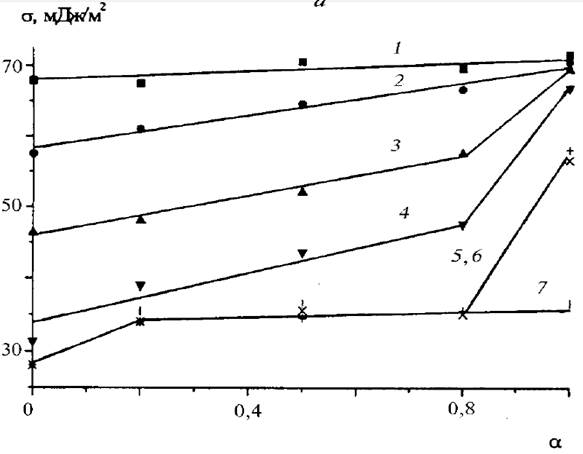
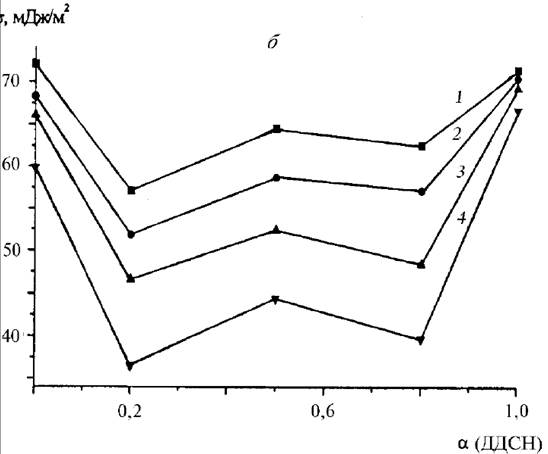
Рис. 3. Зависимость поверхностного натяжения растворов смесей
ДДСН/ТХ-100 (а) и ДДСН/ЦТАБ (б) от мольной доли ДДСН в смеси (α); общая концентрация ПАВ в растворах смесей (М): 10–7 (1);10–6 (2); 10–5 (3); 10–4 (4); 6 .10–4 (5); 10–3 (6); 10–2 (7).
Для анализа поведения компонентов смесей на границе раствор–воздух был использован известный подход Рубина и Розена, основанный на теории регулярных растворов. С использованием экспериментальных изотерм поверхностного натяжения σжг =f(с) были рассчитаны параметры взаимодействия молекул и ионов компонентов смесей ДДСН/TX-100 и ДДСН/ЦТАБ в смешанных адсорбционных слоях на границе раствор–воздух (βσ) и состав адсорбционных слоев. Расчеты проводили по уравнениям:
(Xσ)2ln(αCσ12/ XС σ1)/(1– X σ )2ln[(1 – α)C σ12/(1 – Xσ )С2] = 1, (1)
βσ = ln (αCσ12/ XσС1σ) /(1–X σ) 2, (2),
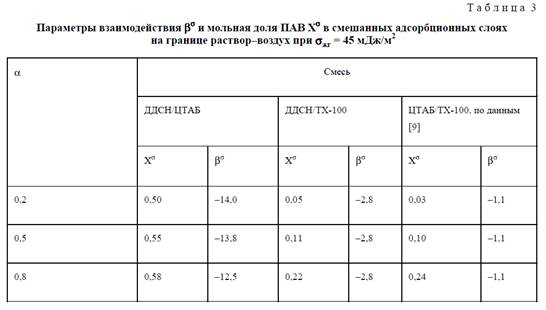
где Xσ – мольная доля ПАВ I в смешанном адсорбционном слое, С1σ, С2σ и С12σ – концентрации индивидуальных ПАВ I и II и общая концентрация ПАВ в смеси, необходимые для понижения поверхностного натяжения до заданного значения. В качестве примера в табл. 3 представлены значения βσ и Хσ при σжг = 45 мДж/м2.
1.3. Экспериментальная часть(опыт №2).
В эксперименте использовали ПАВ фирмы «Merck» (чистота 98%). Общую концентрацию С растворов смесей DTAB–ТХ-100 меняли от 10–5 до 5·10–2, смесей ди-DDAB–ТХ-100 – от 10–5 до 2,5·10–3 М. Мольная доля неионогенного ПАВ (α) в смесях составляла 0,2; 0,5 и 0,8. Растворы были приготовлены на дистиллированной воде (электропроводность æ = 2·10–3 Ом/см). Эксперимент проводили при комнатной температуре (20–22°С). Поверхностное натяжение растворов измеряли методом максимального давления в пузырьке воздуха.
1.4. Результаты(опыт №2)
Изотермы поверхностного натяжения растворов индивидуальных ПАВ и их смесей изображены на рис. 1,2. И похожи между собой: с ростом
концентрации ПАВ поверхностное натяжение сначала снижается, а при достижении ККМ принимает постоянное значение (или слабо падает). Величины ККМ, полученные графически по излому на изотермах поверхностного натяжения растворов ПАВ, приведены в табл. 4.
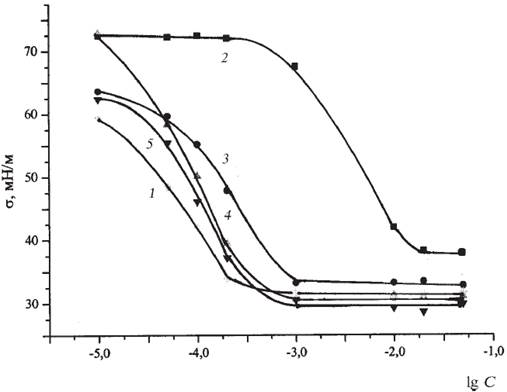
Рис. 1. Изотермы поверхностного натяжения растворов ТХ-100 (1), DTAB (2) и смесей ТХ-100 DTAB α = 0,2 (3), α = 0,5 (4), α = 0,8 (5).
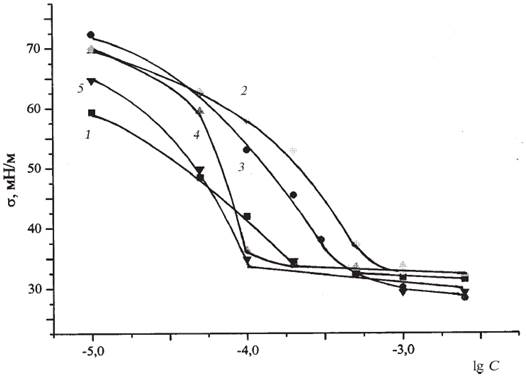
Рис. 2. Изотермы поверхностного натяжения растворов ТХ-100 (1), ди-DDAB (2) и смесей ТХ-100–ди-DDAB α = 0,2 (3), α = 0,5 (4), α = 0,8 (5).
Для термодинамического описания поведения мицеллярных растворов ПАВ наибольшее развитие получила псевдофазовая модель мицеллообразования. Согласно этой модели мицеллы представляют собой
отдельную фазу, находящуюся в равновесии с раствором ПАВ в мономерной форме. Из равенства химических потенциалов раствора и мицелл можно получить следующие соотношения для первого и второго
компонентов:
αС12m = f1C1mX1m, (3)
(1-α)С12m = (1-X1m) f2 C2m, (4)
где С1m и С2m - ККМ первого и второго компонентов соответственно, С12m- ККМ смеси, Х1m –мольная доля первого компонента в смешанной мицелле, f1 и f2 - коэффициенты активности первого и второго компонентов соответственно в смешанной мицелле.
Рассчитаем коэффициенты активности в смешанных мицеллах и определим их состав и параметр взаимодействия. Для коэффициентов активности ПАВ в смешанной мицелле можно записать:
f1 = exp βm (1-X1m)2, (5)
f2 = exp βm (X1m)2, (6)
где βm -параметр взаимодействия, Х1m – мольная доля 1-го компонента в мицелле.
βm = (E11 + E22 – 2E12) / RT, (7)
Е11, Е22 - энергии взаимодействия между молекулами ПАВ одного типа в мицеллах, Е12 -энергия взаимодействия между молекулами ПАВ разного типа.
Отсюда получаем
(X1m)2 ln(α C12m/X1mC1m)/ (1-X1m)2 ln[(1-α)C12m/(1-X1m)C2m]=1, (8)
βm =ln(αC12m/X1mC1m)/ (1-X1m)2 (9)
Определив экспериментально значения ККМ индивидуальных ПАВ и их смесей при численном решении уравнения (6), находят Х1m, а подставив полученные значения Х1m в (7), определяют параметр взаимодействия ПАВ в смешанных мицеллах.
Смеси ПАВ при мицеллообразовании или адсорбции на межфазной поверхности раствор/воздух ведут себя неидеально; наблюдаются синерге-
тические или антагонистические эффекты. Синергизм проявляется в том, что данная величина поверхностного натяжения (или ККМ) достигается при концентрациях меньших, чем это было бы при идеальном смешении компонентов.
Критерием синергизма при мицеллообразовании будет выполнение двух условий:
1) βm<0, (10)
2) | ln(C1m/C2m)| < | βm |.
Для определения состава и параметров взаимодействия в смешанных мицеллах систем ТХ-100–DТАВ и ТХ-100–ди-DDAB были использованы данные из табл. 4. Полученные значения Х1m представляют собой мольную долю ТХ-100 в смешанных мицеллах.Расчет состава таких мицелл и параметров взаимодействия, проведенный по уравнениям (6) и (7), показал, что мицеллы ТХ-100–DTAB обогащены более сильным ПАВ ТХ-100 (табл. 1), причем при α(ТХ-100 )= 0,8 мицеллы практически полностью состоят из ТХ-100.
Мицеллы ТХ-100–ди-DDAB при мольной доле ТХ-100 в растворе 0,2 и 0,5 также обогащены ТХ-100, однако в значительно меньшей степени, чем мицеллы ТХ-100–DTAB, а смесь с α = 0,8 обогащена ди-DDAB.
1.5. Выводы.
На основе работы, описанной выше, можно сделать следующие выводы :
1.Мы выяснили, как и почему появляюся синергетические и антагонические эффекты,а также выяснили как ведут себя разные растворы веществ(неионогенные,ионогенные и катионные) на границе воздух-вода при мицеллообразовании и адсорбции.
2.Приведены примеры расчетов параметров взаимодействия(поход Рубина и Розена(опыт №1), а также псевдофазовая модель мицеллообразования(опыт №2)). Узнали как при разных концентрациях ведут себя мицеллы разных веществ при мицеллообразовании и адсорбции.
3. Также, произвели сравнение индивидуального ПАВ и смешанного ПАВ и было выяснено , что перспективнее выглядит использование бинарных смесей ПАВ,нежели индивидуального ПАВ.
4. Щелочь имеет функцию разделения поверхностно-активных веществ в
водную фазу.
5.Были исследованы ККМ и синергетические эффекты в смесях анионного ПАВ и двух различных катионных амфифильных лекарственных средств
в присутствии добавленной соли. Было выяснено, что величина синергизма немного больше для катионного лекарственного средства.
2. Литература
1. Ю.Г. Богданова, В.Д. Должикова, Б.Д. Сумм // ВЛИЯНИЕ ХИМИЧЕСКОЙ ПРИРОДЫ КОМПОНЕНТОВ
НА СМАЧИВАЮЩЕЕ ДЕЙСТВИЕ РАСТВОРОВ СМЕСЕЙ
ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ // ВЕСТН. МОСК. УН-ТА. СЕР. 2. ХИМИЯ. 2004. Т. 45. № 3 c. 186.
2 . О.А. Соболева, М.В. Кривобокова // СМЕШАННЫЕ МИЦЕЛЛЫ И АДСОРБЦИОННЫЕ СЛОИ НЕИОНОГЕННОГО ПОВЕРХНОСТНО - АКТИВНОГО ВЕЩЕСТВА С КАТИОННЫМ ( МОНОМЕРНЫМ И ДИМЕРНЫМ ) // ВЕСТН. МОСК. УН-ТА. СЕР. 2. ХИМИЯ. 2004. Т. 45. № 5 c.344.
3. Ю.Г. Богданова, В.Д. Должикова // ПОВЕРХНОСТНЫЕ И ОБЪЕМНЫЕ СВОЙСТВА ВОДНЫХ РАСТВОРОВ БИНАРНЫХ СМЕСЕЙ ПЛЮРОНИКА L61 С НИЗКОМОЛЕКУЛЯРНЫМИ
ПОВЕРХНОСТНО-АКТИВНЫМИ ВЕЩЕСТВАМИ // ВЕСТН. МОСК. УН-ТА. СЕР. 2. ХИМИЯ. 200 6 . Т. 4 7 . № 4 c.284.
4. L. Magnus Bergström , Tobias Bramer // Synergistic effects in mixtures of oppositely charged surfactants as calculated from the Poisson–Boltzmann theory: A comparison between theoretical predictions and experiments // Journal of Colloid and Interface Science 8 March 2008.
5. Krassimir D. Danov , Peter A. Kralchevsky , Kavssery P. Ananthapadmanabhan // Micelle–monomer equilibria in solutions of ionic surfactants and in ionic–nonionic mixtures: A generalized phase separation model // Advances in Colloid and Interface Science 13 March 2013.
6. Lu Zhang, Lan Luo, Sui Zhao, and Jiayong Yu // Synergism/Antagonism in Surfactant/Model Oil Systems // Journal of Colloid and Interface Science March 22, 2002.
3.Приложения
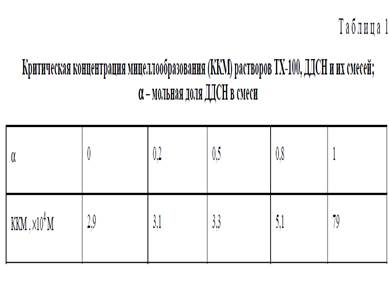
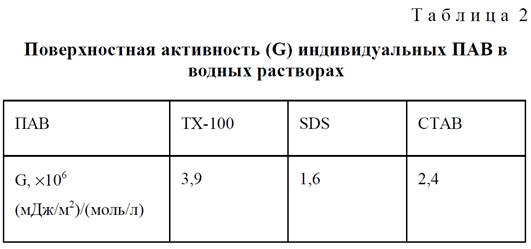
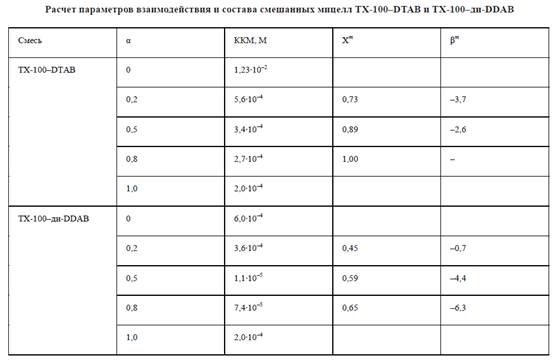 |
Таблица 4








