Исходные данные. 1. Состав стали типа X18H9: ; ; ; . 2. Растворимость азота в железе при 1 атм Чипман и Корриган описывали уравнением
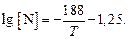 (6.1)
(6.1)
3. Учесть параметры взаимодействия только первого порядка: 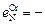 0,047;
0,047; 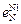 = 0,0063;
= 0,0063; 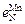 = – 0,02;
= – 0,02; 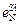 = 0,047.
= 0,047.
Теория. Чипман и Корриган, анализируя экспериментальные данные различных авторов по поведению азота в жидком железе в присутствии легирующих элементов 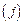 , эмпирически нашли, что энтальпийный параметр
, эмпирически нашли, что энтальпийный параметр 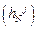 линейно зависит от параметра взаимодействия первого порядка
линейно зависит от параметра взаимодействия первого порядка 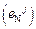 :
:
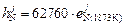 . (6.2)
. (6.2)
По определению
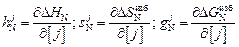 .
.
Изменение избыточной парциальной мольной свободной энергии 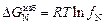 .
.
Тогда
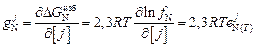 .
.
Дифференцируя уравнение 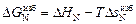 по
по 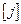 , получаем, что
, получаем, что 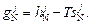
Для 1873 К имеем
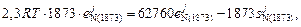
откуда
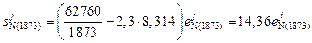 .
.
При температуре Т имеем
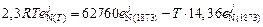 ,
,
откуда
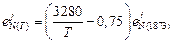 .
.
Тогда коэффициент активности азота в сплаве 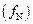 при данной темературе Т выражается уравнением
при данной темературе Т выражается уравнением
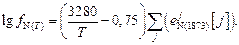
Растворимости азота в железе 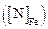 и сплаве
и сплаве 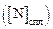 при данной Т связаны соотношением
при данной Т связаны соотношением 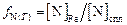 .
.
Тогда
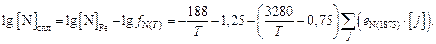
Решение
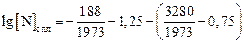 (–0,047·18 + 0,0063∙9 –
(–0,047·18 + 0,0063∙9 –
– 0,02∙1,5 + 0,047∙0,5) = –0,62;
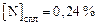 .
.
Итак, растворимость азота в стали при 1700 °С и 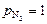 атм равна 0,24 %.
атм равна 0,24 %.
Дополнение. Для описания температурной зависимости растворимости азота в железе за последние годы предложены уравнения, отличающиеся от (6.1). В данном расчете необходимо использовать то уравнение, которое применяли Чипман и Корриган, так как соотношение (6.2) получено на его основе.
55. Расчет концентрации титана,
отвечающей нитридообразованию
Задача. Термодинамическим расчетом определить, при какой концентрации титана в стали 08Х18Н10 при 1550 °С и 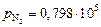 Па (0,79 атм) образуются нитриды.
Па (0,79 атм) образуются нитриды.
Исходные данные
1. 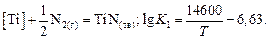 (6.3)
(6.3)
2. 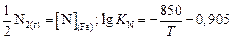 . (6.4)
. (6.4)
3. Параметры взаимодействия:
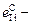 нет данных ;
нет данных ; 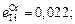
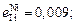
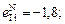
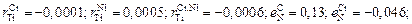
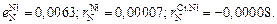
Теория. Константа реакции нитридообразования (6.3)
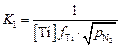 ,
,
отсюда
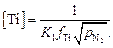 (6.5)
(6.5)
Температурную зависимость 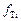 получим на основе соотношения, вытекающего из теории квазирегулярных растворов:
получим на основе соотношения, вытекающего из теории квазирегулярных растворов:
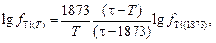 (6.6)
(6.6)
где 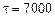 К.
К.
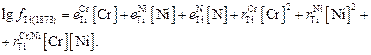 (6.7)
(6.7)
Определим концентрацию азота 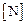 , равновесную с нитридом:
, равновесную с нитридом:
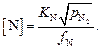 (6.8)
(6.8)
Значение 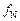 при 1550 °С вычислим по уравнению Чипмана – Корригана:
при 1550 °С вычислим по уравнению Чипмана – Корригана:
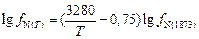 . (6.9)
. (6.9)
Решение. Вычислим 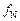 без учета
без учета 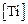 :
:
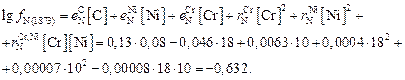
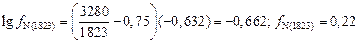 .
.
Рассчитаем 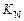 :
:
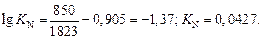
Определим 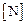 по формуле (6.8):
по формуле (6.8):
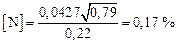 .
.
Вычислим 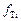 :
:
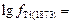 0,022∙18 + 0,009∙10 – 1,8∙0,17 –
0,022∙18 + 0,009∙10 – 1,8∙0,17 –
– 0,0001∙182 + 0,0005∙102 – 0,0006∙18∙10 = 0,09;
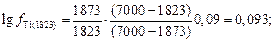
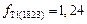 .
.
Рассчитаем 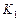 :
:
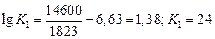 .
.
Определим искомую концентрацию титана 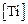 по уравнению (6.5):
по уравнению (6.5):
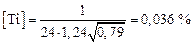 .
.
Итак, нитриды титана в стали 08Х18Н10 при 1550 °С и 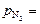 0,79 атм могут образовываться при концентрации титана 0,036 %.
0,79 атм могут образовываться при концентрации титана 0,036 %.
Примечание. Для уточнения результата иногда полезно сделать вторую итерацию, учтя, что 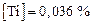 тоже влияет на
тоже влияет на 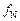
(а может быть и на 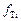 ).
).
56. Расчет температуры нитридообразования
в стали
Задача. Сталь 08Х18Н10Т содержит 0,04 % азота и 0,6 % титана. Определить, при какой температуре в ходе охлаждения в ней может начаться образование нитридов титана.
Исходные данные
1. 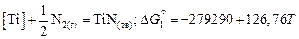 Дж/моль. (6.10)
Дж/моль. (6.10)
2. 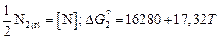 Дж/моль. (6.11)
Дж/моль. (6.11)
3. 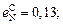
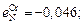
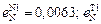 = –0,53;
= –0,53;
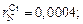
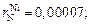
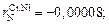
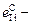 нет данных;
нет данных; 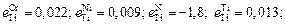
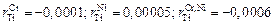 .
.
Теория. Реакция образования нитрида титана в стали имеет вид
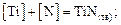 (6.12)
(6.12)
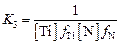 . (6.13)
. (6.13)
Прологарифмируем (6.13):
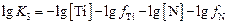 . (6.14)
. (6.14)
Изменение энергии Гиббса реакции (6.12) 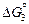 находим, комбинируя уравнения (6.10) и (6.11):
находим, комбинируя уравнения (6.10) и (6.11):
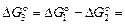 –279290 + 126,76T – (16280 + 17,32T) =
–279290 + 126,76T – (16280 + 17,32T) =
= –295570 + 109,44T Дж/моль.
Тогда зависимость K от Т определяется выражением
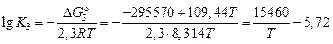 . (6.15)
. (6.15)
Для определения температурной зависимости 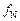 используем соотношение Чипмана – Корригана:
используем соотношение Чипмана – Корригана:
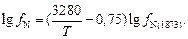 (6.16)
(6.16)
Зависимость 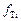 от Т получим на основе теории квазирегулярных растворов.
от Т получим на основе теории квазирегулярных растворов.
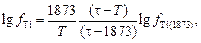 (6.17)
(6.17)
где 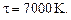
Подставив (6.16) и (6.17) в (6.14) и приравняв правые части выражений (6.14) и (6.15), получим уравнение, из которого можно найти температуру нитридообразования Т:
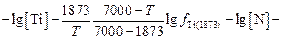
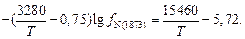 (6.18)
(6.18)
 Решение. Вычислим
Решение. Вычислим 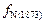 и
и 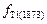 :
:
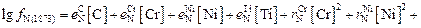
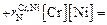 0,13∙0,08 – 0,046∙18 + 0,0063∙10 – 0,53∙0,6 +
0,13∙0,08 – 0,046∙18 + 0,0063∙10 – 0,53∙0,6 +
+ 0,0004∙182 + 0,00007∙102 – 0,00008∙18∙10 = –0,95;
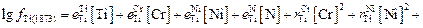
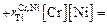 0,013∙0,6 + 0,22∙18 + 0,009∙10 – 1,8∙0,04 – 0,0001 182+
0,013∙0,6 + 0,22∙18 + 0,009∙10 – 1,8∙0,04 – 0,0001 182+
+ 0,0005∙102 – 0,0006∙18∙10 = 0,33.
Подставим 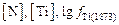 и
и 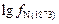 в (6.18):
в (6.18):
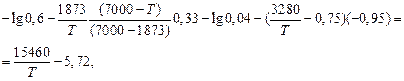
откуда Т = 1960 K (1687 °С).
57. Растворимость газов в шлаке
Задача. С целью удаления водорода из синтетического шлака, предназначенного для обработки жидкого металла, шлак при температуре 1823 К предварительно продувают азотом в ковше, футерованном керамическими материалами, через керамическую фурму. Определить степень загрязнения шлака азотом в результате такой продувки и изменение содержания азота, если использовать в качестве материала для фурмы и ковша графитовые огнеупоры.








