2.3 Герметизовані свинцево-кислотні акумулятори
Перший працездатний свинцево-кислотний акумулятор був винайдений у 1859 р. французьким вченим Гастоном Планте. Конструкція акумулятора являла собою електроди з листового свинцю, розділені сепараторами з полотна, які були згорнуті в спіраль і поміщені в посудину з
10 % розчином сірчаної кислоти. Недоліком перших свинцево-кислотних акумуляторів була їх невисока ємність. Спочатку для її збільшення проводили велику кількість циклів заряду-розряду. Для досягнення істотних результатів було потрібно до двох років таких тренувань. Причина недоліку була явною – конструкція пластин. Тому подальше вдосконалювання конструкції свинцево-кислотних акумуляторів було зосереджене на вдосконалюванні конструкції використовуваних у них пластин і сепараторів.
У 1880 р. К. Фор запропонував методику виготовлення намазаних електродів шляхом нанесення на пластини окислів свинцю. Така конструкція електродів дозволила значно підвищити ємність акумуляторів. А в 1881 р.
Е. Фолькмар запропонував застосовувати як електродно-намазні ґрати. У тому ж році вченому Селлону був виданий патент на технологію виготовлення ґрат зі сплаву свинцю й сурми.

Рисунок 2.2 – Акумулятор із свинцевими пластинами
Спочатку практичне використання свинцево-кислотних акумуляторів було ускладнене через відсутність зарядних пристроїв – для заряду застосовували первинні елементи конструкції Бунзена. Тобто хімічне джерело струму заряджалося від іншого хімічного джерела – батареї гальванічних елементів. Положення кардинально змінилося з появою недорогих генераторів постійного струму.
Саме свинцево-кислотні батареї першими у світі з акумуляторних батарей набули комерційного застосування. До 1890 року в багатьох промислово розвинених країнах був освоєний їх серійний випуск. У 1900 році німецька фірма Varta зробила перші стартерні акумулятори для автомобілів.
У 70-х роках XX століття були створені акумуляторні батареї, що не обслуговують кислотні, здатні працювати в будь-якому положенні. Рідкий електроліт у них замінили гелієвим або адсорбованим (відібраним) сепараторами електролітом, батареї герметизували, а для відведення газів, що виділяються під час заряджання або розряджання, установили клапани. Строго кажучи, абсолютна герметизація свинцево-кислотних акумуляторів не може бути досягнута, тому що не можна забезпечити повну рекомбінацію кисню й водню, які виділяються в них під час заряджання й зберігання. Але спеціальними заходами виділення газів і втрати води в процесі експлуатації вдається звести до мінімуму.
Були розроблені нові конструкції пластин на базі мідно-кальцієвих сплавів, покритих оксидом свинцю, а також на основі титанових, алюмінієвих і мідних ґрат. Свинцеві акумулятори є найпоширенішими серед всіх існуючих на цей час хімічних джерел струму. Їх масштабне виробництво визначається як відносно низькою ціною, обумовленою порівняльною недефіцитністю вихідних матеріалів, так і розробленням різних варіантів цих акумуляторів, що відповідають вимогам широкого кола споживачів.
2.4 Ключові електрохімічні процеси у свинцево-кислотному акумуляторі
Активні речовини акумулятора зосереджені в електроліті й позитивних та негативних електродах, а сукупність цих речовин називається електрохімічною системою. У свинцево-кислотних акумуляторних батареях електролітом є розчин сірчаної кислоти (H2SO4), активною речовиною позитивних пластин – двоокис свинцю (Pb2), негативних пластин – свинець (Pb).
Основні процеси, що проходять на електродах, описують такі реакції:
на негативному електроді:
Pb + HSO 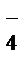 → PbSO4 + H+ + 2e- (розряд),
→ PbSO4 + H+ + 2e- (розряд),
PbSO4 + H+ + 2e- → Pb + HSO4- (заряд);
на позитивному електроді:
PbO2 + HSO 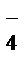 + 3H+ + 2e- → PbSO4 + 2H2O (розряд),
+ 3H+ + 2e- → PbSO4 + 2H2O (розряд),
PbSO4 + 2H2O → PbO2 + HSO4- + 3H+ + 2e- (заряд).
Сумарна реакція у свинцевому акумуляторі має такий вигляд:
PbO2 + Pb + 2H2SO4 → 2PbSO4 + 2H2O (розряд),
2PbSO4 + 2H2O → PbO2 + Pb + 2H2SO4 (заряд ).
Таким чином, при розрядженні свинцевого акумулятора на обох електродах формується малорозчинний сульфат свинцю (подвійна сульфатація) і відбувається сильне зменшення густини сірчаної кислоти.
Напруга розімкнутого ланцюга зарядженого акумулятора дорівнює 2,05–2,15 В залежно від концентрації сірчаної кислоти. Під час розряджання в міру зменшення густини електроліту напруга розімкнутого ланцюга акумулятора знижується й після повного зарядження дорівнюватиме 1,95–2,03 В.
При заряджанні свинцево-кислотного акумулятора, як і в інших акумуляторах з водним електролітом, мають місце побічні реакції виділення газів. Виділення водню починається при повному зарядженні негативного електрода. Кисень починає виділятися набагато раніше: у звичайних умовах заряджання при 50–80 % зарядженості (залежно від струму зарядження), а при температурі 0 °С уже після зарядження на 30–40 %. Внаслідок цього віддача позитивного електрода за ємністю становить 85–90 %. Для одержання повної розрядної ємності під час заряджання акумулятору повинен бути забезпечений перезаряд на 10–20 %. Цей перезаряд супроводжується істотним виділенням водню на негативному електроді й кисню – на позитивному.
Виділення водню має місце і при зберіганні зарядженого свинцево-кислотного акумулятора. Саморозряд його визначається переважно швидкістю розчинення свинцю відповідно до реакції
Pb + H2SO4 → PbSO4 + H2.
Швидкість цього процесу залежить від температури, обсягу електроліту і його концентрації, але найбільше – від чистоти компонентів. За відсутності домішок реакція проходить повільно через велику перенапругу виділення водню на свинці. Але на практиці на поверхні свинцевого електрода завжди багато домішок, серед яких найбільший вплив робить сурма, кількість якої в сплаві для ґрат і струмоведучих деталей доходить до 6 %.
На позитивному електроді може також мимовільно проходити реакція відновлення діоксиду свинцю:
PbO2 + H2SO4 → PbSO4 + 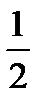 O2 + H2O,
O2 + H2O,
у результаті якої виділяється кисень, але швидкість її незначна.
У процесі експлуатації саморозряд акумулятора може збільшуватися через утворення дендритних містків із металевого свинцю. Втрати ємності щойно виготовленого акумулятора за рахунок саморозряду, як правило, не перевищують 2–3 % за 1 місяць. Але при експлуатації вони швидко збільшуються.








