Поверхностное натяжение s определяется количеством энергии в форме работы, приходящегося на изменение единицы площади поверхности дисперсной фазы.
Силикагель (аморфная форма оксида кремния SiO2) в виде порошка с удельной поверхность 5 – 800 м2/г. применяют как адсорбент для осушки газов и органических жидкостей от влаги.
Смачивание - прилипание (адгезия) жидкости к твердой поверхности.
Субстрат – тело, к которому прилипает адгезив.
Физическая адсорбция – обратимый процесс концентрирования вещества на поверхности, который осуществляется под действием сил Ван дер Ваальса или в результате образования водородных связей.
Химическая адсорбция – необратимая химическая реакция адсорбтива с адсорбентом на поверхности раздела фаз.
Цеолиты – специально прогретые белые, иногда бесцветные порошки алюмосиликатов, являются молекулярными ситами – микропористыми материалами, способными избирательно поглощать вещества, размеры молекул которых меньше размеров микропор.
Вопросы для проверки знаний
1. В чем причина нескомпенсированности сил межмолекулярного взаимодействия на границе раздела фаз?
2. Какой физический смысл несет понятие «поверхностное натяжение»?
3. Какие межмолекулярные взаимодействия определяют явления смачивания и адгезии?
4. Справедливо ли утверждение, что «уменьшение поверхностного натяжения, процессы смачивания и прилипания (адгезии) являются самопроизвольными процессами»?
5. Почему поверхностно-активные вещества уменьшают поверхностное натяжение?
6. В чем различие между физической, химической и ионообменной адсорбцией?
7. В чем различие между адсорбентом, адсорбтивом и адсорбатом?
Упражнение
1. Докажите, к физической или химической адсорбции относится адсорбционный процесс, сопровождающийся выделением 300 кДж/моль энергии.
ТЕМА 3
ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ
Частицы жидкой или твердой дисперсной фазы проявляют электрические свойства. Согласно современным представлениям взаимодействие частиц дисперсной фазы и дисперсионной среды приводит к образованию двойного электрического слоя на межфазной поверхности. Процесс происходит самопроизвольно в результате стремления системы уменьшить поверхностное натяжение на границе раздела фаз и перейти в устойчивое состояние. Критерием самопроизвольного протекания процесса служит функция Гиббса DG сист. < 0.
3.1. Механизм образования двойного электрического слоя на границе раздела фаз
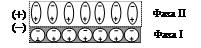
Образование двойного электрического слоя возможно в результате ориентационного, индукционного или дисперсионного взаимодействия молекул, расположенных на поверхностях соприкасающихся фаз. В этом случае поверхность одной из соприкасающихся фаз заряжается положительно, другой – отрицательно (рис. 18).
| |||||||||
| |||||||||
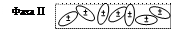 | |||||||||
 | |||||||||
 | |||||||||
Рис. 18. Модель образования двойного электрического слоя на границе раздела фаз в результате индукционного взаимодействия:
а) поверхности двух фаз до контакта; б) образование двойного электрического слоя
Положительный заряд несет поверхность, вещество которой имеет большую диэлектрическую проницаемость. Так происходит с водой, поверхность которой заряжается положительно при контакте с поверхностью менее полярных веществ (рис. 18).
Другой путь возникновения двойного электрического слоя реализуется в результате избирательной адсорбции катионов или анионов на границе раздела фаз твердое тело – раствор электролита. Так происходит образование устойчивого золя (высокодисперсной коллоидной системы) йодистого серебра в результате обменной реакции:
AgNO3(р-р) + KI(р-р) ® AgI(т)¯ + KNO3(р-р),
Ag+(р-р)+NO3-(р-р) + K+(р-р) + I-(р-р) ® AgI(т)¯+ K+(р-р) + NO3-(р-р),
Ag+(р-р) + I-(р-р) ® AgI(т)¯.
На поверхности твердой частицы избирательно адсорбируются только те ионы, которые способны достроить её кристаллическую решетку (правило Панета-Фаянса). Если одна из солей, участвующая в обменной реакции, взята в избытке, например, избыток AgNO3 по отношению к KI – образуются микрокристаллы AgI (ядра) в окружении родственных кристаллической решетке положительно заряженных ионов серебра. Ионы серебра «достраивают» кристаллическую решетку уже в отсутствие ионов йода. Формируется мицелла (рис. 19), состоящая из ядра и двойного электрического слоя:
Мицелла
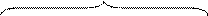 |
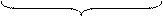 [AgI]m nAg+|(n - у)NO3- | уNO3- .
[AgI]m nAg+|(n - у)NO3- | уNO3- .
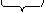
ядро двойной электрический слой
где m - количество ионных пар в структуре ядра, n - количество потенциалопределяющих ионов, у - количество противоионов в диффузной части двойного электрического слоя.
 |
|



 |
Рис. 19. Модель мицеллы [AgI]m nAg+|(n - у)NO3- | уNO3- .
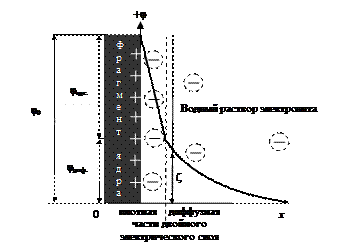
Рис. 20. Модель распределения зарядов в двойном электрическом слое мицеллы йодистого серебра в водном растворе, содержащем избыток AgNO3; х – расстояние от поверхности частицы в объем жидкой фазы
Двойной электрический слой, окружающий ядро, включает ионы адсорбционного и диффузного слоя (рис. 20). По мере удаления от поверхности твердого тела на расстояние (х) в объем электролита наблюдается падение разности потенциалов между твердой и жидкой фазами. Полное падение потенциала в двойном электрическом слое называется термодинамическим потенциалом j0. Он включает скачки потенциалов адсорбционной (плотной) и диффузной частей двойного электрического слоя:
j0 = jадс + jдиф.
Полная компенсация заряда твердой поверхности суммарным зарядом противоионов происходит на расстоянии х, где заканчивается диффузионный слой.
Адсорбционный слой противоионов примыкает к заряженной поверхности твердой частицы и имеет толщину гидратированного иона (гидратированные ионы адсорбционного слоя обведены пунктирными кружками). Ядро с адсорбционным слоем прочно связано электростатическими и адсорбционными силами и образует единое целое – заряженную микрочастицу коллоидного раствора, которая свободно перемещается в дисперсионной среде независимо от диффузного слоя. При движении частицы золя разрывается двойной электрический слой на так называемой границе скольжения. Граница скольжения лежит между адсорбционным и диффузным слоем или несколько удаляется от адсорбционного в диффузный слой. В последнем случае частица «захватывает» при своем движении некоторое количество противоионов диффузного слоя. Дзета-потенциал (z) – потенциал границы скольжения. Он определяет скорость перемещения дисперсной фазы относительного дисперсионной среды (рис. 20).
При избытке в растворе ионов йода (по отношению к ионам серебра) строение мицеллы изменяется:
Мицелла
 |
[AgI]m nI- |(n - у)K+ | уK+.
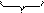 |  | ||
ядро двойной электрический слой
 Потенцииалоопределяющими становятся ионы йода, и микрочастицы приобретают отрицательный заряд (рис. 21).
Потенцииалоопределяющими становятся ионы йода, и микрочастицы приобретают отрицательный заряд (рис. 21).
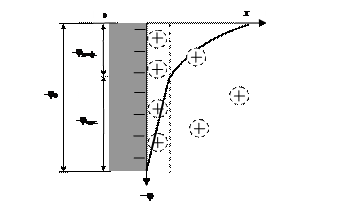
Рис. 21. Модель распределения зарядов в двойном электрическом слое мицеллы йодистого серебра в водном растворе, содержащем избыток КI; х – расстояние от поверхности в объем жидкой фазы
По цвету золь йодистого серебра напоминает молоко. Частицы золя имеют размеры, соответствующие высокодисперсной системе (10-9 ¸ 10-7м). Они не оседают из-за небольшой массы и не слипаются в силу того, что имеют одинаковый знак заряда частиц золя.
Обратим еще раз внимание на правило Панета-Фаянса: на поверхности частиц золя адсорбируются родственные кристаллу ионы серебра или йода, и лишь затем располагаются противоионы.
Знак и величина заряда частицы зависят в существенной степени от специфической адсорбции потенциалоопределяющих ионов. Может оказаться, что адсорбционные силы и концентрация противоионов настолько высока, что происходит перезарядка частиц золя. В этом случае дзета-потенциал изменяет свой знак (рис. 22).
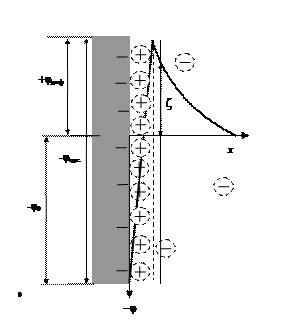
Рис. 22. Изменение z-потенциала поверхности при перезарядке частиц золя
Так происходит, если к золю йодистого серебра
Мицелла
 |
[AgI]m nI- |(n - у)K+ | уK+.
 | |||
 | |||
ядро двойной электрический слой
добавить, например, нитрат железа Fe(NO3)3. Ионы Fe3+ обладают высокой адсорбционной способностью. Они будут входить в адсорбционный (плотный) слой вместе с ионами К+ в таком количестве, что изменят знак заряда частицы золя. При этом ионы Fe3+ не способны достраивать кристаллическую решетку частиц золя в силу действия известного правила Панета-Фаянса, т.к. не имеют никакого сходства по размеру (неизоморфны) с ионами серебра Ag+, входящими в ионную кристаллическую решетку частиц золя: Мицелла
 |
 [AgI]m nI- |(nK+ + уFe3+)| (n + 3уNO3-.
[AgI]m nI- |(nK+ + уFe3+)| (n + 3уNO3-.
 |
ядро двойной электрический слой
Это приводит к перезарядке частиц золя.
3.2 Электрокинетические явления
Электрокинетические явления – это движение дисперсной фазы и дисперсионной среды под воздействием внешнего электрического поля или возникновения разности потенциалов при движении дисперсной фазы и дисперсионной среды.
К такому виду явлений относится электроосмос - это вызванное внешним электрическим полем движение дисперсионной среды относительно неподвижной дисперсной фазы и электрофорез - движение частиц дисперсной фазы относительно дисперсионной среды, также вызванное внешним электрическим полем.
К электрокинетическим явлениям относятся также явления, противоположные электроосмосу и электрофорезу. При протекании жидкости через капиллярно-пористую перегородку возникает разность потенциалов на электродах, расположенных на концах пористой перегородки (потенциал протекания). Между электродами, расположенными на разной высоте, также возникает разность потенциалов, если в сосуде происходит оседание частиц дисперсной фазы (потенциал седиментации).
Электроосмос
Напомним о явлении осмоса (др.-греч wsmoV толчок, давление). В общем случае осмос – односторонний перенос растворителя из раствора с меньшей концентрацией в раствор с большей концентрацией растворенного вещества через полупроницаемую перегородку, разделяющую растворы. Известны полупроницаемые перегородки (мембраны), пропускающие только растворитель и другие – пропускающие только растворенное вещество. Различные биологические мембраны проницаемы не только для частиц растворителя, но избирательно пропускают некоторые ионы и молекулы растворенных веществ. В данном разделе рассматриваются осмотические явления с участием мембран, пропускающих растворитель.
На рис. 23 представлен термодинамически разрешенный (самопроизвольный) процесс выравнивания концентраций в результате перехода растворителя из менее концентрированного в более концентрированный раствор через мембрану. В результате осмоса объем раствора в коленах U-образного сосуда изменяется. Создается препятствующее осмосу гидростатическое давление (осмотическое давление p) столба жидкости h, в итоге наступает осмотическое равновесие.
исходное состояние конечное (равновесное) состояние системы

Рис. 23. Схема прибора, демонстрирующего явление осмоса.
Если в одном колене находится раствор соли, а в другом – чистая вода, то высота столба жидкости и, соответственно, осмотическое давление тем больше, чем больше концентрация соли в воде:
p = с RT .
Электроосмос не является самопроизвольным процессом. Требуется затратить некоторое количество электрической энергии на перемещение растворителя из одного колена в другое через мембрану, функцию которой может выполнять, например, кварцевый песок (рис. 24).
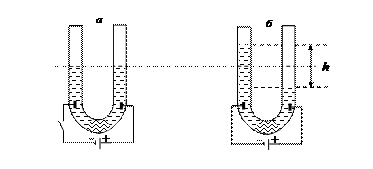
Рис. 24. Явление электроосмоса в U-образной трубке, заполненной кварцевым песком и водой: а) уровни воды в обоих коленах одинаковые, система находится в состоянии равновесия; б) при наложении электрического поля наблюдается перемещение жидкости, происходящее до тех пор, пока не будет достигнуто давление, препятствующее дальнейшему изменению уровней
Под воздействием постоянного электрического поля наблюдается изменение уровней жидкости в коленах U-образной трубки, содержащей кварцевый песок.
В результате реакции:
SiO2 + 2H2O ® H2SiO3 + H2O ® H3O+ + HSiO3-
частицы дисперсной фазы (кварцевого песка) представляют собой мицеллы.
Мицелла
 |
 [SiO2]m nHSiO3- |(n - у) H3O+ | у H 3 O +.
[SiO2]m nHSiO3- |(n - у) H3O+ | у H 3 O +.
ядро двойной электрический слой диффузный слой
Окруженные двойным электрическим слоем частицы кварца создают условия, когда при действии внешнего электрического поля гидратированные ионы диффузной части (Н3О+) мицеллы перемещаются к отрицательному электроду, повышая уровень жидкости в левой части U-образного колена (рис. 24).
На рис. 25 показана модель движения гидратированных ионов диффузного слоя внутри капилляра из кварцевого песка в результате действия электроосмоса. Положительно заряженные противоионы Н3О+ движутся в направлении отрицательно заряженного электрода источника тока.
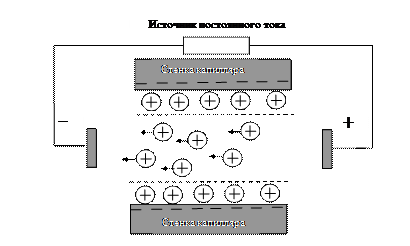
Рис. 25. Модель электроосмоса – модель движения гидратированных ионов диффузного слоя внутри капилляра из кварцевого песка
Электроосмос используется при обезвоживании капиллярно-пористых тел, сыпучих материалов, сахарных сиропов, при очистке воды и осушке стен зданий.
Известно, что при нарушении гидроизоляции стен подвальных помещений они сыреют от почвенной влаги, проникающей в стены по капиллярам. В этом случае для осушки стен используют электроосмос. В верхнюю часть стены подвального помещения вблизи потолка устанавливают один электрод, а другой помещают в грунт через отверстие в полу. Знаки электродов устанавливают так, чтобы влага в составе гидратированных ионов диффузного слоя уходила по капиллярам из стены в почву.
Стены старых зданий необходимо не только сушить. Для поддержания их в сухом состоянии приходится постоянно поддерживать разность потенциалов, препятствующую увлажнению стен капиллярной водой в течение всего времени дальнейшей эксплуатации здания.
Электрофорез
Явление электрофореза, вызванное внешним электрическим полем, наблюдается, когда частицы дисперсной фазы могут свободно перемещаться в дисперсионной среде. Для изучения электрофореза используют высокодисперсные системы – золи.
Явление электрофореза - подобно электролизу, с тем отличием, что в дисперсионной среде в движении участвуют не только ионы, но и заряженные частицы дисперсной фазы.
Прибор, с помощью которого можно наблюдать электрофорез, представлен на рис. 26.
С помощью кранов колена U-образной трубки соединены с золем той же электропроводности, что и электролит. Золь подают снизу через воронку при открытых кранах. После заполнения золем колен U-образной трубки кран у воронки закрывают и замыкают электрическую цепь. Наблюдают перемещение золя к тому электроду, который имеет знак, противоположный заряду частиц дисперсной фазы.
Электрофорез широко применяется в исследовании биологических систем и в медицине (физиотерапия). С помощью электрофореза проводят разделение природных белков различной структуры, определяют степень чистоты антибиотиков и витаминов. Примером технического применения электрофореза может служить окраска кузовов автомобилей в электрическом поле высокого напряжения.
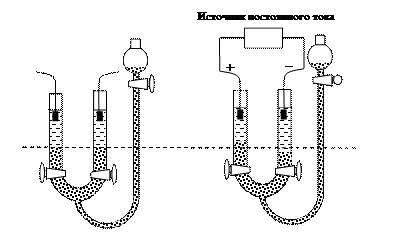
Рис. 26. Схема прибора для электрофореза: а) исходное состояние системы; при открытых кранах снизу через воронку заливают золь в колена U-образной трубки, содержащие раствор электролита; б) при закрытом кране у воронки включают источник постоянного тока и наблюдают явление электрофореза по изменению уровней золя в коленах.








