Основность органических соединений.
Органические соединения, в состав молекулы которых входят атомы азота, кислорода, серы, могут выступать в роли оснований, присоединяя протон водорода за счет неподеленной пары электронов на внешнем энергетическом уровне. Гетероатом в молекуле органического вещества, присоединяющий протон, называется центром основности.
Основания по Бренстеду делятся на n – основания и π – основания.
n – Основания могут быть нейтральными или отрицательно заряженными частицами. К ним относятся:аммониевые (R3N, R=NH, RCN), оксониевые (RC(O)R1, R-O-R1), сульфониевые (R-S-R1, RC(S)R1)
. π -основания (алкины, алкены, диены, арены) в них центром основности являются электроны π-связи. Это очень слабые основания, так как протонируемые электронные пары несвободны.
Сила основания определяется стабильностью образующегося катиона (сопряженной кислоты). Чем стабильнее катион, тем сильнее основание.
Для количественной характеристики основности обычно используют величину pK BH+ - показатель константы основности сопряженной кислоты. Чем больше pK BH+, тем сильнее основание.
Факторы, влияющие на основность
1. Природа гетероатома в основном центре
Н3С - NH2 > Н3С - OH Н3С - OH > Н3С – SH
Сила оснований зависит от электроотрицательности гетероатома в основном центре. Чем больше ЭО атома, тем слабее основные свойства, поэтому спирты и простые эфиры являются более слабыми основаниями по сравнению с аминами.
2. Строение радикала, связанного с основным центром.
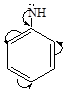 анилин Н3С → СН2 → NH2 этиламин
анилин Н3С → СН2 → NH2 этиламин
Алифатические амины проявляют более выраженные основные свойства, чем ароматические, так как электронная плотность от углеводородного радикала смещается к NH2, а чем больше электронной плотности на основном центре, тем лучше присоединяется Н+. в ароматических аминах NH2 входит в общее сопряжение с бензольным кольцом и отдает электронную плотность на кольцо, поэтому Н+ присоединяется труднее, основные свойства слабее.
3. Влияние заместителей. Электронодонорые заместители усиливают основные свойства, а электроноакцепторные – уменьшают, например:
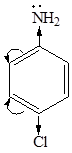 4-хлоранилин
4-хлоранилин 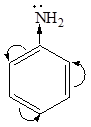 анилин
анилин 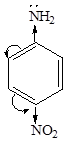 4-нитроанилин
4-нитроанилин
РКВН+ 5,1 4,6 1,0

уменьшение основности
4. Влияние растворителя
В водной среде важную роль играет уменьшение пространственных препятствий для гидратации, поэтому вторичные амины лучше гидратируются, чем третичные, которые пространственно труднодоступны.
 H3C - NH – CH3 > H3C – NH2 > H3C - N – CH3
H3C - NH – CH3 > H3C – NH2 > H3C - N – CH3
CH3
 |
основность уменьшается
В газовой среде основность возрастает с увеличением углеводородных радикалов, так как усиливается их стабилизирующее действие за счет +I-эффекта на катион сопряженной кислоты, поэтому третичные амины проявляют более сильные основные свойства по сравнению с другими аминами.
 H3C - N – CH3 > H3C - NH – CH3 > H3C – NH2
H3C - N – CH3 > H3C - NH – CH3 > H3C – NH2
CH3
 основность уменьшается
основность уменьшается
4. Теория Льюиса.
Дж. Льюисом (1923) была предложена более общая теория кислот и оснований, опирающаяся на строение внешних электронных оболочек атомов. По теории Льюиса кислотные и основные свойства соединений определяются их способностью принимать или отдавать пару электронов с образованием связи.
Кислотами Льюиса могут быть атом, молекула или катион, обладающие вакантной орбиталью и способные принимать пару электронов с образованием ковалентной связи. Примерами аогут служить галогениды элементов второй и третьей групп ПСЭ ( BF3, AlCl3, FeCl3, ZnCl2, катионы металлов, Н+. кислоты Льюиса в гетеролитических реакциях участвуют как электрофильные реагенты.
Основаниями Льюиса могут быть атом, молекула или анион, имеющие пару валентных электронов, которые они должны предоставить партнеру для образования ковалентной связи. Основания Льюиса представляют собой нуклеофильные реагенты. К ним относятся амины, спирты, простые эфиры, тиолы, тиоэфиры, соединения, содержащие π-связи или систему сопряженных π-связей.
Важным следствием теории Льюиса является то, что любое органическое соединение можно представить как кислотно-основной комплекс. Например, этилиодид можно рассматривать как комплекс, состоящий из этил-катиона С2Н5+ (кислота Льюиса) и иодид иона –I (основание Льюиса). Отсюда большинство реакций с этилиодидом можно классифицировать как обмен иодид-иона на другие основания Льюиса (ОН-, СN-, NH2-, H3C-O-) или как обмен этил-катиона на другие кислоты Льюиса (К+, Н+ и др.).
Вопросы для самоконтроля
1. Современные представления о кислотах и основаниях.
2. Теория Бренстеда-Лоури. Сопряженные кислоты и основания.
3. Кислотные свойства органических соединений с водородосодержащими функциональными группами (спирты, фенолы, тиолы, карбоновые кислоты, амины).
4. Основные свойства органических соединений. π-основания и n-основания. Теория Льюиса.
5. Факторы, влияющие на реакционную способность кислот и оснований.
6. Объясните, какое из соединений проявляет более сильные кислотные свойства и почему?
а) CH3 -SH, б) CH3-NH2, в) CH3-OH.
7. Какая кислота является более сильной и почему?
а) СH3COOH, б) Сl-CH2COOH, в) Cl2- CH – COOH.
8. Объясните, почему анилин проявляет более слабые основные свойства, по сравнению с этиламином.
9. Напишите какая из реакций доказывает более сильные кислотные свойства фенола по сравнению со спиртами:
10. В качестве антидота при отравлении солями мышьяка был предложен 2,3-димеркаптопропанол. Объясните, чем определяется его большая кислотность в сравнении с пропантриолом.








