3 .1.3 Определение общей жесткости воды
В коническую колбу наливаем 80 мл испытуемой воды, разбавленный до 100 мл дистиллированной водой. При этом суммарное содержание ионов кальция и магния во взятом объеме воды не должно превышать 0,5 ммоль. Затем прибавляем 5 мл буферного раствора, 0,1 г сухой смеси индикатора хромогена черного с сухим хлористым натрием и сразу же титруем при сильном взбалтывании 0,05 н. раствором трилона Б до изменения окраски в эквивалентной точке. Проводим три параллельных титрования.
Окраску получили синею. Появление этого окрашивания свидетельствует об отсутствии ионов 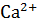 и
и 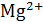 в растворе, т.е. о полном связывании их с трилоном Б.
в растворе, т.е. о полном связывании их с трилоном Б.
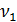 = 6,2 мл;
= 6,2 мл; 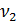 = 6,4 мл;
= 6,4 мл; 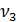 = 6,1 мл;
= 6,1 мл;
Общую жесткость воды вычисляют по уравнению (3)
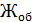 =
= 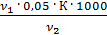
К – поправочный коэффициент к нормальной концентрации раствора трилона Б
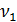 – количество трилона Б, израсходованное на титрование пробы
– количество трилона Б, израсходованное на титрование пробы
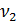 – объем воды, взятой для определения общей жесткости
– объем воды, взятой для определения общей жесткости
Для раствора трилона Б с концентрацией 0,05 н. поправочный коэффициент равен К=0,9600. Поправочный коэффициент был взят из учебника «Курс аналитической химии II том» А.П. Крешков, А.А. Ярославцев стр. 251.
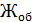 =
= 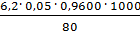 = 3,72 мг-экв/л
= 3,72 мг-экв/л
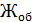 =
= 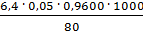 = 3,84 мг-экв/л
= 3,84 мг-экв/л
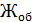 =
= 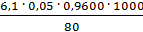 = 3,66 мг-экв/л
= 3,66 мг-экв/л
Рассчитываем среднюю общую жесткость
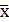 =
= 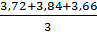 = 3,74 мг-экв/л
= 3,74 мг-экв/л
Рассчитываем относительную погрешность
ᵟ = 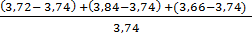 · 100%= 5,3%
· 100%= 5,3%
3.1.4 Определение рН воды с помощью стеклянного электрода
Промыть электроды и стакан для пробы дистиллированной водой. Налить в стакан для пробы исследуемый раствор. Включить прибор рН-метр. На потенциометре установить температуру раствора. Переключить mV/pH, установить в положение «рН». При помощи держателя погрузить электроды в стакан с исследуемым раствором. Запишем установившееся значение рН.
t = 21,60C
pH = 8,3
3.2 Определение показателей качества воды из Метлино
3 .2.1Определение общей кислотности воды
В коническую колбу емкостью 250 мл отмеряем пипеткой 100 мл исследуемой воды, прибавляем 3 капли фенолфталеина. Пробу титруем раствором щелочи до появления слабо-розовой окраски, не исчезающей в течение 1-2 минут. Проводим два параллельных титрования.
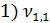 = 2,8 мл(объем щелочи, израсходованной на титрование)
= 2,8 мл(объем щелочи, израсходованной на титрование)
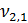 = 100 мл (объем воды, взятой для исследования)
= 100 мл (объем воды, взятой для исследования)
Н = 0,1 (нормальная концентрация рабочего раствора щелочи)
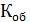 =
= 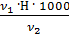 =
= 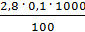 = 2,8 мг-экв/л (1)
= 2,8 мг-экв/л (1)
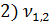 = 3,0 мл(объем щелочи, израсходованной на титрование)
= 3,0 мл(объем щелочи, израсходованной на титрование)
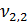 = 100 мл (объем воды, взятой для исследования)
= 100 мл (объем воды, взятой для исследования)
Н = 0,1 (нормальная концентрация рабочего раствора щелочи)
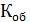 =
= 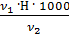 =
= 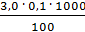 = 3,0 мг-экв/л (1)
= 3,0 мг-экв/л (1)
Рассчитываем среднюю общую кислотность
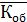 =
= 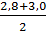 = 2,9 мг-экв/л
= 2,9 мг-экв/л








