Анализ диаграммы состояния системы медь—никель
Сплав Сu —Ni относится к сплавам—твердым растворам. Компоненты такого сплава имеют неограниченную растворимость как в жидком, так и твердом состояниях, т. е., смешиваясь между собой, образуют один тип кристаллической решетки. Общий вид диаграммы приведен на рис. 5. Линия асв на диаграмме состояния Сu – Ni называется ликвидус. Выше этой линии все сплавы данной системы находятся в жидком состоянии. Линия адв называется солидус ﴿. Ниже этой линии все сплавы находятся в твердом состоянии. Между ликвидусом и солидусом одновременно находятся две фазы: жидкий и твердый растворы. Чтобы охарактеризовать фазовое состояние конкретного сплава при заданной температуре, необходимо определить природу фаз, находящихся в равновесии при данной температуре, их химический состав и относительное количество. Для примера рассмотрим изменение фазового состояния, происходящее при снижении температуры в сплаве, содержащем 30 % Ni и 70 % Сu.
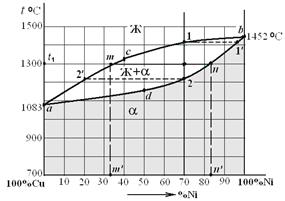
Рис. 5. Диаграмма состояния системы «медь – никель»
Для определения фазового состояния сплава в интервале кристаллизации применяют правило отрезков. Например, при произвольно выбранной температуре t1 через точку, лежащую на ординате сплава, проводят горизонтальную линию - изотерму - до пересечения с ближайшими линиями диаграммы.
Точки пересечения укажут, какие фазы находятся в равновесии у данного сплава при t1 : m – соответствует жидкому раствору, n – твердому раствору α. По проекциям точек пересечения на ось концентрации определяют химические составы равновесных фаз: в жидкой фазе содержится о m ' % Ni (остальное – Сu); в α-фазе - о n' % Ni (остальное – Сu).
Количественное соотношение равновесных фаз определяют по отрезкам: количество жидкой фазы пропорционально к n , а α-фазы -mk . Линию mn называют конодой.
При охлаждении сплава из жидкого состояния ниже точки 1, лежащей на линии ликвидус, начинается кристаллизация. При переходе через точку 2 на линии солидус кристаллизация заканчивается. В процессе кристаллизации концентрация компонентов в жидком растворе изменяется согласно ликвидусу от точки 1 до точки 2', а в растворе α – согласно солидусу от точки 1' до точки 2.
После окончания кристаллизации структура сплава состоит из зерен твердого раствора α, имеющих одинаковый состав. Поскольку сплав был выбран произвольно, то рассуждения о формировании его структуры применимы к любому сплаву этой системы, кроме чистых Cu и Ni.
Применение сплавов
Сплавы – смеси применяются в качестве:
1. Литейных, т.к. они обладают хорошей жидкотекучестью, из-за наличия в их составе эвтектики.
2. Припоев для пайки.
3. Тепловых предохранителей, т.к. сплавы при любой концентрации имеют одинаковую температуру начала плавления, что обеспечивает точность срабатывания предохранителей при повышении температуры в помещении до заданных значений.
4. Типографских шрифтов (доэвтектический сплав Pb-Sb)
5. Подшипников скольжения (баббиты), состоящие из
мягкой основы – эвтектики и твердых включений, мягкая основа обеспечивает хорошую прирабатываемость подшипника к валу, а твердые включения—высокую износостойкость.
Сплавы – твердые растворы применяются в качестве:
1. Коррозионностойких (нержавеющих), что обеспечивается их однофазной структурой;
2. Электросопротивлений, реостатной проволоки (Сu - Ni, Ni - Мn), нагревательных элементов электроприборов (Ni - Сr, Fе-Сr). Высокое электросопротивление имеет место из-за наличии в кристаллической решетке металла—растворителя чужеродных атомов растворенного металла.
Микроструктуры сплавов:
Pb – Sb



х135 х135 х135
доэвтектический (Pb+Э) эвтектический (Э) эвтектический (Pb+Э)
С u – Ni


х135 х135
литой деформированный и отожженный
Задание. Построить кривую охлаждения для сплава Pb – Sb заданной концентрации
| Вари- ант | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| Sb, % | 1,5 | 5 | 9 | 12 | 15 | 18 | 19 | 25 | 29 | 36 | 42 | 59 | 65 | 69 | 73 | 82 | 86 | 92 | 95 | 2,5 | 10 | 100 |
ЛАБОРАТОРНАЯ РАБОТА № 4
АНАЛИЗ ДИАГРАММЫ СОСТОЯНИЯ








