Предварительное цианирование
Операция предварительного цианирования проводится в 6-секционном аппарате выщелачивания. Для удобства пользования и нумерации каждую секцию называют пачуком. Из первого пачука во второй пульпа попадает через нижнее отверстие в перегородке, из второго в третий пачук — через верхнюю кромку перегородки переливом, в четвертый — через нижнее отверстие в перегородке и т.д. Такое движение пульпы в пачуках цианирования позволяет исключить проскок непроцианированного материала.
В 1-й пачук подается крепкий раствор цианистого натрия насосом-дозатором, установленным у расходного чана цианидного раствора в реагентном отделении. Дозировка цианистого раствора производится в таком количестве, чтобы в пульпе поддерживать концентрацию NaCN не менее 0,25-0,3%. Цианирование проводится в режиме интенсивной аэрации и перемешивания воздухом пульпы.
При проведении операции предварительного цианирования очень важно следить, чтобы в процесс подавалась пульпа с плотностью не менее 50% тв., в противном случае при перемешивании сжатым воздухом в пачуках начинается обильное пенообразованис, что мешает обслуживанию и не позволяет нормально контролировать процесс.
Извлечение золота в раствор пульпы при предварительном цианировании составляет не менее 50-60%.
Растворение золота проходит очень быстро и через два часа концентрация золота в растворе пульпы достигает 50-60 г/м3 при содержании золота в концентрате 100 г/т. Если из концентрата за 2-4 часа растворяется более 50% золота, то не имеет смысла вести процесс цианирования дольше, так как дальше происходит уменьшение скорости растворения золота, но зато начинают активно взаимодействовать с цианидом медные и цинковые минералы. В 1-й пачук цианирования подается раствор цианида с концентрацией 20% по NaCN.
Десорбция металлов с угля
В процессе сорбционного выщелачивания уголь, перемещаясь от последнего аппарата сорбции навстречу потоку пульпы, насыщается золотом, серебром, а так же ионами тяжелых металлов. Наряду с этим, к концу сорбции присутствующие в жидкой фазе пульпы простые CN- ионы, а также кремнезем, масла, ксантогенаты и другие растворимые органические вещества подавляют сорбционную активность угля, забивая поры сорбента.
Такой уголь необходимо выводить из процесса и, либо сжигать с последующей плавкой на черновой слиток золота, либо подвергать регенерации, обрабатывая растворами реагентов с целью снятия с него благородных металлов. Так как сжигать уголь нерационально из-за его высокой стоимости, то в большинстве случаев уголь подвергается регенерации. В настоящее время основным методом десорбции металлов с угля, который широко применяется на ЗИФ, является процесс элюации. Вещества, с помощью которых с угля десорбируются металлы, называются элюентами. Наиболее рациональными и эффективными элюентами, нашедшими применение на практике признаны цианистый натрий, едкий натр, жидкий безводный аммиак.
Наиболее простейшим и менее опасным элюентом является гидроксид натрия NaOH. Раствор, содержащий 4-6 г/л едкого натра, подогревается в автоклаве до температуры 175-185°С с одновременным повышением давления среды и прокачивается через герметичный аппарат с насыщенным углем. Процесс элюации благородных металлов длится 50-70 минут. Действие гидроксильных ионов в процессе десорбции объясняется следующим образом: ионы ОН- нейтрализуют на поверхности угля активные группы основного характера, но, с другой стороны, ионизируют кислые поверхностные группы угля. Благодаря этому уголь приобретает в целом отрицательный заряд, который вследствие проводниковых свойств угля распространяется на весь его каркас. В результате этого, за счет действия электростатических сил отрицательно заряженные анионы золота Au(CN)2- и серебра Ag(CN)2- отталкиваются с поверхности угля в объем раствора. При указанных условиях в элюат переходит 98-99% золота и 80-90% серебра.
20.2.3 Регенерация угля
Снять с активного угля золото и серебро методом высокотемпературной десорбции еще не значит восстановить его сорбционные свойства. После десорбции на поверхности и в порах угля остаются различные примеси, адсорбированные из цианистого раствора пульпы, органические вещества, тонкие шламы и илы, остатки реагентов и масел.
Отрицательное влияние щелочи при высокой температуре процесса десорбции объясняется тем, что попавшие в поры угля тонкие шламы силикатов и алюмосликатов частично растворяются, образуя гели, закупоривающие поры угля. Для удаления из пор угля гелей и тонких шламов в конце автоклавной десорбции проводится резкий сброс давления из аппарата десорбции до атмосферного. Резкое снижение давления приводит посредством вывода парожидкостной фазы к вскипанию жидкости в порах и выбросу из них вместе с паровой фазой шламов и образовавшихся гелей. Оптимальная скорость снижения давления в аппарате десорбции составляет – 0,15-0,5 кг/см2/с, при 2-3-х кратном повторении.
Осуществление операции сброса давления наряду с удалением шламов из пор угля позволяет интенсифицировать скорость десорбции в конце процесса и снизить остаточные содержания золота и серебра в угле за счет осуществления конвективного (механического) переноса благородных металлов из фазы сорбента в объем элюирующего раствора. При использовании в пульповом процессе известкового молока в качестве защитной щелочи поры угля кальцинируются (на стенках пор осаждаются карбонат кальция). С течением времени поры угля полностью зарастают карбонатом кальция, что приводит к снижению удельной поверхности угля и, как следствие, к снижению скорости сорбции и рабочей емкости по золоту. Для очистки пор угля от кальция применяется обработка угля раствором соляной кислоты. Оптимальной концентрацией является 0,7-1% раствор. Десорбция кальция проводится в колонне с углем 1-3 объемами указанного раствора в течение 1-1,5 часа. При этом с угля десорбируется 80-85% кальция. Кислотная обработка угля проводится после автоклавной десорбции золота и серебра. Если кальция в растворе пульпы содержится много, то кислотную обработку включают в постоянную схему регенерации угля; если кальция в растворе сравнительно немного, то кислотную обработку включают в схему периодически по мере кальцинации угля.
Реактивация угля
Необходимость реактивации обуславливается тем, что при элюации золота растворами не удается вымыть из угля адсорбированные масла, ксантогенаты, кремнистые соединения, большая часть которых на угле находится в нерастворимом виде.
Реактивация угля проводится путем его обжига при температуре 650-700°С в водно-газовой среде. В этом случае все органические загрязнители угля, особенно флотационные реагенты и гумминовые кислоты, полностью выжигаются. При обжиге на поверхности угля в водно-газовой среде восстанавливаются функциональные радикалы, способные к возобновлению обмена ионов в пульпе.
Реактивацию угля проводят в специальных ретортных вращающихся печах (рис. Рисунок 76) в непрерывном режиме с подачей в печь воды или пара. При проведении реактивации решающим фактором для удаления органики и восстановления активности угля являются температура и водно-газовое взаимодействие, которое устанавливается опытным путем.

Рисунок 76 – Печь для реактивации угля
Электрическая печь для реактивации угля состоит из толстостенной трубы (реторты), изготовленной из нержавеющей жаропрочной стали с внутренним диаметром 325 мм и длиной 6,5 м. Реторта помещается в нагревательную камеру. Вращение реторты осуществляется электроприводом. Нагревательная камера представляет собой кожух из листовой стали, внутри которого помещаются нагреватели. Нагреватели теплоизолированы от наружной стенки кожуха легким огнеупорным кирпичом. Реторта с нагревательной камерой смонтирована на мощной опорной конструкции, предусматривающей изменение угла наклона реторты.
В загрузочное устройство печи входят бункер угля вместимостью 1000 л и шнековый питатель для подачи угля из бункера в реторту. Шнековый питатель приводится в действие электродвигателем постоянного тока через клиноременную передачу. Достоинством электропривода является то, что им можно изменять число оборотов шнека, тем самым регулируя количество подаваемого угля в реторту, т.е. имеется возможность регулировать производительность печи по углю.
При вращении реторты уголь перемещается к загрузочному концу, проходя три зоны нагрева, в каждой из которых происходят определенные превращения угля. В 1-й зоне нагрева при температуре 550-600°С происходит испарение воды из пор угля и образование водяного пара. Во второй зоне нагрева при температуре 650°С идет пиролиз — разложение органических веществ под действием высоких температур. Органические вещества, находящиеся в порах угля, разлагаются с образованием и выделением летучих веществ в паровоздушный поток, который движется по реторте. При этом в порах происходит образование реакционноспособного углерода.
В третьей зоне при температуре 550°С перегретый водяной пар взаимодействует с реакционноспособным углеродом, в результате чего происходит разблокирование поровой структуры угля. Из третьей зоны уголь поступает в разгрузочное устройство, где охлаждается до температуры 200-250°С, после чего высыпается в контейнер.
Образующиеся летучие вещества в составе паровоздушной смеси на выходе из реторты через специальный патрубок отсасываются вытяжной вентиляцией.
Процесс реактивации угля в печи осуществляется в непрерывном режиме. Производительность печи по углю от 50 до 100 кг в час.
Реактивация угля имеет несомненные преимущества и существенным образом повышает эффективность использования активированного угля.
Цианистая обработка и очистка угля от меди
Если активный уголь в процессе сорбции получил значительное насыщение цианистыми ионами меди и цинка, то его перед десорбцией золота обрабатывают 1%-ным раствором цианида при комнатной температуре в течение 2-3 часов. Эта операция называется "холодная" десорбция и с её помощью уголь очищают от цинка и меди. После проведения холодной десорбции получающийся при высокотемпературной элюации золотосодержащий элюат содержит в основном золото и серебро и при последующем его электролизе получается более высокопробный по драгметаллам катодный осадок.
Холодную десорбцию насыщенного угля необходимо проводить только в том случае, когда в этом есть необходимость. Если содержание названных металлов сравнительно невелико и составляет не более 50% рабочей емкости угля по золоту и серебру, то холодную десорбцию проводить необязательно.
Аппаратурная схема процесса сорбции представлена на рисунке Рисунок 77. Для повышения емкости сорбента поступающую на сорбцию пульпу подвергают предварительному цианированию.
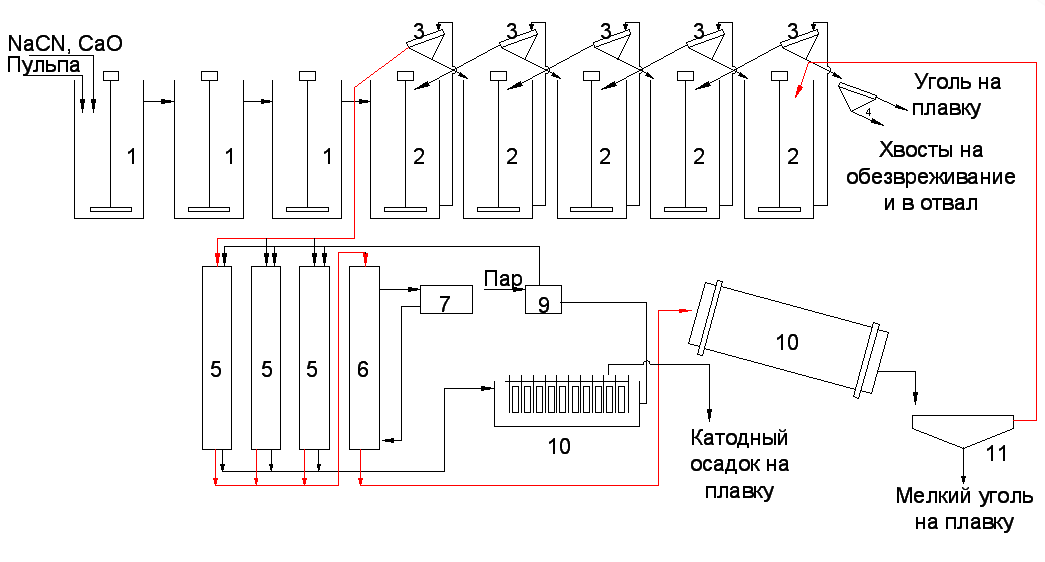
Рисунок 77 – Схема сорбции из пульпы с применением активного угля. 1 – аппараты для предварительного цианирования; 2 – аппараты для сорбционного выщелачивания; 3 - грохоты для разделения угля и пульпы; 4 - контрольный грохот; 5 – колонны для элюирования; 6 – колонный для кислотной обработки угля; 7 – чан для кислоты; 8 – электролизная ванна; 9 – теплообменник; 10 – барабанная печь; 11 – грохот (красным показано движение угля, черным движение пульпы, раствора).
Последующий процесс сорбционного выщелачивания ведут в цепочке из 5-10 аппаратов с пневматическим или механическим перемешиванием при противоточном движении угля и пульпы. Размер зерен угля от 1,2 до 3,4 мм. Сорбцию ведут из пульп, содержащих 40-45% твердого, при концентрации цианида 0,01-0,02%, рН 10-10,5 и единовременной загрузке сорбента 10-30 г/л. Растворы пропускают через слой активированного угля снизу вверх в колоннах.
Одну или две колонны после заполнения гранул активированного угля золотом отключают из цепочки осаждения и переключают на цикл снятия золота с угля (десорбция) и регенерации (активации) угля. В этом цикле горячие (90-100 °С) растворы цианида натрия и щелочи под небольшим избыточным давлением [50—100 кПа (0,5— 1,0 атм)] пропускают через колонны с золотосодержащим активированным углем, при этом осажденное золото растворяется и переходит в более концентрированный золотосодержащий раствор (100-300 мг/л). Выделение золота из богатых по золоту растворов осуществляют посредством электролиза, при этом золото осаждается на специальном катоде (вата из тонкой проволоки нержавеющей стали). Катодное золото (80—90 % чистоты) плавят с флюсами на черновое золото (сплав Доре) с содержанием 96-98 % (рис. Рисунок 78, Рисунок 79).
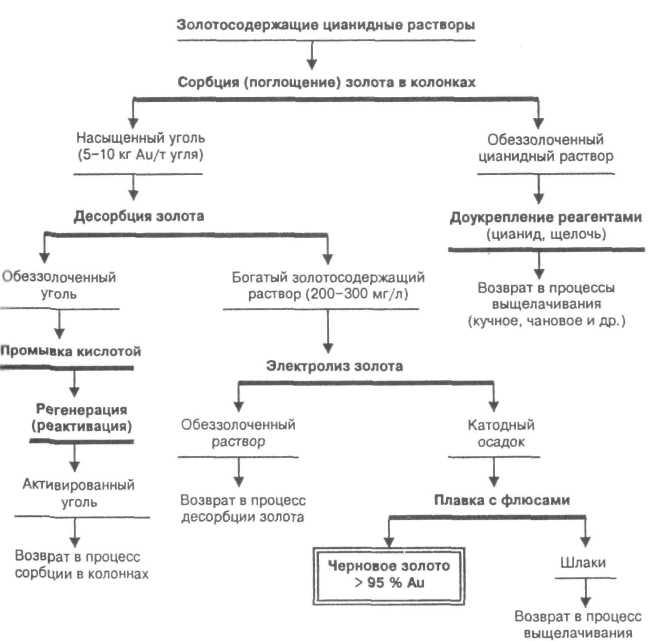
Рисунок 78 - Технологическая схема переработки растворов KB на активированных углях

Рисунок 79 – Нижне-Якотинсокое золото на катодах электролизера
Активированный уголь без золота после десорбции поступает в цикл регенерации (активации) для восстановления его первоначальных свойств с последующим возвращением в цикл осаждения золота в системе сорбционных колонн.
20.3 Сорбция на смолу
В России на некоторых предприятиях используют ионообменные смолы, представляющие собой синтетические высокомолекулярные соединения на основе стирола и дивинилбензола с различными функциональными группами, которые способны в водных растворах поглощать ионы различного заряда.
К преимуществам ионообменных смол перед активированным углем относят следующие:
- более высокую степень насыщения смол до 20-30 кг/т смолы по сравнению с 3—5 кг/т для угля;
- значительную скорость реакции и извлечения золота из растворов - уменьшение продолжительности процесса в 3—5 раз, что обусловливает соответственно сокращение массы сорбента и объема сорбционного оборудования;
- более высокую степень извлечения из продуктивных растворов - остаточное содержание в растворах 0,01-0,03 мг/л для смол по сравнению с 0,1 мг/л для углей.
Сорбенты (иониты) – это твердые вещества, которые благодаря наличию в них ионообменных групп, способны обменивать свои ионы на ионы, присутствующие в растворах.
Иониты делятся:
1) природные (цеолиты, монтморилловые, глаукониты);
2) синтетические (неорганические – пермутиты, органические - смолы).
Смолы стойки по отношению к растворам кислот и щелочей. Различают катиониты, аниониты и амфолиты (амфотерные иониты).
Ионит, способный к обмену катионов, называется катионитом:
2NaR+CaCl2→CаR2+2NaCl.
Ионит, способный к обмену анионов, называется анионитом:
2RCl+H2PtCl6→R2PtCl6+2HCl.
Амфолиты проявляют высокую избирательность к катионам металлов, т.к. образуют с последними комплексы хелатного типа, например:
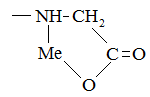
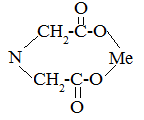
У катионитов фиксированные катионы –SO3-, COO-, -PO32-, -AsO32- и др., у анионитов –NH3+, =NH23+, ≡NH+, ≡N+.
Фиксированный ион связан с противоином и образует с ним ионообменную группу, которую часто называют активной или функциональной группой.
Активными группами являются: -SO3H, -SO3Na, -COOH, -PO3H2, -AsO3Na2, -NH3Cl, ≡NOH и др.
По степени диссоциации активных групп различают сильнокислотные катиониты (активные группы -SO3H и -PO3H2) и слабокислотные (активные группы -COOH). Аналогично этому различают высокоосновные и низкоосновные аниониты.
Высокоосновные аниониты содержат в качестве активных групп хорошо диссоциирующие четвертичные аммониевые или пиридиниевые основания.
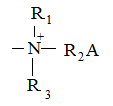 или
или 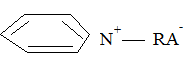
где R, R1, R2, R3 – углеводородные радикалы (каркас); А – анион соли.
Подобные смолы способны к обмену анионов не только в кислых, но и в щелочных средах.
Низкоосновные аниониты содержат первичные, вторичные и третичные аминогруппы, которые являются слабыми основаниями и диссоциируют лишь при рН<7.
Для синтеза ионообменных смол используют процессы полимеризации или поликонденсации стирола и дивинилбензола с последующим сульфированием или аминированием полимеров.
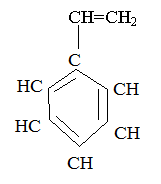
Стирол (получают из этилена и бензола)
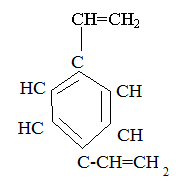
Дивинилбензол (винил – радикал этилена СН2=СН-)
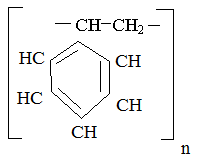
Полистирол
При связывании цепей поперечными связями с помощью дивинилбензола образуется нерастворимый стирол в виде гранул.
Гранулы полистирола обрабатывают концентрированной серной кислотой (сульфируют), при этом образуются сульфокислоты – катиониты с ионной сульфогруппой –SO3H:
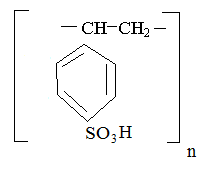
Сильнокислотный сульфокатионит (KY-2)
При обработке аминированием хлорметилирового полистирола получает низкосоновные аниониты с первичными, вторичными и третичными аминогруппами
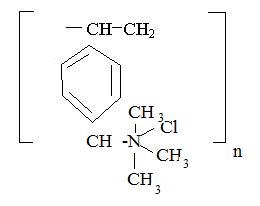
Хлорметиллированный сополимер стирола и дивилбензола, аминированный триметиламином (третичным амином). Высокоосновный ионит АВ-17.
Основной формой нахождения элементов в растворах KB являются цианидные комплексы [Au(CN)2]-, [Ag(CN)2]-, [Cu(CN)3]2-, [Zn(CN)4]2- и т.д. Все эти соединения будут сорбироваться смолой АМ-2Б благодаря протеканию процессов
R-OH+ [Ме(СN)4]k- <=> R - [Me(CN)4]k- + ОН-
R-CN+ [[Ме(СN)4]k- <=> R- [Me(CN)4]k- + CN-.
При равных молярных концентрациях элементов в растворе смола АМ-2Б имеет следующий ряд сродства элементов: Аu > Zn > Ni > > Ag > Сu > Fe.
При сорбции из растворов цианидные комплексы связываются с матрицей ионообменной смолы с различной прочностью.
Параметрами, характеризующими прочность связи аниона со смолой, являются:
1) заряд комплексного цианидного аниона. Наиболее прочно связаны со смолой однозарядные анионы [Au(CN)2]-, [Ag(CN)2]-. С увеличением заряда аниона прочность связи снижается. Поэтому такие комплексы, как [[Cu(CN)3]2-, [Zn(CN)4]2- легче десорбируются со смолы при различных операциях (кислотная отмывка, тиомочевинная десорбция), чем соединения золота и серебра.
2) размер комплексного цианидного аниона. Соответствие размеров иона и диаметра каналов (пор) в зерне ионообменного материала определяет прочность связи комплексного цианидного аниона со смолой. Смола "Россион-12" синтезирована таким образом, чтобы размер пор в ее матрице максимально соответствовал размеру аниона [Au(CN)2]-. Таким образом, при обработке смолы "Россион-12" растворами H2SO4 в первую очередь будут десорбироваться примеси-соединения Zn, Сu, Ni и Со. Десорбция ионов [Au(CN)2]-, [Ag(CN)2]- в этом случае происходить не будет.
Для десорбции Au(I) и Ag(I) со смолы используют химическое разложение цианидных комплексов кислыми растворами тиомочевины:
[Au(CN)2]-+ 2SCN2H4 + 2H+ → 2HCN↑ + [Au(SCN2H4)]2+,
[Ag(CN)2]-+ 2SCN2H4 + 2H+ → 2HCN↑ + [Ag(SCN2H4)]2+.
Поскольку тиомочевинный комплекс золота является менее прочным, разрушение комплексного цианидного аниона [Au(CN)2]- и переход его в комплексный цианидный катион [Au(SCN2H4)]2+ осуществляют с добавлением кислоты. Кислота способствует разрушению цианидного комплекса.
Нагревание способствует процессу замещения аниона CN- нейтральной молекулой SCN2H4, благодаря удалению выделившегося HCN из реакционной сферы в газовую фазу. Таким образом, происходит превращение сорбированного аниона [Au(CN)2]- в катион [Au(SCN2H4)]2+.
Последний не может удерживаться в фазе смолы и переходит в раствор.
Из кислот для указанной цели подходят любые сильные неокисляющие кислоты (НСl, H2SO4 и др.), но из экономических соображений, а также для уменьшения коррозии оборудования используют серную кислоту.
Анионообменные смолы по сравнению с активированными углями обладают более высокими механической прочностью и кинетическими характеристиками. Для десорбции смол не требуется повышенного давления и высоких температур. Смолы не подвержены "отравлению" органическими веществами и карбонатом кальция, для восстановления сорбционных свойств они не требуют термической реактивации.
Существенное упрощение схемы регенерации анионообменных смол можно ожидать при использовании низкоосновных смол, так как для регенерации насыщенной металлами смолы достаточно в этом случае провести ее обработку при температуре 50-60 °С щелочным раствором следующего состава: 10 г/л NaOH и 1 г/л NaCN. Десорбция золота и регенерация сорбента совмещены в одной операции щелочной обработки.
20.3.1 Основные характеристики ионообменных смол
1 Набухание
Воздушно-сухие иониты, выпускаемые промышленностью, состоят из твердых гранул или бусин размером от 0,5 до 3—4 мм. При погружении в воду иониты набухают вследствие поглощения определенного количества воды. Набухание сопровождается растяжением пространственной сетки смолы и увеличением ее объема (иногда в несколько раз). Способность к набуханию зависит от числа ионогенных групп и поперечных связок. С увеличением числа поперечных связок набухаемость уменьшается (возрастает жесткость каркаса). В случае жесткой структуры стремление к набуханию может привести к растрескиванию смолы.
Проникновение воды в поры ионита обусловлено стремлением ионов, находящихся в порах смолы в высокой концентрации, к гидратации. Набухание характеризуется коэффициентом набухания, равным отношению удельного объема набухшей смолы к удельному объему смолы в исходной форме.
Кроме того, определяют «весовое набухание» — количество поглощенной воды на 1 г сухого ионита.
2 Обменная емкость (или ионообменная способность) смолы
Полная обменная емкость (ПОЕ) характеризует максимальное количество ионов, которое может быть поглощено смолой при ее насыщении. Это постоянная для данной смолы величина, которую можно определить либо в статических, либо в динамических условиях.
Динамическая (рабочая) обменная емкость (ДОЕ) — количество ионов, поглощенных смолой при фильтрации раствора через слой ее до проскока сорбируемого иона.
Рабочая емкость определяется по выходной кривой (Рисунок 80). Она также не является постоянной величиной — зависит от скорости пропускания раствора через смолу, величины зерен смолы и состава раствора.
Площадь, ограниченная выходной кривой и осями координат (S1+S2), отвечает полной динамической обменной емкости (ПДОЕ), площадь S1 соответствует рабочей емкости (до проскока).
Процесс десорбции поглощенного на смоле иона называют элюированием. При осуществлении элюирования в динамических условиях (в колонне) выходная кривая элюирования имеет вид, показанный на рис.Рисунок 80. В результате элюирования поглощенных ионов, если смола достаточно «нагружена», получают элюаты с концентрацией металла в 100 и более раз выше, чем в исходных растворах. Так, например, при исходной концентрации молибдена 0,2—0,3 г/л получают элюаты с содержанием 80-100 г/л Мо (т.е. концентрирование в 300-500 раз). Из растворов содержащих 0,5-2 г/л U, получают растворы с содержание 60-70 г/л U.
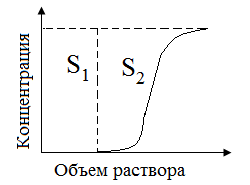
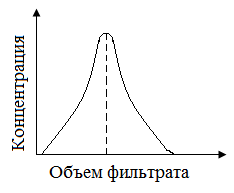
Рисунок 80 - Рабочая емкость, кривая элюирования
Операции сорбции и регенерации можно проводить в одних и тех же аппаратах (колоннах) без перегрузки смолы. При использовании низкоосновных смол снижаются капитальные и эксплуатационные затраты в сравнении с применением активированных углей и смол типа АМ-2Б и "Россион-12".
20.3.2 Сорбционное оборудование
Принципиально оборудование для проведения сорбционного процесса извлечения благородных металлов одинаково для смол и углей. Это колонны разного объема, выполненные из различных материалов в зависимости от агрессивности применяемых выщелачивающих растворов. Например, для цианидных растворов используют обычную углеродистую сталь.
Большой объем перерабатываемых продуктивных растворов определяет высокие скорости потока растворов в колоннах, достигающие 60 м3/ч на 1 м2 поперечного сечения колонны.
Обычно в цикле сорбционного извлечения золота из продуктивных растворов для более полного насыщения сорбента процесс проводят непрерывно в трех колоннах в противоточном режиме: растворы поступают в колонну № 1, проходят последовательно далее колонны № 2 и № 3, а сорбент (уголь, смола), свежий или отрегенерированный, загружают в колонну № 3 и затем последовательно порциями перегружают из колонны № 3 до колонны № 1.
Насыщенный золотом сорбент выводят из колонны № 1, объединенный раствор после выхода из колонны № 3 направляют в оборот на кучное выщелачивание после доукрепления реагентами. Насыщенная смола из колонны № 1 поступает в цикл элюирования — регенерации — выделения золота в виде чернового металла.
Элюирование или десорбцию золота с насыщенной смолы проводят в таких же аппаратах-колоннах с обработкой смол различными десорбирующими растворами. Так, для селективной десорбции золота используют растворы тиомочевины (80-90 г/л) в серной кислоте (20-30 г/л) при температуре 60 °С.
Кроме того, в случае высокого содержания примесей в рудах и продуктивных растворах осуществляют селективную десорбцию примесей:
- меди, цинка и никеля — растворами серной кислоты перед десорбцией золота;
- серосодержащих примесей — растворами едкого натра после десорбции золота перед возвращением смолы на стадию сорбционного извлечения.
В этом и заключается регенерация ионообменной смолы, т.е. восстановление ее сорбционных способностей для обеспечения высоких показателей работы в сорбционном процессе извлечения золота из продуктивных растворов.
Растворы после десорбции золота в зависимости от содержания его на смоле имеют концентрацию по золоту от 0,5 до 2 г/л и вступают в стадию выделения товарного продукта — чернового металлического золота. Эта стадия включает в себя следующие операции:
- осаждение гидратов растворами едкого натра и фильтрация осадка с возвратом растворов тиомочевины на стадию десорбции золота;
- удаление примесей из осадка посредством обработки раствором серной или азотной кислоты;
- сушка осадка, смешивание с флюсами и плавка в печах при температуре 1200 °С с получением слитков чернового металлического золота (серебра) или их сплава — сплава Доре.








