Величина внутренней энергии определяется состоянием внутренней энергии – поэтому внутреннюю энергию называют функцией состояния.
Изменение внутренней энергии в термодинамическом процессе не зависит от пути процесса, зависит от исходного и конечного состояния системы. 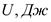
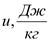 .
.
Для идеального газа внутренняя энергия зависит только от температуры.
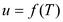 ;
; 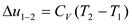
Энтальпия представляет собой сумму внутренней энергии и потенциальной энергии, внешнего давления.
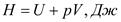 ;
; 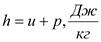 ( удельная энтальпия).
( удельная энтальпия).
Энтальпия есть функция состояния: .
17. Первый закон термодинамики
Первый закон термодинамики является частным случаем закона сохранения энергии: теплота, подведенная к термодинамической системе, расходуется на увеличение внутренней энергии и совершение работы.
Аналитические выражения первого закона термодинамики:
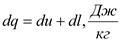 - дифференциальная форма;
- дифференциальная форма;
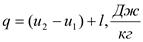 -для конечного процесса, на 1 кг вещества;
-для конечного процесса, на 1 кг вещества;
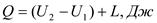 ,- для произвольного количества вещества;
,- для произвольного количества вещества;
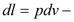 для бесконечно малого процесса.
для бесконечно малого процесса.
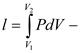 работа изменения объема
работа изменения объема
Выведем уравнение первого закона термодинамики во второй форме, то есть через энтальпию:
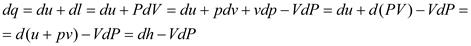
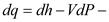 для элементарного процесса.
для элементарного процесса.
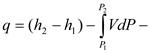 для конечного процесса
для конечного процесса
18.Энтропия, её физический смысл и свойства
Энтропия есть мера деградации энергии, мера рассеяния энергии. S, Дж/К
Увеличение энтропии термодинамической системы в элементарном обратимом процессе.
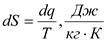 ,
,
где 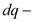 теплота, передаваемая термодинамической системе,
теплота, передаваемая термодинамической системе, 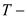 температура.
температура.
Приращение энергии в конечном обратимом процессе.
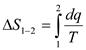
Физические свойства:
-энтропия изолированной системы не изменяется, когда в системе протекают обратимые процессы;
-энтропия возрастает, когда в системе протекают необратимые процессы;
-переход термодинамической системы от неравновесного состояния к равновесному, сопровождается ростом энтропии;
-в равновесном состоянии энтропия достигает максимума;
-энтропия сложной системы равна сумме энтропий компонентов.
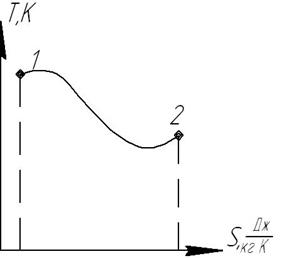
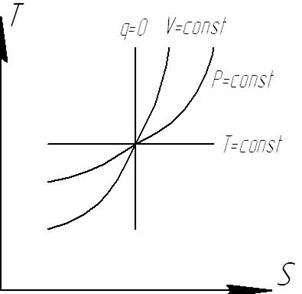
19. Расчетные зависимости изменения энтропии в различных процессах.TS диаграмма
• изохорный процесс 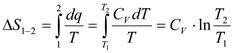
• изобарный процесс 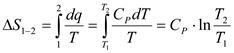
• изотермический процесс 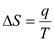
• адиабатный обратимый процесс 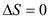
• политропный процесс 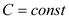 ;
; 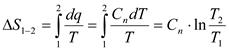
Изменение энтропии идеального газа:
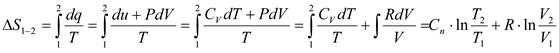
изменение энтропии газа через другие основные параметры состояния:
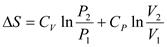 ;
; 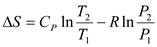
Если условно принять уровень отсчета на котором энтропия равна нулю, то, пользуясь формулами можно вычислить абсолютную энтропию в любом состоянии термодинамической системы. За уровень отсчета обычно принимают нормальные условия. 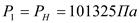 ;
; 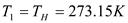 ;
; 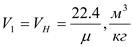 .
.
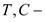 диаграмма
диаграмма
20. Круговые термодинамические процессы. Прямой цикл, термический КПД. Обратный цикл, холодильный коэффициент.
При однократном расширении рабочего тела можно выполнить органическую работу. Для повторного расширения рабочее тело нужно вернуть к исходному состоянию (сжать). При многократном расширении и сжатии, то есть совершении кругового термодинамического процесса можно получить любое количество работы.
Необходимые условия работы тепловой машины:
• наличие рабочего тела;
• наличие теплоисточника и теплоприемника;
• цикличность работы.
Изображение цикла в 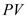 координатах:
координатах:
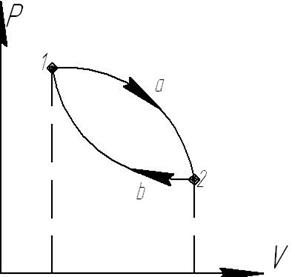
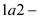 расширение рабочего тела с теплоподводом
расширение рабочего тела с теплоподводом 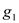 ;
;
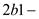 сжатие рабочего тела с теплоотводом
сжатие рабочего тела с теплоотводом 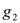 .
.
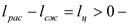 в прямом цикле работа положительна.
в прямом цикле работа положительна.
В результате полного цикла после возвращения системы к исходному состоянию, все параметры, включая внутреннюю энергию, примут первоначальные значения. Поэтому, на основании первого закона термодинамики работа цикла равна теплоте переданной рабочему телу: 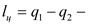 работа цикла.
работа цикла.
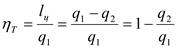
Изобразим обратный цикл в 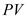 координатах:
координатах:
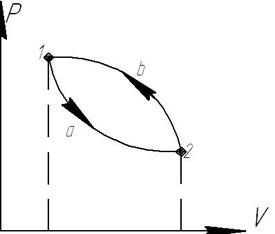
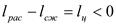
По обратному циклу работают компрессионные установки, холодильные установки. Основная термодинамическая характеристика – холодильный коэффициент:
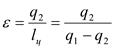 .
.








